Foram encontradas 13.432 questões.
Abaixo estão representados cinco frascos contendo soluções aquosas diluídas dos compostos indicados.
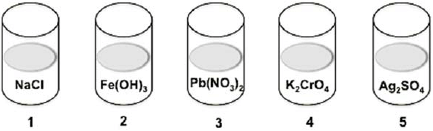
Gotejando solução de HCl 1M sobre cada uma dessas cinco soluções, haverá a formação de precipitado somente nos frascos
Provas
Observe o esquema abaixo.

O esquema representa de forma abreviada as reações químicas do ciclo do cobre. As etapas em que o cobre é, respectivamente, oxidado e reduzido são as
Provas
Trifluoreto de boro reage com boridreto de sódio e produz tetrafluorborato de sódio e diborano, que, ao reagir com o oxigênio do ar, produz óxido de boro e água, como representado nas equações químicas não balanceadas:
!$ BF_3(g) !$+!$ NaBH_4(s) !$!$ → !$!$ NaBF_4(s) !$+!$ B_2H_6(g) !$
!$ B_2H_6(g) !$+!$ O_2(g) !$!$ → !$!$ B_2O_3(s) !$+!$ H_2O(I) !$
Partindo-se de 111 gramas de boridreto de sódio e considerando que este é o reagente limitante e, ainda, que o rendimento da reação é 90%, a massa, em gramas, de óxido de boro produzido será
Massas Molares (!$ g·mol^{-1} !$): Na=23 ; B=10 ; O=16 ; H=1
Provas
Entre os ácidos inorgânicos, cujas fórmulas são citadas, o único classificado como diácido é o
Provas
Considere a reação química a seguir
!$ HNO_2(aq)\,+\,HPO_4\,^{2-}(aq) \rightleftharpoons NO_2\,^-(aq)+H_2PO_4\,^{-}(aq) !$
De acordo com a teoria ácido-base de Bronsted-Lowry, nessa reação o
Provas
Uma amostra de sulfato cúprico hidratado pesando 125,2 g foi seca em estufa a 110ºC para remover toda a água de hidratação. Após a secagem, a amostra pesou 80,0 g. Então a fórmula do sal hidratado em questão é
Massas Molares (!$ g·mol^{-1} !$): Cu=63,5; S=32; O=16; H=1
Provas
Uma amostra de volume “a” mL de solução de um ácido monoprótico foi titulada com solução !$ { \large c \over 10} !$ molar de uma monobase, usando-se como indicador a fenolftaleína. O ponto de viragem foi observado quando foram consumidos “b” mL da solução titulante. Então, a concentração normal da solução titulada (!$ N_t !$) pode ser expressa por
Provas
O técnico encontrou no laboratório de química dois frascos, “A” e “B”, contendo líquidos em seus interiores. Nos rótulos dos dois frascos estava escrito apenas a fórmula !$ C_3H_6O !$. Como existem compostos orgânicos distintos, um aldeído e uma cetona, com essa fórmula molecular, o técnico colocou em tubos de ensaio distintos alíquotas dos dois líquidos e, em seguida, gotejou reagente de Tollens (solução de !$ Ag^+ !$ em amônia aquosa) sobre cada uma das duas alíquotas contidas nos tubos de ensaio. Notou a formação de uma película prateada somente no tubo de ensaio que continha o líquido do frasco “A”. Então, o líquido que está no frasco “A” é o(a)
Provas
Dispõe-se em estoque de um frasco contendo !$ HC_2H_3O_2 !$ concentrado (massa molar 60,05 g·!$ mol^{-1} !$, densidade 1,05 g·!$ cm^{-3} !$ e % p/p 99,5) e deseja-se preparar 1 litro de solução 0,1N desse ácido. O volume, em mL, do ácido concentrado que deve ser utilizado no preparo dessa solução é
Provas
Para realizar uma titulação ácido-base, além de reagentes, indicador, bureta e erlenmeyer, é necessário utilizar um(a)
Provas
Caderno Container