Foram encontradas 13.431 questões.
Texto 8A1-II
O SO2Cl2 (g) decompõe-se facilmente de acordo com a equação:
!$ SO_2 Cl_2(g) \rightleftharpoons SO_2(g) + Cl_2(g)\,\,\,\triangle H>0 !$
Por esse motivo, ele é muito empregado como fonte de Cl2 (g) em reações químicas.
Considere que todas as espécies gasosas envolvidas nessa reação apresentem comportamento ideal e que a lei de velocidade para a reação seja dada pela equação v = k × [SO2Cl2]. Considere também que, na temperatura em que a reação ocorre (T), a constante de equilíbrio (Keq) da reação valha 0,40.
Considerando-se as informações do texto 8A1-II, se, inicialmente, houver SO2Cl2 (g) à pressão parcial inicial de 1,50 bar em um sistema fechado isento de SO2 (g) e Cl2 (g), então a pressão parcial do SO2Cl2 (g), quando atingido o equilíbrio químico à temperatura T, será igual a
Provas
Em uma expansão isotérmica reversível, à temperatura T, de n mols de um gás ideal desde um volume inicial de 10 L até um volume final de 20 L, se R representa a constante universal dos gases, então a variação de entropia (!$ \triangle !$S) do sistema pode ser corretamente calculada por meio da expressão
Provas
Caso se deseje aquecer uma amostra de gás natural,
Provas
Um tanque foi carregado com determinada quantidade de gás natural comprimido à temperatura ambiente e, ao se medir a pressão no tanque, verificou-se que ela era consideravelmente menor que a esperada de acordo com a lei dos gases ideais para a temperatura em questão.
Nessa situação, o comportamento descrito deve-se
Provas
A determinação do teor de umidade e do número de água de cristalização de um sal hidratado foi realizada pela secagem em estufa até obter massa constante. Esse procedimento corresponde ao método de
Provas
Dentre as seguintes soluções aquosas dos compostos a seguir, de mesma concentração molar, qual delas terá o ponto de congelamento mais baixo?
Provas
Uma solução aquosa de molalidade 1,35 mol/kg de um composto X tem a temperatura de ebulição de 101,4 °C, sob pressão de 1,0 atm. É correto afirmar que o composto X é (Dado: Constante de elevação do ponto de ebulição da água: 0,52 °C kg/mol)
Provas
Considere a titulação de uma solução de ácido acético com uma solução de hidróxido de sódio, a 25°C. Com respeito aos estágios dessa titulação, analise as assertivas e assinale a alternativa que aponta a(s) correta(s).
I. Na pré-equivalência, após a adição de um volume de titulante, tem-se uma solução tampão formada pela mistura acetato de sódio e ácido acético.
II. No ponto de meia-equivalência (metade do volume de titulante adicionado), a solução terá pH igual ao valor de Ka (ácido acético).
III. Na equivalência química, a solução resultante terá [OH−] > [H3O+].
Provas
Para a padronização da solução de permanganato de potássio, um analista usou 0,268g de Na2C2O4 e gastou 20,00mL da solução de KMnO4.
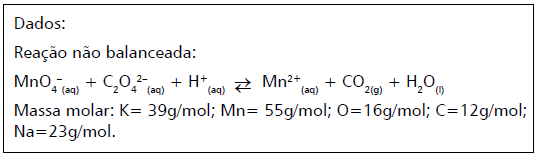
A molaridade dessa solução de KMnO4 é
Provas
Ponto de fulgor à pressão constante é a temperatura
Provas
Caderno Container