Foram encontradas 70 questões.
Considere as seguintes afirmações sobre equilíbrio de fases e propriedades coligativas.
I. A adição de um soluto não volátil a um solvente puro, em uma dada temperatura constante, sempre provoca uma diminuição na pressão de vapor.
II. A pressão de vapor de uma solução formada por dois líquidos voláteis é sempre menor que a pressão de vapor dos líquidos puros a uma mesma temperatura.
III. O valor absoluto do abaixamento no ponto de congelamento de uma solução é menor se o soluto dimeriza parcialmente no solvente, comparado ao sistema nas mesmas condições em que não há a dimerização do soluto.
IV. A pressão osmótica é a pressão exercida pelas moléculas de soluto numa membrana semipermeável.
V. Uma mistura formada por duas substâncias nunca solidifica inteiramente em uma única temperatura.
Assinale a opção que contém a(s) afirmação(ões) CORRETA(S):
Provas
Considere a estrutura de Lewis de um tricloreto.
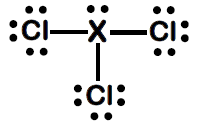
São feitas as seguintes afirmações a respeito da estrutura geométrica da molécula e a possível identidade do átomo X:
I. A molécula adota uma estrutura trigonal plana, com ângulo de ligação Cl-X-Cl maior ou igual a 120°.
II. A molécula adota uma estrutura tetraédrica, com ângulo de ligação Cl-X-Cl maior que 109,5°.
III. O átomo “X” pode ser o nitrogênio, preservando a geometria molecular.
IV. O átomo “X” pode ser o boro, preservando a geometria molecular.
Assinale a opção que contém a(s) afirmação(ões) CORRETA(S):
Provas
Em um reator mantido à temperatura constante, PCl5(g) encontra-se em equilíbrio com 1 atm de Cl2(g) e 2 atm de PCl3(g). Sabendo-se que a constante de equilíbrio da reação de dissociação do PCl5(g) nessa temperatura é kp = 4, assinale a alternativa que apresenta a nova pressão de equilíbrio do PCl5(g) (em atm) após adição de mais 2 atm desse gás ao reator.
Provas
Considere as seguintes afirmações sobre processos termodinâmicos, que podem ocorrer em uma ou mais etapas, em que ΔT se refere à variação de temperatura entre os estados inicial e final:
I. Um processo termodinâmico é definido pelo estado final e estado inicial do sistema.
II. ΔT é sempre nula em um processo isotérmico.
III. A troca de calor envolvida em um processo isotérmico deve ser nula (q = 0).
IV. Todo processo em que ΔT = 0 é um processo isotérmico.
V. ΔT = 0 para todo processo em sistema isolado.
Assinale a opção que contém as afirmações ERRADAS:
Provas
São feitas as afirmações a respeito de reações de substituição de compostos aromáticos.
I. A reação do metil benzeno com o ácido sulfúrico fumegante é mais rápida comparada à reação do benzeno nas mesmas condições experimentais.
II. A reação de nitração do metil benzeno produz preferencialmente compostos orto- e para-substituídos.
III. A nitração do benzeno é mais rápida do que a nitração do nitrobenzeno, a qual requer uma maior concentração de ácido nítrico e uma temperatura maior.
IV. O único produto resultante da reação de nitração do 1-hidroxi-4-metil-benzeno é o 1-hidroxi-2-nitro-4-metil-benzeno.
V. A reação de nitração do ácido benzoico produz preferencialmente o composto meta-substituído.
Assinale a opção que contém as afirmações CORRETAS:
Provas
Considere a seguinte reação em fase gasosa, inicialmente conduzida a uma pressão de 200 atm e a uma temperatura de 400°C. Considere que partindo de um sistema contendo apenas A e B, o equilíbrio é alcançado após 60 min de reação.
!$ 2A + B \rightleftarrows C + D + Q !$
em que A e B são reagentes, C e D os produtos e Q o calor liberado. Avalie as seguintes suposições sobre o efeito das modificações de um parâmetro da reação, mantendo os outros constantes.
I. Conduzir a reação a 600°C gera uma fração maior de C e D.
II. Conduzir a reação a 600°C faz com que o equilíbrio seja alcançado em menos de 60 min.
III. Conduzir a reação a uma pressão de 100 atm gera uma fração menor de C e D.
IV. Remover C e D do meio reacional após o equilíbrio e então retomar a reação permitem obter uma fração total maior de C e D.
Escolha a opção que lista a(s) afirmação(ões) CORRETA(S).
Provas
Assinale a opção que apresenta a sequência que melhor descreve o ciclo de ações envolvidas no método científico (hipotético - dedutivo):
Provas
Considere a seguinte configuração experimental, constituída de um canhão de partículas !$ \alpha !$, dois detectores de partículas !$ \alpha !$ posicionados ortogonalmente entre si e uma folha fina de um determinado material (W, X, Y, Z).

Experimentos foram realizados, bombardeando cada material com uma quantidade de partículas !$ \alpha !$ e registrando o número de partículas coletadas em cada detector, conforme a tabela abaixo.
| Experimento | Partículas lançadas | Material | Partículas Coletadas | |
| Detector 1 | Detector 2 | |||
| I | 8000 | W | 7903 | 1 |
| II | 10 | X | 10 | 0 |
| III | 10 | Y | 10 | 0 |
| IV | 10 | Z | 10 | 0 |
A partir dessas informações, assinale a alternativa que apresenta a conclusão CORRETA sobre as observações feitas nos experimentos.
Provas
Sistemas compostos por água e tensoativos em diferentes proporções, depois de homogeneizados, passam por um processo termodinâmico quando atingem temperaturas em torno de 0°C. A variação de entalpia (ΔH) desse processo foi determinada para cada mistura em função da composição do sistema, conforme apresentado no gráfico.
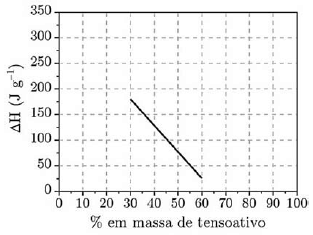
Considere que o ponto de fusão do tensoativo puro é menor que -20 °C e o calor latente de fusão da água pura é 334 J.g-1. Sobre esses sistemas são feitas as seguintes afirmações:
I. O ΔH refere-se à transição de fase do tensoativo.
II. O calor latente de fusão do tensoativo puro é -180 J.g-1.
III. Até 35% em massa de água pode se apresentar na forma associada à substância e não funde.
IV. O ΔH é proporcional à quantidade de água não associada ao tensoativo.
Com base no gráfico e nas informações do enunciado, assinale a opção que indica a(s) afirmação(ões) CORRETA(S).
Provas
São feitas as seguintes afirmações a respeito do ciclo do oxigênio no meio ambiente:
l. A concentração de oxigênio na atmosfera está diminuindo significativamente no último século, devido à queima de combustíveis fósseis e à redução da vegetação terrestre e marinha.
II. Os maiores contribuintes para a produção de oxigênio e sua liberação na atmosfera terrestre são florestas densas, pastagens, ervas e arbustos.
III. O oxigênio está envolvido, em algum grau, em todos os outros ciclos biogeoquímicos.
IV. Águas doces frias são as maiores fontes de oxigênio livre na Terra.
Assinale a alternativa que apresentam as afirmações ERRADAS.
Provas
Caderno Container