Foram encontradas 35.976 questões.
Algumas pilhas galvânicas comuns têm papel importante em nossas vidas, fornecendo-nos energia
elétrica, dentre elas têm a pilha seca de zinco-carbono. Este tipo de pilha é usado em lanternas, rádios
portáteis, brinquedos etc. Na figura 1, a seguir, mostra-se um diagrama em corte de uma pilha seca de
zinco-carbono típica.
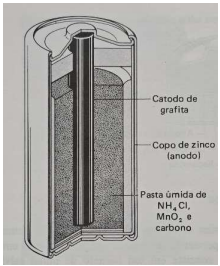
Figura 1. Pilha Galvânica, pilha seca de Zinco-Carbono. Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere as assertivas a seguir:
I. As pilhas secas têm uma camada externa de papelão ou metal, que serve apenas para isolá-la da atmosfera, e, interiormente a este revestimento, há um copo de zinco que serve como ânodo.
II. O copo de zinco é cheio de uma massa úmida, consistindo de cloreto de amônio, dióxido de manganês e carbono finamente dividido, e imerso nesta pasta há um bastão de grafita, que serve como cátodo.
III. A amônia produzida no cátodo reage com parte do Zn 2+, formado no ânodo, para dar o íon complexo Zn(NH3)4 2+ . Devido a natureza da pilha não se pode escrever uma única reação global.
IV. As pilhas secas não podem ser recarregadas e, portanto, têm um tempo de vida relativamente longo, como, por exemplo, quando comparadas com a bateria de chumbo e a pilha de níquel-cádmo que são recarregáveis.
V. No ânodo, o zinco é reduzido, enquanto que, no cátodo, a mistura de MnO2/NH4Cl sofre oxidação, para dar uma mistura complexa de produtos.
Assinale a alternativa que contenha APENAS as afirmações corretas.

Figura 1. Pilha Galvânica, pilha seca de Zinco-Carbono. Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere as assertivas a seguir:
I. As pilhas secas têm uma camada externa de papelão ou metal, que serve apenas para isolá-la da atmosfera, e, interiormente a este revestimento, há um copo de zinco que serve como ânodo.
II. O copo de zinco é cheio de uma massa úmida, consistindo de cloreto de amônio, dióxido de manganês e carbono finamente dividido, e imerso nesta pasta há um bastão de grafita, que serve como cátodo.
III. A amônia produzida no cátodo reage com parte do Zn 2+, formado no ânodo, para dar o íon complexo Zn(NH3)4 2+ . Devido a natureza da pilha não se pode escrever uma única reação global.
IV. As pilhas secas não podem ser recarregadas e, portanto, têm um tempo de vida relativamente longo, como, por exemplo, quando comparadas com a bateria de chumbo e a pilha de níquel-cádmo que são recarregáveis.
V. No ânodo, o zinco é reduzido, enquanto que, no cátodo, a mistura de MnO2/NH4Cl sofre oxidação, para dar uma mistura complexa de produtos.
Assinale a alternativa que contenha APENAS as afirmações corretas.
Provas
Questão presente nas seguintes provas
O cromo é um elemento químico com várias características importantes, dentre elas pode-se citar no
setor industrial, sendo amplamente utilizado na fabricação de ligas (como o aço inoxidável), na produção
de pigmentos (como o óxido de cromo) e em tratamentos de superfícies para proteção contra corrosão. É
um elemento relativamente resistente à corrosão e à oxidação, especialmente em sua forma metálica.
Contudo, sua toxicidade e impacto ambiental são preocupantes. Os compostos de cromo, especialmente
o cromo hexavalente, são tóxicos e carcinogênico, podendo causar sérios problemas de saúde e
ambientais.
Sobre o átomo de cromo sabemos que ele apresenta múltiplos estados de oxidação, sendo +3 e +6 os mais comuns, com base nesta informação em qual das espécies a seguir o átomo de cromo apresenta número de oxidação +3?
Sobre o átomo de cromo sabemos que ele apresenta múltiplos estados de oxidação, sendo +3 e +6 os mais comuns, com base nesta informação em qual das espécies a seguir o átomo de cromo apresenta número de oxidação +3?
Provas
Questão presente nas seguintes provas
“A amônia, apesar do seu tempo de vida relativamente curto, de aproximadamente 10 dias, é o terceiro
composto de nitrogênio mais abundante na atmosfera, ficando atrás apenas do N2e N2O. A sua
concentração é variável no espaço e no tempo, sendo os valores característicos na faixa de 0,1-10
mL/m3
. As principais fontes incluem a decomposição enzimática da ureia proveniente de urina e
excremento animais, emissão pelo solo, queima de biomassa e perdas durante a produção e aplicação
de fertilizantes, que representam a emissão global de cerca de 104,5 MtN (Megatonelada de Nitrogênio
106 ano como amônia”.
MARTINS, C. R. et al.; Ciclos Globais de Carbono, Nitrogênio e Enxofre: a importância na Química da Atmosfera. Cadernos Temáticos de Química Nova na Escola. Nº 5, Novembro, 2003, p.35.
Observando a fixação do Nitrogênio para a produção de amônia como indica a reação a seguir:
3H2(g) + N2 (g) ⇆ 2NH3(g)
Considere que na reação de fixação do nitrogênio para a produção de amônia, a uma temperatura de 500º C, a constante de equilíbrio (Kc) tem valor igual a 6,0 x10 -2 , imagine se, em um simulador de reator industrial a esta temperatura, há 0,250 mol dm-3 de H2 e 0,0500 mol dm-3 de NH3 presentes no equilíbrio, qual é a concentração de N2?
MARTINS, C. R. et al.; Ciclos Globais de Carbono, Nitrogênio e Enxofre: a importância na Química da Atmosfera. Cadernos Temáticos de Química Nova na Escola. Nº 5, Novembro, 2003, p.35.
Observando a fixação do Nitrogênio para a produção de amônia como indica a reação a seguir:
3H2(g) + N2 (g) ⇆ 2NH3(g)
Considere que na reação de fixação do nitrogênio para a produção de amônia, a uma temperatura de 500º C, a constante de equilíbrio (Kc) tem valor igual a 6,0 x10 -2 , imagine se, em um simulador de reator industrial a esta temperatura, há 0,250 mol dm-3 de H2 e 0,0500 mol dm-3 de NH3 presentes no equilíbrio, qual é a concentração de N2?
Provas
Questão presente nas seguintes provas
Muitos compostos contendo nitrogênio são encontrados na natureza, pois este elemento químico possui
grande capacidade de fazer ligações químicas, com números de oxidação variando de (–3) a (+5). É o
mais abundante elemento químico na atmosfera terrestre, contribuindo com aproximadamente 78% de
sua composição. A molécula de N2 é extremamente estável e quase não desempenha papel químico
importante, exceto na termosfera (altitude maior que 90 km) onde pode ser fotolizada ou ionizada. Os
constituintes minoritários, tais como óxido nitroso (N2O), óxido nítrico (NO), dióxido de nitrogênio (NO2),
ácido nítrico (HNO3) e amônia (NH3) são quimicamente reativos e têm importantes papéis nos problemas
ambientais contemporâneos, incluindo a formação e precipitação ácida (chuva ácida), poluição
atmosférica (smog fotoquímico), aerossóis atmosféricos e a depleção da camada de ozônio. Os óxidos de
nitrogênio, NO e NO2, são rapidamente interconversíveis e existem em equilíbrio dinâmico.
Assim, em experimento no laboratório, observando a reação do gás castanho NO2, um poluente do ar, e o gás incolor N2O4 que se encontram em equilíbrio, como indica a equação a seguir, foram adicionados em um reator de 5dm³, 0,625 mol de N2O4 e deixou-se decompor até atingir o equilibro com o NO2.
A concentração de equilíbrio do N2O4 obtida foi de 0,0750 M. Qual a constante de equilíbrio, kc, para esta reação?
2NO2 ⇄ N2O4
Assim, em experimento no laboratório, observando a reação do gás castanho NO2, um poluente do ar, e o gás incolor N2O4 que se encontram em equilíbrio, como indica a equação a seguir, foram adicionados em um reator de 5dm³, 0,625 mol de N2O4 e deixou-se decompor até atingir o equilibro com o NO2.
A concentração de equilíbrio do N2O4 obtida foi de 0,0750 M. Qual a constante de equilíbrio, kc, para esta reação?
2NO2 ⇄ N2O4
Provas
Questão presente nas seguintes provas
O amoníaco e seus sais são fertilizantes valiosos, a fabricação do amoníaco pela combinação direta do
N2 com o H2 constitui um dos principais equilíbrios químicos mais importantes para a civilização. E
através do estudo de equilíbrio químico podemos observar os fatores que afetam um equilíbrio químico e
como lidar com um equilíbrio quantitativamente. Assim, segundo o princípio de Le Chatelier: Quando uma
perturbação é aplicada em um sistema em equilíbrio dinâmico, ele tende a se ajustar para reduzir ao
mínimo o efeito da perturbação.
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
Considerando a equação abaixo:
CO(g) + H₂O(g) ⇌ CO₂(g) + H₂(g) ΔH < 0
Qual das seguintes alternativas representa uma ação que levará ao aumento da produção de CO₂?
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018.
Considerando a equação abaixo:
CO(g) + H₂O(g) ⇌ CO₂(g) + H₂(g) ΔH < 0
Qual das seguintes alternativas representa uma ação que levará ao aumento da produção de CO₂?
Provas
Questão presente nas seguintes provas
“Um equilíbrio em fase de gás responde à compressão - a redução de volume - do recipiente da reação.
De acordo com o princípio de Le Chatelier, a composição tende a mudar para reduzir ao mínimo o efeito
do aumento da pressão.”
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018, p. 429.
Como responderá o equilíbrio da seguinte equação se o volume do recipiente que a contém for reduzido?
N₂(g) + 3H₂(g) ⇌ 2NH₃(g) ΔH < 0
ATKINS, P.; JONES, L.; LAVERMAN, L. Princípios de química: questionando a vida moderna e o meio ambiente. 7. ed. Porto Alegre: Bookman, 2018, p. 429.
Como responderá o equilíbrio da seguinte equação se o volume do recipiente que a contém for reduzido?
N₂(g) + 3H₂(g) ⇌ 2NH₃(g) ΔH < 0
Provas
Questão presente nas seguintes provas
A joia de prata escurece devido a um processo chamado oxidação. Quando a prata é exposta ao ar e à
umidade, ela pode reagir com o enxofre presente no ambiente, formando sulfeto de prata, (Ag₂S), que é
um composto escuro e fica na superfície da prata, esse é o principal agente responsável pelo
escurecimento da Ag. Além disso, fatores como o suor, produtos químicos e poluição também podem
acelerar esse processo. Para remover este escurecimento, manchas, em vez de usar líquidos e panos
de limpeza, que podem retirar apenas uma parte deste escurecimento, é possível limpar colocando as
peças de prata em um recipiente de alumínio com uma solução diluída de soda cáustica, de modo que o
objeto fique totalmente imerso. Forma-se uma célula eletrolítica, em que o íon prata passa a prata
metálica. Desse modo, a superfície da peça de prata tornar-se-á limpa.
Este processo de limpeza do objeto de prata é representado pela reação:
3 Ag2S(s) + 2 Al(s) +2 NaOH(aq) + 2 H2O (l) ⟶ 6 Ag(s) + 3 H2S(aq) + 2 NaAlO2(aq)
A partir da equação, indique qual o elemento oxidado e o elemento reduzido?
Este processo de limpeza do objeto de prata é representado pela reação:
3 Ag2S(s) + 2 Al(s) +2 NaOH(aq) + 2 H2O (l) ⟶ 6 Ag(s) + 3 H2S(aq) + 2 NaAlO2(aq)
A partir da equação, indique qual o elemento oxidado e o elemento reduzido?
Provas
Questão presente nas seguintes provas
Uma ligação predominantemente iônica ocorre com o ganho e perda de elétrons, por isso dizemos que os
átomos que estabelecem esse tipo de ligação adquirem uma carga real. Já uma ligação
predominantemente covalente ocorre por compartilhamento de elétrons, desde que essa ligação não seja
100% covalente (isto é, desde que exista diferença de eletronegatividade entre átomos ligados), dizemos
que cada átomo adquire uma carga elétrica aparente. E denomina-se NOX a carga elétrica real ou
aparente que um átomo adquire quando estabelece ligações com outros átomos, podendo ocorrer
reações de óxido-redução.
Na equação não balanceada a seguir, os agentes redutor e oxidantes são, respectivamente:
Kbr + K2Cr2SO4 + H2SO4 ⟶ Br2 + K2SO4 + Cr2(SO4)3 + H2O
Na equação não balanceada a seguir, os agentes redutor e oxidantes são, respectivamente:
Kbr + K2Cr2SO4 + H2SO4 ⟶ Br2 + K2SO4 + Cr2(SO4)3 + H2O
Provas
Questão presente nas seguintes provas
O ar atmosférico não poluído, de locais de mangues, pântanos e erupções vulcânicas contêm, além de
nitrogênio, oxigênio e argônio, uma série de outros gases em pequenas quantidades, entre eles o gás
carbônico, CO2 (g) (± 0,03%).
De posse destas informações analise as seguintes afirmativas.
I. A medida do grau de acidez de uma solução (como a chuva ácida) é definida pelo teor de íons hidrônio, H+3O, livres por unidade de volume que ela apresenta, o que é denominado potencial hidrogeniônico e simbolizado por pH. Neste caso, quando o pH é maior que 7, a chuva é classificada como ácida.
II. O gás carbônico CO2 (g) é um óxido ácido e, portanto, reage com a água da chuva produzindo o ácido carbônico que reage, em parte e ioniza-se formando íon hidrônio, H+ 3O, e íon de hidrogenocarbonato, HCO3 1- , e em parte volta a formar água e gás carbônico, assim a chuva é naturalmente ácida em menor ou maior intensidade, como exemplifica a reação a seguir.
CO2 (g) + H2O(l) ⟶ H2CO3(aq) + H3O 1+ (aq) + HCO1- 3(aq)
III. As chuvas em regiões onde o ar é considerado não poluído costuma ter pH em torno de 5,6. Convencionou-se, então, chamar chuva ácida aquela cujo pH é menor do que 5,6. A chuva ácida, definida dessa maneira, pode ocorrer tanto devido a processos naturais como devido a atividades humanas.
IV. O monóxido de nitrogênio, NO, reage rapidamente com o ozônio, O3(g) da estratosfera, formando o dióxido de nitrogênio, NO2(g), este por sua vez reage com a água da chuva formando os ácidos nítrico e nitroso, mas não reagem formando a chuva ácida.
Assinale a alternativa que contenha APENAS as afirmações corretas.
De posse destas informações analise as seguintes afirmativas.
I. A medida do grau de acidez de uma solução (como a chuva ácida) é definida pelo teor de íons hidrônio, H+3O, livres por unidade de volume que ela apresenta, o que é denominado potencial hidrogeniônico e simbolizado por pH. Neste caso, quando o pH é maior que 7, a chuva é classificada como ácida.
II. O gás carbônico CO2 (g) é um óxido ácido e, portanto, reage com a água da chuva produzindo o ácido carbônico que reage, em parte e ioniza-se formando íon hidrônio, H+ 3O, e íon de hidrogenocarbonato, HCO3 1- , e em parte volta a formar água e gás carbônico, assim a chuva é naturalmente ácida em menor ou maior intensidade, como exemplifica a reação a seguir.
CO2 (g) + H2O(l) ⟶ H2CO3(aq) + H3O 1+ (aq) + HCO1- 3(aq)
III. As chuvas em regiões onde o ar é considerado não poluído costuma ter pH em torno de 5,6. Convencionou-se, então, chamar chuva ácida aquela cujo pH é menor do que 5,6. A chuva ácida, definida dessa maneira, pode ocorrer tanto devido a processos naturais como devido a atividades humanas.
IV. O monóxido de nitrogênio, NO, reage rapidamente com o ozônio, O3(g) da estratosfera, formando o dióxido de nitrogênio, NO2(g), este por sua vez reage com a água da chuva formando os ácidos nítrico e nitroso, mas não reagem formando a chuva ácida.
Assinale a alternativa que contenha APENAS as afirmações corretas.
Provas
Questão presente nas seguintes provas
As emissões de SO₂ são reguladas em muitos países devido aos seus efeitos prejudiciais à saúde e ao
meio ambiente e, por ser uma das substâncias poluentes do ar, possui um odor forte, semelhante ao de
fósforos queimados; é tóxico e pode causar irritação nos olhos, pele e trato respiratório, sendo um agente
redutor pode reagir com oxigênio, formando trióxido de enxofre (SO₃), além de gerar problemas ambientais devido à chuva ácida.
Considerando as informações descritas acima, a alternativa CORRETA é:
Considerando as informações descritas acima, a alternativa CORRETA é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container