Foram encontradas 35.976 questões.
Uma amostra de 25,0 ml de solução de ácido sulfúrico,
H2SO4, de concentração desconhecida é titulada com uma
solução padronizada de hidróxido de sódio, NaOH, 0,100
mol L-1. Se o ponto de equivalência é atingido após a adição
de 30,0 ml da solução básica, qual é a concentração da
solução ácida, em mol L-1?
Provas
Questão presente nas seguintes provas
Dentre os vários instrumentos presentes em um laboratório
biológico, uma solução tampão deve ter seu pH aferido por
Provas
Questão presente nas seguintes provas
Sabendo que a massa molar do NaCl é 58,44 g/mol, para se
preparar 10 ml de solução aquosa de NaCl a 1 M, qual massa
de soluto deve-se utilizar, considerando um arredondamento
de 3 casas decimais após a vírgula?
Provas
Questão presente nas seguintes provas
EXPERIMENTO DAS VELAS
Materiais:
• duas velas;
• dois pratos de sobremesa;
• dois vidros altos e largos;
• uma pequena muda de planta.
Instruções:
1. Fixe cada uma das velas em um prato etiquetando-os com as letras A e B.
2. Junto da vela do prato B coloque a muda de planta.
3. Acenda ambas as velas.
4. Coloque os vidros sobre as velas e as observe.
A partir deste contexto, analise as afirmações a seguir.
A partir deste contexto, analise as afirmações a seguir.
I- As observações das chamas das velas acesas são resultantes de uma reação química.
II- A chama da vela no prato B irá durar por mais tempo.
III- Imediatamente quando o vidro for colocado sobre a vela A, ela irá apagar.
É CORRETO o que se afirma em:
Materiais:
• duas velas;
• dois pratos de sobremesa;
• dois vidros altos e largos;
• uma pequena muda de planta.
Instruções:
1. Fixe cada uma das velas em um prato etiquetando-os com as letras A e B.
2. Junto da vela do prato B coloque a muda de planta.
3. Acenda ambas as velas.
4. Coloque os vidros sobre as velas e as observe.
A partir deste contexto, analise as afirmações a seguir.
A partir deste contexto, analise as afirmações a seguir.
I- As observações das chamas das velas acesas são resultantes de uma reação química.
II- A chama da vela no prato B irá durar por mais tempo.
III- Imediatamente quando o vidro for colocado sobre a vela A, ela irá apagar.
É CORRETO o que se afirma em:
Provas
Questão presente nas seguintes provas
O processo de fabricação da cerveja começa com a germinação da cevada para torná-la malte, um processo que garante a presença de
açúcares e amido além das enzimas amilase e protease. Seguem-se então as seguintes etapas: 1) o malte da cevada é misturado à água
quente; 2) a massa resultante é filtrada, obtendo-se uma solução açucarada chamada de mosto; 3) adiciona-se lúpulo ao mosto que é
fervido em uma caldeira de fermentação; 4) em seguida o mosto é resfriado e o lúpulo é filtrado; 5) a solução é levada para um
recipiente de fermentação adicionando-se levedura; 6) a cerveja só é bebível depois de condicionada, processo no qual a levedura
quebra compostos de sabor ruim.
A partir deste contexto, analise as afirmações a seguir.
I- É a partir do processo da etapa 5 que se formam o etanol e o CO2, a partir da conversão do mosto.
II- O resultado da etapa 1 é uma mistura homogênea.
III- Nas etapas 2, 3 e 4 ocorrem processos físicos de separação de misturas.
É CORRETO o que se afirma em:
A partir deste contexto, analise as afirmações a seguir.
I- É a partir do processo da etapa 5 que se formam o etanol e o CO2, a partir da conversão do mosto.
II- O resultado da etapa 1 é uma mistura homogênea.
III- Nas etapas 2, 3 e 4 ocorrem processos físicos de separação de misturas.
É CORRETO o que se afirma em:
Provas
Questão presente nas seguintes provas
A testosterona é um hormônio esteroide fundamental, principalmente conhecido como o principal
hormônio masculino, embora também esteja presente em mulheres em níveis mais baixos. É crucial para
o desenvolvimento das características sexuais secundárias masculinas, como aumento da massa
muscular, pelos faciais e corporais e profundidade da voz. Contribui para a densidade óssea, distribuição
de gordura, produção de glóbulos vermelhos e libido. A progesterona é um hormônio esteroide
importante, especialmente relacionado à reprodução e à saúde feminina. Em mulheres é produzida
principalmente pelos ovários, especialmente após a ovulação, e pela placenta durante a gravidez. Abaixo
são representadas as respectivas estruturas, figura 4.
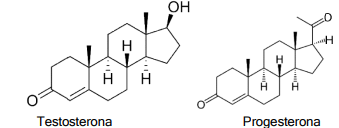
Figura 4. Hormônios esteroides masculino e feminino. Disponível em: https://pt.wikipedia.org/wiki/Testosterona/Progesterona. Acessado em: setembro.2024
Nas alternativas descritas, assinale corretamente qual delas indica as funções orgânicas presentes nas duas substâncias.

Figura 4. Hormônios esteroides masculino e feminino. Disponível em: https://pt.wikipedia.org/wiki/Testosterona/Progesterona. Acessado em: setembro.2024
Nas alternativas descritas, assinale corretamente qual delas indica as funções orgânicas presentes nas duas substâncias.
Provas
Questão presente nas seguintes provas
No grupo de funções orgânicas oxigenadas, o manitol é um tipo de açúcar que é utilizado em várias
aplicações na indústria alimentícia, farmacêutica e médica. Dente elas, o manitol é frequentemente
utilizado como um adoçante em produtos dietéticos e sem açúcar, devido ao seu baixo índice glicêmico,
também atua como um agente de textura e conservante. Na medicina, o manitol é utilizado como um
diurético osmótico, ajudando a reduzir a pressão intracraniana e a pressão ocular. É frequentemente
utilizado em emergências, como em pacientes com edema cerebral ou glaucoma. Pode ser encontrado
naturalmente em algumas plantas, como em frutas (por exemplo, maçãs e peras) e em algas. Sua
fórmula estrutura é apresentada na figura 3 a seguir.
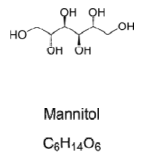
Figura 3. Fórmula estrutural do manitol. Disponível em https://pt.dreamstime.com/manitol-mannite-ou-f%C3%B3rmula-qu%C3%ADmica-do-a%C3%A7%C3%BAcar-manna-e-estruturaesquel%C3%A9tica-de-manga-is%C3%B4mero-sorbitol-utilizado-como-image209330436. Acesso em: setembro.2024.
Qual o nome oficial segundo o International Union of Pure and Applied Chemistry (IUPAC) desse açúcar?

Figura 3. Fórmula estrutural do manitol. Disponível em https://pt.dreamstime.com/manitol-mannite-ou-f%C3%B3rmula-qu%C3%ADmica-do-a%C3%A7%C3%BAcar-manna-e-estruturaesquel%C3%A9tica-de-manga-is%C3%B4mero-sorbitol-utilizado-como-image209330436. Acesso em: setembro.2024.
Qual o nome oficial segundo o International Union of Pure and Applied Chemistry (IUPAC) desse açúcar?
Provas
Questão presente nas seguintes provas
O elemento Tório (Th) é um metal prateado e macio, que se torna mais duro e quebradiço quando
oxidado. Seu isótopo mais abundante é o tório-232 (²³²Th), que é radioativo e possui uma meia-vida de
aproximadamente 14 bilhões de anos. Mas sua radioatividade é relativamente baixa em comparação com
outros elementos como o urânio ou o plutônio. Dentre seus usos cita-se: como combustível em reatores
nucleares, e produzem menos resíduos que reatores de urânio, em lâmpadas de gás de alta intensidade,
é usado também na produção de cerâmicas especiais, devido à sua alta resistência ao calor.
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Suponha que este elemento, 90Th232 , de número atômico 90 e número de massa igual a 232, emita sucessivamente uma partícula α seguida de duas emissões β e novamente uma emissão α. Ao final, o átomo que encerra essa série de emissões terá em seu núcleo:
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Suponha que este elemento, 90Th232 , de número atômico 90 e número de massa igual a 232, emita sucessivamente uma partícula α seguida de duas emissões β e novamente uma emissão α. Ao final, o átomo que encerra essa série de emissões terá em seu núcleo:
Provas
Questão presente nas seguintes provas
No estudo da interação de radiação com a matéria, as partículas alfa (α), beta (β) e gama (ϒ) emitidas
em processos de decaimento nuclear são altamente energéticas e provocam alterações químicas
substanciais, à medida que interagem com a matéria. A excitação eletrônica de uma molécula pode levar
a sua dissociação em átomos ou outras moléculas. Os íons atômicos e moleculares produzidos pela
radiação são também muito reativos, e isso pode ter importantes consequências químicas.
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Neste contexto, o Ferro (Ferro – 59, 26Fe59) é um isótopo radioativo, bastante usado em análises clínicas no diagnóstico de anemia.
A equação nuclear para o decaimento do 26Fe59 , como um emissor beta é:
MAHAN, Bruce M. Química: um curso universitário. 4ª ed. Editora Blücher, São Paulo: 1995. p. 582.
Neste contexto, o Ferro (Ferro – 59, 26Fe59) é um isótopo radioativo, bastante usado em análises clínicas no diagnóstico de anemia.
A equação nuclear para o decaimento do 26Fe59 , como um emissor beta é:
Provas
Questão presente nas seguintes provas
Quando a água cai espontaneamente, em uma cachoeira, a Física explica o fato afirmando que a água
caiu de um nível de maior energia para outro, de menor energia (no caso, energia potencial). Quanto
maior for a quantidade de água e maior a altura da queda, maior será a energia liberada pela água (que
pode ser transformada, por exemplo, em energia elétrica, em uma usina hidroelétrica). Fato idêntico
ocorre com as pilhas, dependendo dos materiais (metais e eletrólitos) que formam a pilha, ela irá
“despejar” uma quantidade maior ou menor de elétrons, com mais ou menos energia, através do circuito
externo. A altura da queda de água corresponde, na eletricidade, ao que se chama de diferença de
potencial (ddp) ou, mais especificamente, de força eletromotriz (fem) da pilha, representa a “pressão” que
move os elétrons através do condutor externo, ela é medida em Volts (V), com o uso de voltímetros.
Com base nas explicações presentes no texto, observe a célula eletroquímica representada na figura 2 a seguir:
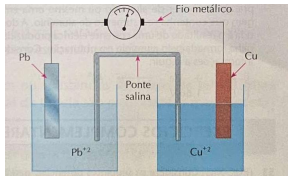
Figura 2. Célula Eletroquímica Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere os Potenciais:
Pb+2 + 2e ⟶ Pb (Eº = - 0,13 V) Cu+2 + 2e ⟶ Pb (Eº = + 0,34 V)
Pode-se afirmar corretamente sobre a célula que:
Com base nas explicações presentes no texto, observe a célula eletroquímica representada na figura 2 a seguir:

Figura 2. Célula Eletroquímica Fonte: Brady. J.E; Humiston, G. E. Química Geral. Vol. 2. 2ª ed. Livros Técnicos e Científicos Editora. 1996.
Considere os Potenciais:
Pb+2 + 2e ⟶ Pb (Eº = - 0,13 V) Cu+2 + 2e ⟶ Pb (Eº = + 0,34 V)
Pode-se afirmar corretamente sobre a célula que:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container