Foram encontradas 35.936 questões.
Ligações iônicas e covalentes são dois tipos extremos
de ligação. Porém, quase sempre as ligações formadas são de caráter intermediário, que podem ser explicadas em termos de poder polarizante e polarizabilidade.
Nesse sentido, é correto afirmar que uma combinação de fatores que favorece a covalência é
Nesse sentido, é correto afirmar que uma combinação de fatores que favorece a covalência é
Provas
Questão presente nas seguintes provas
Em 1923, Johannes Bronsted e Thomas Lowry propuseram a definição de que uma reação ácido-base ocorre quando há transferência de um íon hidrogênio, H+
,
de uma espécie para outra.
A partir desta informação, é INCORRETO afirmar que, na reação entre
A partir desta informação, é INCORRETO afirmar que, na reação entre
Provas
Questão presente nas seguintes provas
Na teoria dos orbitais moleculares (TOM), os elétrons
de valência são associados a todos os núcleos da molécula.
Associe corretamente a distribuição eletrônica pelos
orbitais moleculares (cujos orbitais moleculares degenerados não estão separados por vírgula) à molécula
correspondente.
DISTRIBUIÇÕES ELETRÔNICAS
1. σ1s2, σ*1s2, σ2s2, σ*2s2, π2py2 π2pz2, σ2px2
2. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py2 π2pz2, π*2py1 π*2pz1
3. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py 2 π2pz2, π*2py2 π*2pz2
4. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py2 π2pz2, π*2py2 π*2pz1
5. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py2 π2pz2, π*2py1 π*2pz0
MOLÉCULAS
( ) O2
( ) NO
( ) O2 2-
( ) CO
( ) O2 -
A sequência correta dessa associação é:
DISTRIBUIÇÕES ELETRÔNICAS
1. σ1s2, σ*1s2, σ2s2, σ*2s2, π2py2 π2pz2, σ2px2
2. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py2 π2pz2, π*2py1 π*2pz1
3. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py 2 π2pz2, π*2py2 π*2pz2
4. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py2 π2pz2, π*2py2 π*2pz1
5. σ1s2, σ*1s2, σ2s2, σ*2s2, σ2px2, π2py2 π2pz2, π*2py1 π*2pz0
MOLÉCULAS
( ) O2
( ) NO
( ) O2 2-
( ) CO
( ) O2 -
A sequência correta dessa associação é:
Provas
Questão presente nas seguintes provas
“O cobre representa 7,9% da produção mineral comercializada no Brasil, de acordo com a Agência Nacional
de Mineração (ANM), mas o País detém apenas 1,8%
dos recursos conhecidos globalmente. O modelamento de potencial mineral para o sul do cráton amazônico executado pelo SGB-CPRM mostrou que, além das
áreas conhecidas no Tapajós e Alta Floresta, ainda há
grande potencial para novas descobertas de cobre e
ouro em outras regiões.”
Disponível em https://www.brasilmineral.com.br/noticias/novo-mapa-sobre-ouro-e-cobre-na-amazonia. Acesso em 01 dez. 2025.
Considerando que o elemento químico “cobre” possui uma mistura isotópica de 69,09% de 63Cu (massa = 62,93 u) e 30,91% de 65Cu (massa = 64,95 u), informe se é verdadeiro (V) ou falso (F) o que se afirma com relação à determinação de massas atômicas.
( ) A massa atômica calculada do átomo de cobre é 63,55 u.
( ) A abundância isotópica é utilizada no cálculo da massa atômica.
( ) O número de massa não é utilizado no cálculo da massa atômica.
( ) O cálculo da massa atômica é feito com a média aritmética simples das massas dos isótopos.
De acordo com as afirmações, a sequência correta é:
Disponível em https://www.brasilmineral.com.br/noticias/novo-mapa-sobre-ouro-e-cobre-na-amazonia. Acesso em 01 dez. 2025.
Considerando que o elemento químico “cobre” possui uma mistura isotópica de 69,09% de 63Cu (massa = 62,93 u) e 30,91% de 65Cu (massa = 64,95 u), informe se é verdadeiro (V) ou falso (F) o que se afirma com relação à determinação de massas atômicas.
( ) A massa atômica calculada do átomo de cobre é 63,55 u.
( ) A abundância isotópica é utilizada no cálculo da massa atômica.
( ) O número de massa não é utilizado no cálculo da massa atômica.
( ) O cálculo da massa atômica é feito com a média aritmética simples das massas dos isótopos.
De acordo com as afirmações, a sequência correta é:
Provas
Questão presente nas seguintes provas
A Lei de Boyle surgiu do estudo independente de Robert Boyle e Edme Mariotte ao analisarem como o
volume ocupado por um gás varia quando a pressão
é alterada a uma determinada temperatura.
Observe os dados da compressão de uma certa quantidade fixa do gás hidrogênio à temperatura de 25 o C.

Avalie o que se afirma sobre a análise desses dados.
I- Quando a pressão do gás é aumentada, o volume diminui linearmente.
II- O gás hidrogênio se comporta como um gás não ideal em todos os experimentos. III- Um gás ideal é aquele que obedece à lei de Boyle.
IV- O volume do gás hidrogênio é de aproximadamente 23,0 mL quando a pressão é 760 mmHg.
Está correto apenas o que se afirma em
Observe os dados da compressão de uma certa quantidade fixa do gás hidrogênio à temperatura de 25 o C.

Avalie o que se afirma sobre a análise desses dados.
I- Quando a pressão do gás é aumentada, o volume diminui linearmente.
II- O gás hidrogênio se comporta como um gás não ideal em todos os experimentos. III- Um gás ideal é aquele que obedece à lei de Boyle.
IV- O volume do gás hidrogênio é de aproximadamente 23,0 mL quando a pressão é 760 mmHg.
Está correto apenas o que se afirma em
Provas
Questão presente nas seguintes provas
A distinção entre água pura e uma solução de água
com sal de cozinha pode ser realizada pela medida
das temperaturas de fusão e de ebulição em laboratório. Observa-se que a água pura ferve à temperatura constante, já para a água salgada o ponto de
ebulição aumenta gradualmente.
Nesse sentido, é correto afirmar que a razão para o aumento gradual é explicada pela
Nesse sentido, é correto afirmar que a razão para o aumento gradual é explicada pela
Provas
Questão presente nas seguintes provas
A nitração de anéis aromáticos é uma reação
fundamental na Química Orgânica, pois permite
introduzir o grupo nitro, um substituinte versátil que
pode ser convertido em diversas outras funções.
Esse processo é essencial na síntese de fármacos,
corantes e intermediários industriais, ampliando
significativamente a utilidade dos compostos
aromáticos.
Considere a reação de nitração a seguir.
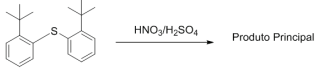
Qual é o produto principal obtido nesse processo?
Considere a reação de nitração a seguir.

Qual é o produto principal obtido nesse processo?
Provas
Questão presente nas seguintes provas
Preencha corretamente as lacunas do texto.
O ciclopentadieno apresenta um pKa anormalmente baixo para um hidrocarboneto, o que é explicado pela grande estabilidade da sua base conjugada, o ânion ciclopentadienila. Essa estabilidade se deve principalmente ao fato de que esse ânion é ______, pois possui ______ elétrons π distribuídos em um sistema contínuo de orbitais______ que se sobrepõem. Além disso, o ânion é estabilizado por ______, o que contribui ainda mais para a facilidade de perda do próton.
A sequência que preenche corretamente as lacunas do texto é:
O ciclopentadieno apresenta um pKa anormalmente baixo para um hidrocarboneto, o que é explicado pela grande estabilidade da sua base conjugada, o ânion ciclopentadienila. Essa estabilidade se deve principalmente ao fato de que esse ânion é ______, pois possui ______ elétrons π distribuídos em um sistema contínuo de orbitais______ que se sobrepõem. Além disso, o ânion é estabilizado por ______, o que contribui ainda mais para a facilidade de perda do próton.
A sequência que preenche corretamente as lacunas do texto é:
Provas
Questão presente nas seguintes provas
As reações orgânicas são processos químicos que
modificam moléculas baseadas em carbono, gerando novos produtos. Esses mecanismos sustentam a
química da vida e têm ampla aplicação na indústria
química e farmacêutica.
Observe cada reação a seguir.
(I)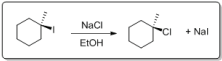
(II)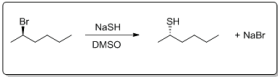
(III)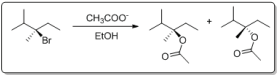
(IV)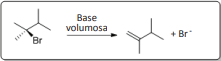
Informe se é verdadeiro (V) ou falso (F) o que se afirma com relação aos processos representados.
( ) A transformação I ocorre via SN1, pois o substrato é terciário; além disso, o solvente empregado favorece esse mecanismo de reação.
( ) A transformação II ocorre via SN2, pois o núcleófilo H2 S é forte; além disso, o solvente é polar aprótico, favorecendo esse mecanismo de reação.
( ) A transformação III ocorre via SN1, pois o nucleófilo fraco e o substrato terciário favorece esse mecanismo que leva a formação de dois diastereoisômeros.
( ) A transformação IV ocorre via reação de eliminação, pois o uso de uma base volumosa favorece a formação do produto de Hofmann.
De acordo com as afirmações, a sequência correta é:
Observe cada reação a seguir.
(I)

(II)

(III)

(IV)

Informe se é verdadeiro (V) ou falso (F) o que se afirma com relação aos processos representados.
( ) A transformação I ocorre via SN1, pois o substrato é terciário; além disso, o solvente empregado favorece esse mecanismo de reação.
( ) A transformação II ocorre via SN2, pois o núcleófilo H2 S é forte; além disso, o solvente é polar aprótico, favorecendo esse mecanismo de reação.
( ) A transformação III ocorre via SN1, pois o nucleófilo fraco e o substrato terciário favorece esse mecanismo que leva a formação de dois diastereoisômeros.
( ) A transformação IV ocorre via reação de eliminação, pois o uso de uma base volumosa favorece a formação do produto de Hofmann.
De acordo com as afirmações, a sequência correta é:
Provas
Questão presente nas seguintes provas
A medição do potencial do eletrodo AgCl/Ag em soluções contendo cloreto permite avaliar alterações químicas na água. Em regiões impactadas pelo garimpo
ilegal, a concentração de íons Cl⁻ pode variar devido
à mobilização de sedimentos e compostos metálicos.
Assim, essa ferramenta auxilia na identificação de
mudanças anômalas na qualidade da água. Considere
que um eletrodo de prata foi imerso em uma amostra
de água e o potencial medido foi igual a 340 mV.
Dado: E0 AgCl/Ag= 0,222 V
Nesse sentido, qual a concentração aproximada, em mol L-1, de íon cloreto nessa amostra?
Dado: E0 AgCl/Ag= 0,222 V
Nesse sentido, qual a concentração aproximada, em mol L-1, de íon cloreto nessa amostra?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container