Foram encontradas 47.681 questões.
Um inibidor altamente específico de CDK4 e CDK6, biodisponível por via oral, demonstrou uma tolerabilidade controlável e potencial terapêutico para uma variedade de tipos de câncer. Dados pré-clínicos sugerem que esse inibidor
pode atravessar a barreira hematoencefálica, apoiando o desenvolvimento clínico adicional do tratamento de tumores
do sistema nervoso central. A análise de amostras de plasma, tumor e líquido cefalorraquidiano (LCR) foi realizada para
avaliar a farmacocinética e a penetração do composto no sistema nervoso central e no tumor.
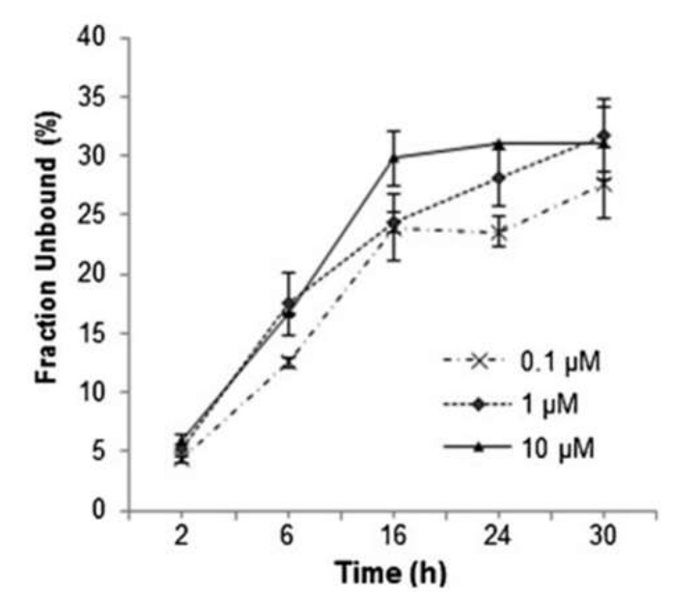
Observe as afirmativas abaixo sobre o gráfico acima: fração não ligada do inibidor (0,1, 1 e 10 μM) no plasma no tempo de equilíbrio de 2, 4, 6, 16 e 24 h.
I. A fração não ligada do inibidor no plasma pode ser determinada por diálise de equilíbrio.
II. O tempo de equilíbrio otimizado da fração não ligada do inibidor no plasma é de 6 h.
III. O inibidor ligou pouco às proteínas plasmáticas.
Das afirmativas acima:

Observe as afirmativas abaixo sobre o gráfico acima: fração não ligada do inibidor (0,1, 1 e 10 μM) no plasma no tempo de equilíbrio de 2, 4, 6, 16 e 24 h.
I. A fração não ligada do inibidor no plasma pode ser determinada por diálise de equilíbrio.
II. O tempo de equilíbrio otimizado da fração não ligada do inibidor no plasma é de 6 h.
III. O inibidor ligou pouco às proteínas plasmáticas.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Sobre os estudos de farmacocinética para otimizar a dose e o regime de dosagem de um composto, é INCORRETO
afirmar que:
Provas
Questão presente nas seguintes provas
C118P, um pró-fármaco com o grupo éster fosfato de C118, que é um novo inibidor de proteína de microtúbulos, está
atualmente em desenvolvimento clínico de Fase I na China para o tratamento de câncer de ovário e câncer de pulmão.
Os gráficos mostram os perfis de concentração plasmática versus tempo de C118P em ratos (A), C118 em ratos (B),
após a administração intravenosa de doses 5, 10, 20 e 50 mg/kg de C118P.
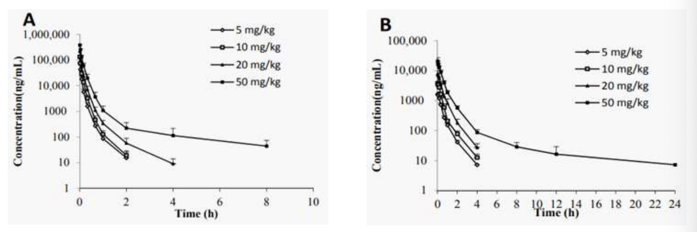
Observe as afirmativas a seguir:
I. Tanto C118P quanto C118 foram detectáveis no plasma de ratos após administração por via intravenosa de C118P.
II. Após a administração intravenosa, C118P pode ser hidrolisado em C118 rapidamente, com C118P e C118 detectáveis no sangue simultaneamente.
III. A área sob a curva de C118 reduziu proporcionalmente a dose no intervalo de 5–50 mg/kg.
Das afirmativas acima:

Observe as afirmativas a seguir:
I. Tanto C118P quanto C118 foram detectáveis no plasma de ratos após administração por via intravenosa de C118P.
II. Após a administração intravenosa, C118P pode ser hidrolisado em C118 rapidamente, com C118P e C118 detectáveis no sangue simultaneamente.
III. A área sob a curva de C118 reduziu proporcionalmente a dose no intervalo de 5–50 mg/kg.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Um novo protótipo antineoplásico foi desenvolvido com mecanismo de morte de células leucêmicas K562, através
de sinalização necroptótica. Devido ao seu efeito promissor, estudos sobre a sua farmacocinética foram realizados utilizando um novo método bioanalítico validado, baseado em cromatografia líquida acoplada à espectrometria de massas
sequencial. A tabela abaixo apresenta a média dos parâmetros farmacocinéticos desse novo protótipo em ratos (n = 3)
após administração intraperitoneal na dose de 100 mg/kg.
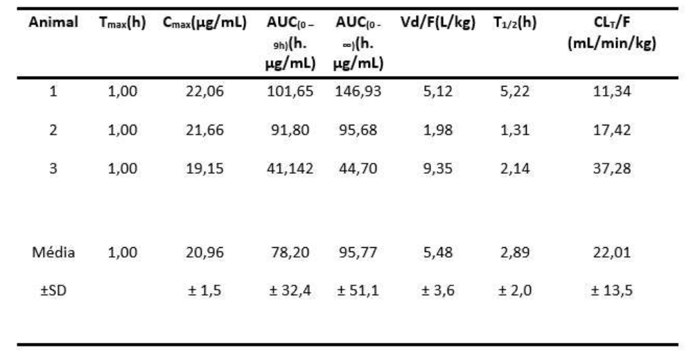
Tmáx (o tempo para atingir o pico de concentração); Cmax (pico da concentração plasmática máxima), AUC(0–9) (área sob a curva desde o tempo zero até 9h); AUC(0 - ∞) (área sob a curva do tempo zero ao infinito); MRT (tempo médio de residência); Vd/F (volume de distribuição aparente); T1/2 (tempo de meia vida de eliminação); F (biodisponibilidade); CL (Clearence).
Sobre os estudos do novo protótipo, é INCORRETO afirmar que:

Tmáx (o tempo para atingir o pico de concentração); Cmax (pico da concentração plasmática máxima), AUC(0–9) (área sob a curva desde o tempo zero até 9h); AUC(0 - ∞) (área sob a curva do tempo zero ao infinito); MRT (tempo médio de residência); Vd/F (volume de distribuição aparente); T1/2 (tempo de meia vida de eliminação); F (biodisponibilidade); CL (Clearence).
Sobre os estudos do novo protótipo, é INCORRETO afirmar que:
Provas
Questão presente nas seguintes provas
Observe as afirmativas a seguir sobre os estudos de metabolismo de medicamentos:
I. Durante o processo de desenvolvimento de medicamentos para avaliar o risco da interação de fármaco - fármaco baseados em citocromo CYP450 -, o primeiro tipo de estudo consiste em identificar a via metabólica do novo medicamento e a capacidade de outras moléculas terapêuticas pretendidas modificarem o metabolismo do novo medicamento.
II. Estudos mais complexos avaliam a possibilidade de o novo medicamento alterar o metabolismo de outros medicamentos.
III. As enzimas citocromo (CYP) do fígado metabolizam uma ampla gama de medicamentos, e mais de 90% das interações de fármaco - fármaco acontecem na etapa catalisada pela enzima CYP.
Das afirmativas acima:
I. Durante o processo de desenvolvimento de medicamentos para avaliar o risco da interação de fármaco - fármaco baseados em citocromo CYP450 -, o primeiro tipo de estudo consiste em identificar a via metabólica do novo medicamento e a capacidade de outras moléculas terapêuticas pretendidas modificarem o metabolismo do novo medicamento.
II. Estudos mais complexos avaliam a possibilidade de o novo medicamento alterar o metabolismo de outros medicamentos.
III. As enzimas citocromo (CYP) do fígado metabolizam uma ampla gama de medicamentos, e mais de 90% das interações de fármaco - fármaco acontecem na etapa catalisada pela enzima CYP.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
O composto CA apresentou atividade terapêutica promissora contra doenças metabólicas, incluindo demência e
osteoporose, e apresentou também efeito antibacteriano, antioxidante, anti-hipertensivo e antidiabético. A tabela abaixo
apresenta os parâmetros farmacocinéticos de CA no plasma de ratos Sprague Dawley (SD) machos após administração
oral (100 mg/kg, n=5, média ± DP) e intravenosa (10 mg/kg, n=5, média ± DP). Observe os parâmetros farmacocinéticos
do CA:

Cmax (pico da concentração plasmática máxima), Tmáx (o tempo para atingir o pico de concentração); T1/2 (tempo de meia vida de eliminação); AUC(0–∞) (área sob a curva do tempo zero ao infinito); Vd (volume de distribuição aparente); CL (Clearance); F (biodisponibilidade).
Sobre o assunto é possível afirmar que:
I. Uma taxa mais lenta de eliminação e depuração significa uma presença prolongada de CA na circulação sistêmica, conduzindo potencialmente a efeitos farmacológicos sustentados e desejáveis.
II. Um maior volume de distribuição e uma menor depuração conduzem a uma redução da meia-vida, o que também terá impacto na eficácia terapêutica da CA.
III. A biodisponibilidade absoluta do CA foi 38%, o que desempenha um papel crítico na determinação do regime de dosagem do CA e está intimamente relacionado com outros parâmetros farmacocinéticos primários, incluindo meia-vida e depuração.
Das afirmativas acima:

Cmax (pico da concentração plasmática máxima), Tmáx (o tempo para atingir o pico de concentração); T1/2 (tempo de meia vida de eliminação); AUC(0–∞) (área sob a curva do tempo zero ao infinito); Vd (volume de distribuição aparente); CL (Clearance); F (biodisponibilidade).
Sobre o assunto é possível afirmar que:
I. Uma taxa mais lenta de eliminação e depuração significa uma presença prolongada de CA na circulação sistêmica, conduzindo potencialmente a efeitos farmacológicos sustentados e desejáveis.
II. Um maior volume de distribuição e uma menor depuração conduzem a uma redução da meia-vida, o que também terá impacto na eficácia terapêutica da CA.
III. A biodisponibilidade absoluta do CA foi 38%, o que desempenha um papel crítico na determinação do regime de dosagem do CA e está intimamente relacionado com outros parâmetros farmacocinéticos primários, incluindo meia-vida e depuração.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
A determinação quantitativa de substâncias em
amostras biológicas por métodos de cromatografia líquida
acoplada à espectrometria de massas inclui a construção e
avaliação de curvas de calibração, utilizando-se a mesma
matriz proposta para o estudo, adicionadas da substância
alvo a analisar, em diferentes concentrações, acrescidas
de uma concentração fixa do padrão interno. Observe as
afirmativas a seguir, em relação à curva de calibração:
I – caso a variância do erro não seja constante em toda a faixa de quantificação do método analítico, deve ser utilizado o método dos mínimos quadrados ponderados, usando a ponderação que apresentar o menor valor para soma dos erros relativos dos valores nominais dos padrões de calibração versus seus valores obtidos pela equação da curva.
II – somente o modelo linear pode ser usado para a construção da equação matemática que descreve a curva de calibração.
III – um modelo não linear pode ser empregado para a construção da equação da curva de calibração, desde que seja demonstrado matematicamente que o modelo linear não é adequado.
Sobre as afirmativas acima, pode-se dizer que apenas:
I – caso a variância do erro não seja constante em toda a faixa de quantificação do método analítico, deve ser utilizado o método dos mínimos quadrados ponderados, usando a ponderação que apresentar o menor valor para soma dos erros relativos dos valores nominais dos padrões de calibração versus seus valores obtidos pela equação da curva.
II – somente o modelo linear pode ser usado para a construção da equação matemática que descreve a curva de calibração.
III – um modelo não linear pode ser empregado para a construção da equação da curva de calibração, desde que seja demonstrado matematicamente que o modelo linear não é adequado.
Sobre as afirmativas acima, pode-se dizer que apenas:
Provas
Questão presente nas seguintes provas
A figura abaixo apresenta cromatogramas de íons extraídos provenientes do uso de padrões internos (IS, do inglês
internal standard) adicionados à amostra biológica objeto de análise antes do preparo da amostra, a fim de efetuar a
análise quantitativa do analito alvo (A) por cromatografia a líquido acoplada à espectrometria de massas sequencial.
Pode-se dizer que nos casos (a), (b) e (c), o padrão interno usado, respectivamente, é uma substância:
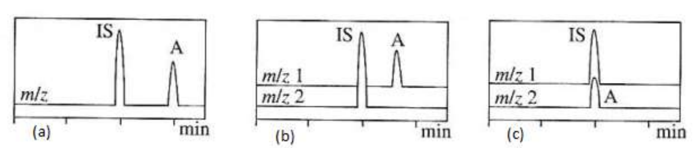
Cromatogramas de íons extraídos apresentando um padrão interno (IS) e um analito alvo (A). Fonte: Lavagnini et al. Quantitative Applications of Mass Spectrometry. John Wiley & Sons Ltd, Chichester, England, 2006.

Cromatogramas de íons extraídos apresentando um padrão interno (IS) e um analito alvo (A). Fonte: Lavagnini et al. Quantitative Applications of Mass Spectrometry. John Wiley & Sons Ltd, Chichester, England, 2006.
Provas
Questão presente nas seguintes provas
A Resolução Anvisa RDC n° 27, de 17 de maio de 2012
dispõe sobre requisitos mínimos para a validação de métodos bioanalíticos empregados em estudos com fins de registro e pós-registro de medicamentos. A validação do método
para a determinação quantitativa de analitos em matrizes
biológicas inclui a construção e avaliação de no mínimo
três curvas de calibração com diferentes concentrações do
padrão do analito adicionados de padrão interno (PI). Para
métodos de cromatografia a líquido acoplada à espectrometria de massas, deve ser utilizado, preferencialmente,
PI marcado com isótopo estável. Observe as afirmativas a
seguir, em relação aos requisitos para PI deuterados:
I – pelo menos 5 átomos de deutério (2H) devem estar presentes na molécula do PI deuterado, a fim de levar a uma diferença de massa de 10 unidades em relação ao analito alvo.
II – os átomos de deutério (2H) devem estar localizados em posições bem definidas da molécula, sem modificação da esteroquímica da molécula.
III – os átomos de deutério (2H) devem estar inseridos em posições estáveis na molécula, sem a possibilidade de troca com átomos de hidrogênio (1H) durante o uso e armazenamento do PI.
Sobre as afirmativas acima, pode-se dizer que:
I – pelo menos 5 átomos de deutério (2H) devem estar presentes na molécula do PI deuterado, a fim de levar a uma diferença de massa de 10 unidades em relação ao analito alvo.
II – os átomos de deutério (2H) devem estar localizados em posições bem definidas da molécula, sem modificação da esteroquímica da molécula.
III – os átomos de deutério (2H) devem estar inseridos em posições estáveis na molécula, sem a possibilidade de troca com átomos de hidrogênio (1H) durante o uso e armazenamento do PI.
Sobre as afirmativas acima, pode-se dizer que:
Provas
Questão presente nas seguintes provas
A injeção direta de amostras biológicas, matrizes
extremamente complexas, em sistemas cromatográficos
convencionais não é indicada, e uma etapa de preparação
de amostra geralmente é necessária. Entre as técnicas
de extração rápidas e simples utilizadas para o preparo
de amostras biológicas para análise por cromatografia a
líquido acoplada à espectrometria de massas (LC-MS), a
que se baseia no equilíbrio de sorção do analito presente
na amostra com o sorvente, em que a amostra é misturada
dinamicamente com o sorvente por meio da aspiração de
ar, é conhecida como:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container