Foram encontradas 348 questões.
O pigmento envolvido na captura de luz durante o processo de fotossíntese é a clorofila, pertencente à classe das porfirinas. Considerando isso, assinale a opção correta.
Com relação aos diferentes tipos de clorofilas, é correto afirmar que
Provas

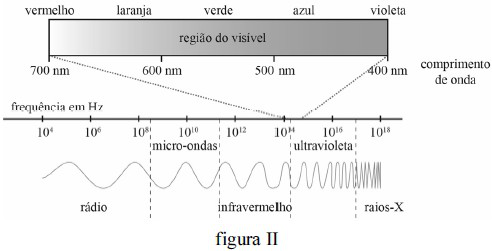
Anteriormente, a figura I mostra o diagrama de funcionamento de um experimento de interferência de luz (experimento de Young), por duas fendas, separadas por 0,01 mm; a figura II apresenta o diagrama do espectro eletromagnético em função do comprimento de onda e frequência. Na figura I, a segunda linha brilhante, m = 2, é formada, no anteparo, a um ângulo !$ \theta !$ em relação ao feixe incidente horizontal tal que sen!$ \theta !$ = 0,2.
Com base nessas informações, julgue o item.
O comprimento de onda referente à quarta linha brilhante, m = 2, localiza-se fora da região do visível no espectro eletromagnético.
Provas


Anteriormente, a figura I mostra o diagrama de funcionamento de um experimento de interferência de luz (experimento de Young), por duas fendas, separadas por 0,01 mm; a figura II apresenta o diagrama do espectro eletromagnético em função do comprimento de onda e frequência. Na figura I, a segunda linha brilhante, m = 2, é formada, no anteparo, a um ângulo !$ \theta !$ em relação ao feixe incidente horizontal tal que sen!$ \theta !$ = 0,2.
Com base nessas informações, julgue o item.
Nesse caso, a interferência construtiva de ordem mais alta possível é para a linha brilhante m = 100.
Provas
Liquens são organismos formados por associação interespecífica entre algas e fungos. Eles são conhecidos bioindicadores dos níveis de poluição atmosférica, pois são extremamente sensíveis a alterações ambientais. Assim, a presença de liquens sugere baixo índice de poluição, ao passo que seu desaparecimento sugere agravamento da poluição ambiental.
Acerca desse assunto, assinale a opção correta.
Os liquens formam um exemplo de importante associação ecológica conhecida como
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.
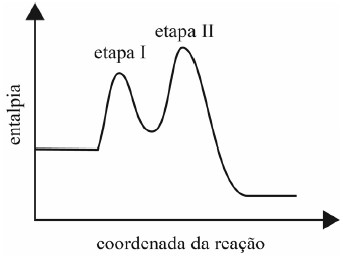
Com base nessas informações, julgue o item subsequente.
Dados o mecanismo e o perfil de variação de entalpia, infere-se que a decomposição do peróxido de hidrogênio na presença de HBr é uma reação com cinética de segunda ordem.
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.

Com base nessas informações, julgue o item subsequente.
Na etapa I, o peróxido de hidrogênio atua como redutor, e, na etapa II, como oxidante.
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.

Com base nessas informações, julgue o item subsequente.
O íon brometo, apesar de reagir na etapa I, atua como catalisador do processo de decomposição do peróxido de hidrogênio.
Provas
O peróxido de hidrogênio (H2O2), um dos agentes mais empregados em desinfecções, decompõe-se lentamente em água e oxigênio, conforme se observa na equação que se segue.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Esse processo pode ser acelerado pela adição de HBr, cujo mecanismo envolve duas etapas, conforme as representações I e II, a seguir.
I 2Br− (aq) + H2O2 (aq) + 2 H+ (aq) → Br2 (aq) + 2 H2O (l)
II Br2 (aq) + H2O2 (aq) → 2 Br− (aq) + 2 H+ (aq) + O2 (g)
No gráfico seguinte, é representada a variação da entalpia em função da coordenada da reação referente ao mecanismo anterior nas condições padrão.

Com base nessas informações, julgue o item subsequente.
No processo de decomposição do peróxido de hidrogênio em condições padrão, a energia absorvida para romper as ligações da molécula de H2O2 é superior à energia liberada na formação das ligações das moléculas H2O e O2.
Provas
A titulação é uma técnica muito utilizada na química para determinar a quantidade de uma espécie química em uma solução (amostra). Na titulação, uma segunda solução, de concentração conhecida de outra espécie que reage com a primeira e cuja concentração se deseja determinar, é adicionada gradualmente à amostra que contém a substância, ou espécie, de interesse.
Com base nesses princípios, um estudante idealizou um experimento para determinar a quantidade de CO2 contida em um cilindro rígido, tendo realizado o trabalho em três etapas:
I borbulhou o CO2 em água destilada, de modo que todo o CO2 contido no cilindro se transformasse em H2CO3, formando uma solução desse ácido;
II titulou, completamente, a solução de H2CO3 preparada, com uma solução de NaOH de concentração 0,1 mol/L;
III determinou, por meio de cálculos estequiométricos, o volume de CO2 inicialmente contido no cilindro, considerando todas as condições do experimento ideais e rendimentos reacionais completos.
Tendo como referência o texto e a situação hipotética precedentes, julgue o item.
O aumento tanto da pressão parcial de CO2 quanto da temperatura da água destilada torna a etapa I mais eficiente.
Provas
A titulação é uma técnica muito utilizada na química para determinar a quantidade de uma espécie química em uma solução (amostra). Na titulação, uma segunda solução, de concentração conhecida de outra espécie que reage com a primeira e cuja concentração se deseja determinar, é adicionada gradualmente à amostra que contém a substância, ou espécie, de interesse.
Com base nesses princípios, um estudante idealizou um experimento para determinar a quantidade de CO2 contida em um cilindro rígido, tendo realizado o trabalho em três etapas:
I borbulhou o CO2 em água destilada, de modo que todo o CO2 contido no cilindro se transformasse em H2CO3, formando uma solução desse ácido;
II titulou, completamente, a solução de H2CO3 preparada, com uma solução de NaOH de concentração 0,1 mol/L;
III determinou, por meio de cálculos estequiométricos, o volume de CO2 inicialmente contido no cilindro, considerando todas as condições do experimento ideais e rendimentos reacionais completos.
Tendo como referência o texto e a situação hipotética precedentes, julgue o item.
Considere que, no experimento citado, a amostra de CO2 estivesse sob pressão de 20 atm no cilindro rígido em questão, pela manhã, a uma temperatura ambiente de 10 ºC. Considere, também, que à tarde a temperatura ambiente tenha chegado a 30 ºC e que, tanto de manhã quanto à tarde, a temperatura do cilindro tenha sido igual à temperatura ambiente. Nesse caso, à tarde a pressão no cilindro seria maior que 50 atm.
Provas
Caderno Container