Foram encontradas 40 questões.
Para viabilizar um medicamento adequado ao público
pediátrico para o tratamento da doença de Chagas, um
laboratório farmacêutico oficial iniciou um projeto para o
desenvolvimento de comprimidos orodispersíveis contendo
um insumo farmacêutico ativo (IFA) de primeira linha.
Seguindo o desenvolvimento do produto pela abordagem de
Quality by Design, foi elaborado o perfil alvo de qualidade
do produto (QTPP). Observe as afirmativas a seguir em
relação ao QTPP para o produto:
I – Sendo o registro do produto feito como medicamento genérico, o QTPP deve ser elaborado considerando a comparação da formulação entre o produto teste e o produto de referência, baseada principalmente nas características de desempenho do produto.
II – O QTPP pode incluir características do produto em questão, como uso pretendido, via de administração, dissolução, teor, assim como características de desempenho para os métodos analíticos utilizados, como precisão e exatidão.
III – O tempo de desintegração e o tempo de molhamento podem ser considerados no QTPP do produto, podendo incluir no perfil alvo qualquer característica que idealmente será alcançada para garantir a qualidade do medicamento.
IV – As características listadas no QTPP contribuem para a definição dos atributos críticos de qualidade (CQAs) que serão posteriormente identificados.
V – A elaboração do QTPP apresenta relação com o desenvolvimento de um medicamento com padrões de qualidade centrados no paciente.
Das afirmativas acima:
I – Sendo o registro do produto feito como medicamento genérico, o QTPP deve ser elaborado considerando a comparação da formulação entre o produto teste e o produto de referência, baseada principalmente nas características de desempenho do produto.
II – O QTPP pode incluir características do produto em questão, como uso pretendido, via de administração, dissolução, teor, assim como características de desempenho para os métodos analíticos utilizados, como precisão e exatidão.
III – O tempo de desintegração e o tempo de molhamento podem ser considerados no QTPP do produto, podendo incluir no perfil alvo qualquer característica que idealmente será alcançada para garantir a qualidade do medicamento.
IV – As características listadas no QTPP contribuem para a definição dos atributos críticos de qualidade (CQAs) que serão posteriormente identificados.
V – A elaboração do QTPP apresenta relação com o desenvolvimento de um medicamento com padrões de qualidade centrados no paciente.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
Foi aberto um projeto de desenvolvimento de um medicamento contendo um antirretroviral da classe II do sistema
de classificação biofarmacêutica, fabricado como comprimidos de liberação imediata. Durante o desenvolvimento do
produto, foram avaliados os perfis de dissolução em 12 cubas nas condições descritas em monografia farmacopeica
sendo elas: 900 mL de meio tampão acetato pH 4,5 com
0,5% de lauril sulfato de sódio a 37 ºC, aparato cesta com
rotação de 75 rpm e com a quantificação por espectroscopia no ultravioleta-visível. Diferentes formulações foram
avaliadas e todas apresentaram semelhança no perfil de
dissolução, porém, foi observado um desvio padrão relativo
maior do que 20% nos primeiros tempos do perfil (5 e 10
minutos) e maior do que 10% nos demais tempos do perfil
(15, 30 e 45 minutos). Sobre o ensaio de perfil dissolução
em questão, pode-se afirmar que:
Provas
Questão presente nas seguintes provas
No desenvolvimento de um medicamento na forma
farmacêutica suspensão oral em veículo aquoso contendo
um insumo farmacêutico ativo (IFA) da classe II do sistema
de classificação biofarmacêutica, foram produzidos três
lotes experimentais sendo cada lote produzido com o IFA de
diferentes fabricantes. O Dossiê de Insumo Farmacêutico
Ativo (DIFA) dos três fabricantes apresenta a informação de
que o IFA é uma forma hidratada e apresenta informações
em relação à posição dos picos de difração em 2 teta. Estão
descritos no DIFA do fabricante A picos de difração em 5,5°,
7,2°, 12,8°, 15,7° e 21,4° com a análise feita com radiação
de cobre (λ =1,5406 Å), no do fabricante B em 5,5°, 7,3°,
12,7°, 15,8° e 21,4° com a análise feita com radiação de
cobre (λ =1,5406 Å) e no do fabricante C em 2,5°, 11,4°,
17,6°, 18,2°, 19,1° e 24,3° com a análise feita com radiação
de cobalto (λ=1,7890 Å). Considerando o exposto, observe
as afirmativas abaixo:
I – É plausível afirmar que o IFA do fabricante B apresenta a mesma forma sólida do fabricante A, não sendo possível garantir que ambos contêm uma única forma sólida, uma vez que os padrões de difração de raios X não foram apresentados.
II – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes B e C podem apresentar diferentes graus de hidratação ou são polimorfos do hidrato de mesma estequiometria.
III – A titulação Karl-Fisher não permite a diferenciação da água de superfície e da água e incorporada na estrutura cristalina do hidrato.
IV – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes A, B e C podem ser selecionados para o desenvolvimento do produto, pois, já que as propriedades físico-químicas dos IFAs são as mesmas não haverá diferenças no desempenho da formulação.
V – É importante a avaliação da interconversão entre as formas sólidas do IFA, uma vez que, em suspensão, pode ocorrer a transição para a forma estável, resultando em crescimento cristalino com consequente alteração na distribuição do tamanho das partículas, o que pode afetar a estabilidade física da suspensão.
Das afirmativas acima:
I – É plausível afirmar que o IFA do fabricante B apresenta a mesma forma sólida do fabricante A, não sendo possível garantir que ambos contêm uma única forma sólida, uma vez que os padrões de difração de raios X não foram apresentados.
II – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes B e C podem apresentar diferentes graus de hidratação ou são polimorfos do hidrato de mesma estequiometria.
III – A titulação Karl-Fisher não permite a diferenciação da água de superfície e da água e incorporada na estrutura cristalina do hidrato.
IV – Considerando a informação do DIFA que os IFAs são hidratos, os fabricantes A, B e C podem ser selecionados para o desenvolvimento do produto, pois, já que as propriedades físico-químicas dos IFAs são as mesmas não haverá diferenças no desempenho da formulação.
V – É importante a avaliação da interconversão entre as formas sólidas do IFA, uma vez que, em suspensão, pode ocorrer a transição para a forma estável, resultando em crescimento cristalino com consequente alteração na distribuição do tamanho das partículas, o que pode afetar a estabilidade física da suspensão.
Das afirmativas acima:
Provas
Questão presente nas seguintes provas
A validação do processo envolve uma série de atividades que ocorrem durante o ciclo de vida do produto e
do processo. Sobre as fases da validação de processos, é
correto afirmar que:
Provas
Questão presente nas seguintes provas
O Guia ICH Q8 aborda duas estratégias para o desenvolvimento farmacêutico, sendo elas a abordagem mínima e
a abordagem aprimorada, conforme apresentado na Coluna
I. Estabeleça a correta correspondência com os aspectos
da Coluna II.
Coluna I
1. abordagem mínima. 2. abordagem aprimorada.
Coluna II
( ) principalmente empírica com o desenvolvimento geralmente realizado avaliando-se uma variável por vez.
( ) a qualidade do medicamento é garantida por uma estratégia de controle baseada em riscos.
( ) o gerenciamento do ciclo de vida é reativo (ou seja, solução de problemas e ação corretiva).
( ) o processo de fabricação é ajustável dentro do design space.
( ) abordagem de ciclo de vida para validação de processo, idealmente com a verificação continuada do processo.
A sequência correta, de cima para baixo, é:
Coluna I
1. abordagem mínima. 2. abordagem aprimorada.
Coluna II
( ) principalmente empírica com o desenvolvimento geralmente realizado avaliando-se uma variável por vez.
( ) a qualidade do medicamento é garantida por uma estratégia de controle baseada em riscos.
( ) o gerenciamento do ciclo de vida é reativo (ou seja, solução de problemas e ação corretiva).
( ) o processo de fabricação é ajustável dentro do design space.
( ) abordagem de ciclo de vida para validação de processo, idealmente com a verificação continuada do processo.
A sequência correta, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
As embalagens farmacêuticas desempenham papel
crucial na preservação da integridade dos medicamentos,
fornecendo proteção contra fatores ambientais como luz,
umidade e contaminação. Avalie as afirmativas abaixo sobre
materiais de embalagem primária de fármacos:
I – É permitido que a empresa solicite o registro de um medicamento em mais de um material de embalagem primária.
II – O vidro tipo I, também denominado vidro borossilicato, é o único tipo de vidro que pode ser utilizado para medicamentos de uso humano por ser totalmente inerte e não trazer riscos de incompatibilidade com a forma farmacêutica.
III – Polímeros termoplásticos podem ser usados para a tecnologia blow-fill-seal, na qual as etapas de formação da embalagem, enchimento com o produto farmacêutico e selagem do sistema final ocorrem em operação contínua.
IV – Embalagens termomoldáveis devem conter plastificantes em suas composições, permitindo a redução da temperatura de transição vítrea dos polímeros para que as temperaturas de processo possam ser reduzidas. São exemplos de plastificantes de embalagens termomoldáveis os ftalatos.
As afirmativas I, II e III e IV são respectivamente:
I – É permitido que a empresa solicite o registro de um medicamento em mais de um material de embalagem primária.
II – O vidro tipo I, também denominado vidro borossilicato, é o único tipo de vidro que pode ser utilizado para medicamentos de uso humano por ser totalmente inerte e não trazer riscos de incompatibilidade com a forma farmacêutica.
III – Polímeros termoplásticos podem ser usados para a tecnologia blow-fill-seal, na qual as etapas de formação da embalagem, enchimento com o produto farmacêutico e selagem do sistema final ocorrem em operação contínua.
IV – Embalagens termomoldáveis devem conter plastificantes em suas composições, permitindo a redução da temperatura de transição vítrea dos polímeros para que as temperaturas de processo possam ser reduzidas. São exemplos de plastificantes de embalagens termomoldáveis os ftalatos.
As afirmativas I, II e III e IV são respectivamente:
Provas
Questão presente nas seguintes provas
Os métodos espectroscópicos desempenham um papel fundamental na análise de medicamentos, permitindo
a identificação e a quantificação de fármacos e outras
substâncias nas matérias-primas e no produto acabado.
Sobre as técnicas espectroscópicas para identificação e
quantificação de insumos farmacêuticos ativos, é correto
afirmar que:
Provas
Questão presente nas seguintes provas
Em relação ao desenvolvimento de método de dissolução para formas farmacêuticas sólidas, avalie se são
verdadeiras (V) ou falsas (F) as afirmativas a seguir:
I – O perfil de dissolução é uma ferramenta importante durante o desenvolvimento do método, pois permite o estabelecimento das condições e das especificações mais adequadas para o controle do desempenho do produto.
II - Volumes de meio de dissolução que não atendam à condição sink podem ser utilizados desde que justificados e desde que haja comprovação da capacidade discriminativa do método.
III - A determinação do poder discriminativo do método de dissolução pode ser realizada por meio da inclusão de lotes que não foram capazes de demonstrar perfil farmacocinético aceitável in vivo.
As afirmativas I, II e III são respectivamente:
I – O perfil de dissolução é uma ferramenta importante durante o desenvolvimento do método, pois permite o estabelecimento das condições e das especificações mais adequadas para o controle do desempenho do produto.
II - Volumes de meio de dissolução que não atendam à condição sink podem ser utilizados desde que justificados e desde que haja comprovação da capacidade discriminativa do método.
III - A determinação do poder discriminativo do método de dissolução pode ser realizada por meio da inclusão de lotes que não foram capazes de demonstrar perfil farmacocinético aceitável in vivo.
As afirmativas I, II e III são respectivamente:
Provas
Questão presente nas seguintes provas
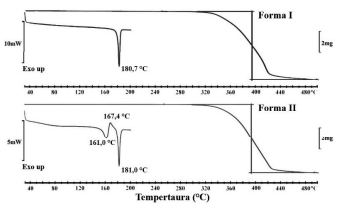
A figura abaixo apresenta as curvas de calorimetria diferencial exploratória (DSC) e de análise termogravimétrica
(TGA) de duas formas sólidas de um insumo farmacêutico
ativo (IFA). Sobre as figuras, pode-se afirmar que:

Provas
Questão presente nas seguintes provas
A figura abaixo apresenta os padrões experimentais de
difração de raios X de pó (DRXP) de 5 amostras (A1, A2, A3,
A4 e A5), obtidos nas mesmas condições de análise, de um
insumo farmacêutico ativo (IFA). A partir destes resultados,
pode-se interpretar que:


Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container