Foram encontradas 35.936 questões.
Calcule o pH de uma solução obtida pela mistura de 100 mL de HCI 0,45M com 200 mL de HNO3 0,60M e assinale a opção correta.
Dados:
log 0,11 = -0,96;
log 0,22 = -0,66;
log 0,33 = -0,48;
log 0,44 = -0,36; e
log 0,55 = -0,26.
Provas
Uma mistura de etano, propano e benzeno foi injetada em um cromatógrafo a gás. O etano produziu um pico fino após 64s de injeção, enquanto o propano e benzeno produziram um pico fino após 96s e 256s, respectivamente. Sabendo disso, analise as afirmativas abaixo:
I- O fator de retenção do benzeno é de 3.
II- O tempo de retenção ajustado do benzeno é de 160s.
III- O fator de retenção do propano é de 2.
IV- O tempo de retenção ajustado do propano é de 32s.
Assinale a opção correta.
Provas
Em relação ao estudo da Eletroquímica, coloque F (falso) ou V (verdadeiro) nas afirmativas abaixo e assinale a opção correta.
( ) A atividade de um íon numa solução é a disponibilidade efetiva do íon na solução. De modo geral, os íons existentes numa solução podem ser considerados como espécies isoladas, já que não são influenciados pelos íons e moléculas polares vizinhos.
( ) O potencial, medido em volt, desenvolvido em um metal imerso em uma solução 1 M de seus íons, é chamado potencial padrão ou potencial normal.
( ) A ponte salina é responsável por estabelecer a condutância iônica, unindo os dois eletrólitos de uma pilha eletroquímica.
( ) Um eletrodo é denominado cátodo quando ocorre nele uma reação de oxidação.
Provas
Referente aos conceitos das Teorias de Ácido-Base, assinale a opção correta.
Provas
O grupo formado em uma ligação peptídica, isto é, em uma ligação entre dois aminoácidos, como no caso do ácido aspártico e da fenilalanina, é característico de qual função orgânica?
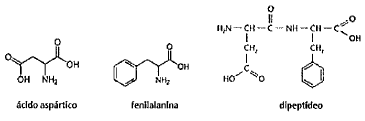
Provas
Segundo Lewis, a ligação covalente consiste em um par de elétrons compartilhado por dois átomos. As características de uma ligação covalente entre dois átomos são decorrentes principalmente das propriedades desses átomos. Com relação à força da ligação covalente, é correto afirmar que:
Provas
Considere uma· solução de 0,635 M de ácido malônico (HO2CCH2CO2H). Quais são as concentrações molares na solução, em mol/L, dos íons [O2CCH2CO2H]" e [O2CCH2CO2]2-, respectivamente?
Dados: Constantes de dissociação ácida K1 = 1,42x10-3 e K2 = 2x10-6
Provas
O modelo de Repulsão dos Pares de Elétrons da Camada de Valência pode ser estendido para moléculas mais complexas, de modo que, quando existe mais de um átomo central, as ligações de cada átomo são tratadas independentemente. Considere a molécula de ácido acético (CH3COOH) e assinale a opção que apresenta a geometria molecular formada ao redor do átomo de carbono do grupamento carboxila.
Provas
Em um recipiente foi colocado um gás hipotético (A) a uma pressão de 0,6 atm. O composto se decompôs nos gases (B) e (C) até alcançar o equilíbrio dinâmico conforme a reação balanceada abaixo:
A(g) !$ \rightleftharpoons !$ B(g) + C(g)
Assim, assinale a opção que apresenta as pressões parciais dos gases no equilíbrio.
Dados: K = 7,6 ; e
!$ \surd !$19 = 4,36
Provas
O Silício é um elemento do Grupo 14 da Tabela Periódica e é importante em um grande número de processos em larga escala, sendo que grande parte do silício produzido é adicionado ao Fe para fabricação de ligas resistentes à corrosão, pela reação:
SiO2 + Fe + 2C → FeSi + 2CO
Supondo um rendimento de reação de 80%, qual é a quantidade mínima de Fe e SiO2, respectivamente, para a produção de 2.100 kg de FeSi?
Dado: massas molares
MFe = 56 g/mol;
MSi = 28 g/mol; e
Mo= 16 g/mol.
Provas
Caderno Container