Foram encontradas 36.174 questões.
Medidas invariavelmente envolvem erros e incertezas. Apenas alguns deles ocorrem devido a equívocos cometidos pelo analista. Mais comumente, os erros são causados por padronizações ou calibrações malfeitas ou variações aleatórias e incertezas nos resultados. […] No limite, entretanto, os erros envolvidos nas medidas são uma parte inerente do mundo quantitativo em que vivemos. Por conta disso, é impossível realizar uma análise química que seja totalmente livre de erros ou incertezas.
ATKINS, Peter; JONES, Loretta. Princípios de Química: questionando a vida moderna e o meio ambiente. Tradução: Ignez Caracelli et al. Bookman, 2001. (original: 1999).
Diante do exposto, é inadequado admitir que uma única análise possa fornecer informações sobre a variabilidade dos resultados. Para realizar um procedimento analítico de forma completa, os químicos costumam repetir um experimento entre duas e cincos vezes (réplicas). Uma vez que exista um conjunto de medidas para uma determinada análise, dois termos emergem como sendo relevantes na interpretação dos resultados, sendo eles:
- Precisão: é a proximidade dos resultados em relação aos demais, obtidos exatamente da mesma forma.
- Exatidão: é a proximidade de um valor medido em relação ao valor verdadeiro ou aceito.
Utilizando um jogo de dardos como modelo de experimento, tem se que o resultado ideal pode ser representado pela Figura 1, em que a maioria dos resultados atinge o centro do alvo.
Figura 1: Resultado ideal alta precisão e alta exatidão

Figura 2: Representação dos alvos A e B

Analisando os alvos A e B representados na Figura 2, verifica se que seus resultados tiveram respectivamente:
Provas
A história da Tabela Periódica pode ser comparada a uma larga avenida de duas mãos. Num primeiro sentido, foram sendo lentamente descobertos diversos elementos químicos, pelas razões e métodos os mais distintos. Depois de se conhecerem algumas dezenas de elementos, passou se a buscar correlações entre eles, para se entender suas peculiaridades, afinidades e reatividades. […] Dessa maneira se passou do conjunto de 63 elementos, conhecidos ao tempo de Mendeleev, aos 118 que constituem a Tabela Periódica moderna.
LIMA, G. M.; BARBOSA, L. C. A.; FILGUEIRAS, C. A. L. Origens e consequências da tabela periódica, a mais concisa enciclopédia criada pelo ser humano Quim. Nova, v. 42, n. 10, p. 1125 1145, 2019.
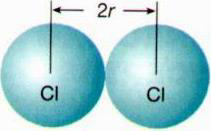
Dentre as propriedades contempladas na tabela periódica, está o raio atômico, que pode ser estimado a partir das distâncias entre os núcleos de dois átomos ligados entre si (Figura 1).
Figura 1: Esquema para a estimativa do raio atômico do átomo de cloro a partir da molécula de Cl2
O tamanho de um determinado átomo está relacionado com o número de partículas que ele contém e também com a distribuição dos elétrons pelos seus níveis de energia. De maneira geral, a tabela periódica indica que o raio atômico de um átomo aumenta ao longo de um mesmo grupo e diminui ao longo de um mesmo período, ou seja, aumenta de cima para baixo e da direita para a esquerda (Figura 2).
Figura 2: Tendência nos valores de raios atômicos de elementos da tabela periódica
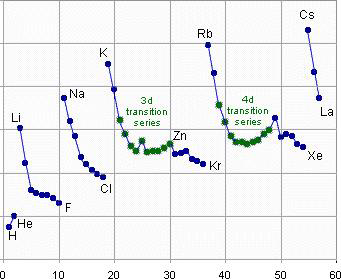
Levando se em consideração o aumento do número atômico ao longo do período, o efeito responsável por essa tendência atípica é:
Provas
A teoria dos orbitais moleculares (TOM) descreve as ligações covalentes em termos de orbitais moleculares (OM), que resultam da interação entre os orbitais atômicos (OA) dos átomos envolvidos na ligação e estão associados a moléculas como um todo. A diferença entre um orbital molecular e um orbital atômico é que este último está associado a somente um átomo.
ATKINS, Peter; JONES, Loretta. Princípios de Química: questionando a vida moderna e o meio ambiente. Tradução: Ignez Caracelli et al. Bookman, 2001. (original: 1999).
Considerando que a TOM constitui uma maneira válida de entender a formação de ligações químicas, os elétrons de valência têm uma influência na estabilidade da molécula. Assim, na formação dos orbitais moleculares a partir dos orbitais atômicos envolvidos na obtenção de uma nova molécula, verifica se que:
Provas
A denominação de água pura pode ter diferentes interpretações, a depender da finalidade de seu uso (doméstico, indústria farmacêutica ou laboratórios). A tabela, a seguir, define a classe de água reagente, segundo o National Committe for Clinical Laboratory Standards (NCCLS). Analise os tipos de água reagente observados na tabela e relacione-os com sua aplicação correta em laboratórios de pesquisa e/ou ensino nas áreas da saúde:
NCCLS | |||
Tipo I | Tipo II | Tipo III | |
Bactérias heterotróficas (UFC/mL) | < 10 | < 1000 | - |
Resistividade (MΩ/cm a 25 ºC) | > 10 | > 1 | > 0,1 |
Condutividade (mS/cm a 25 ºC) | < 0,1 | < 1 | < 10 |
Silicatos (mg/L) | < 0,05 | < 0,1 | < 1 |
Carbono orgânico (TOC) ng/g (ppb) | - | - | - |
Partícula (µm) | < 0,22 | - | - |
( - ) Não indicado | |||
Provas
Todo laboratório de manipulação de reagentes químicos possui vidrarias adequadas às suas atividades. As vidrarias, os equipamentos e os utensílios devem ser mantidos limpos, desinfetados e guardados em local apropriado. Uma dessas vidrarias é de uso geral em laboratórios, apresenta diversos volumes e é utilizada para dissolução, pesagem ou aquecimento de substâncias, podendo ser de vidro ou plástico. A medida realizada com este tipo de vidraria é muito imprecisa, podendo ela ser graduada ou não. Quando feita de vidro refratário, pode ser utilizada para aquecimento em uma ampla faixa de variação de temperatura. A vidraria descrita corresponde
Provas
O cloridrato de xilazina foi o primeiro alfa2-agonista amplamente utilizado em grandes animais e continua sendo o mais comumente administrado em ruminantes. Seguindo dosagem recomendada de 0,05 mg/kg, por via intravenosa, para um bovino de 400 kg de peso corporal, o volume a ser administrado de cloridrato de xilazina a 2% é:
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Considerando o coeficiente de solubilidade do bicarbonato de sódio igual a 9,6 g/100 mL de água a 20 °C, ao diluir-se 4,0 g de NaHCO3 em 50 mL de água a 20 °C, a solução formada será do tipo
Provas
Em situação hipotética, para a realização de uma aula prática, é necessário preparar uma solução aquosa de cloreto de sódio a 2,1 mol/L. Considerando a massa molar aproximada Na=23 e Cl=35, qual a quantidade aproximada necessária de NaCl para uma diluição em 100 mL de água?
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Na mistura de soluções, “os indicadores são substâncias que servem para indicar a viragem e o ponto de titulação, ou seja, de acordo com o indicador utilizado será indicado o ponto final da titulação com a mudança de cor ou precipitação de substância”
(MELZER, EHRICK EDUARDO MARTINS. Preparo de soluções: reações e interações químicas. 1 ed. São Paulo: Érica, 2014, p. 111).
Assim sendo, qual indicador tem função de detectar a presença de amido e estruturas químicas similares?
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Considere as soluções 1 e 2 a seguir:
Solução 1: concentração = 4,0 g/L e volume = 200 mL
Solução 2: concentração = 6,0 g/L e volume = 300 mL
Ao misturar os volumes totais das soluções 1 e 2, a concentração final da solução resultante é:
Provas
Caderno Container