Foram encontradas 36.174 questões.
Observação: Caso necessário, utilize a Tabela Periódica.
O etanol é um composto que apresenta uma gama de aplicações, dentre as quais se destacam o uso como fonte renovável de combustível e como matéria-prima de tintas, solventes, aerossóis, fabricação de detergentes e produtos têxteis. Grande parte do etanol produzido no Brasil é proveniente da cana de açúcar, a partir de um processo dividido em várias etapas, tais como a moagem da cana de açúcar, produção do melaço, fermentação do melaço, e destilação do mosto fermentado. Outra forma de produção do etanol ocorre por meio de uma reação entre o carbono grafite, o hidrogênio e o oxigênio, conforme mostra a equação química a seguir:
!$ 2C_{(graf)}+3H_{2(g)}+1⁄2\ O_{2(g)}→C_2H_6O_{(l)} !$
Considere as seguintes equações que representam os processos de combustão:
Eq. 1: combustão completa do carbono grafite !$ (C_{graf}) !$
!$ C_{(graf)}+O_{2(g)}→CO_{2(g)\ }\quad\quad !$ !$ ΔH=-394kJmol^{-1}; !$
Eq. 2: combustão do hidrogênio gasoso
!$ H_{2(g)}+1⁄2\ O_{2(g)}→H_2O_{(l)}\ \quad\quadΔH=-286kJmol^{-1}; !$
Eq. 3: combustão completa do etanol
!$ C_2H_6O_{(l)}+3O_{2\left(g\right)}→2CO_{2(g)}+3H_2O_{(l)}\ \quad\quadΔH=-1368kJmol^{-1}; !$
Empregando a Lei de Hess e as equações representativas de combustão, verifica-se que a entalpia de formação do etanol, a partir do grafite, é igual a
Provas
- FundamentosTransformações: Estados Físicos e Fenômenos
- Química CinéticaRepresentação das Transformações Químicas
Observação: Caso necessário, utilize a Tabela Periódica.
Em um artigo publicado, em 2018, na revista Visão Acadêmica*, do curso de Farmácia da Universidade Federal do Paraná (UFPR), os autores buscaram desenvolver um padrão secundário para o medicamento cloridrato de tramadol. A substância escolhida para o desenvolvimento do padrão secundário foi o ácido perclórico (HClO₄). No entanto, no processo de titulação, para a validação de um padrão secundário, é necessária uma comparação com outra substância, denominada de padrão de referência primário. No caso do ácido perclórico, o padrão primário utilizado foi o biftalato de potássio. Para que uma substância seja considerada padrão primário deve apresentar, dentre outras, a seguinte característica:
*KLOTH, Paula Caroline; HENKE, Aline Tavares; GABRIEL, Maria Madalena; WAGNER, Ricardo. Preparo de padrão secundário para identificação de cloridrato de tramadol. Revista Visão Acadêmica, v. 19, n. 2, p. 44-54, 2018.
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
Observação: Caso necessário, utilize a Tabela Periódica.
Soluções aquosas contendo íons cromato (amarela) e dicromato (alaranjada) são utilizadas em um experimento clássico de laboratório, que é realizado para demonstrar a existência do equilíbrio químico e o Princípio de Le Chatelier. Esse equilíbrio químico é representado pela seguinte equação:
!$ 2CrO_{4(aq)}^-+2H_{\ \ \ (aq)}^+\ ⇌\ Cr_2O_{7(aq)}^-+H_2O_{(I)} !$
A adição de solução de hidróxido de sódio em um sistema aquoso contendo íons cromato e dicromato em equilíbrio resultará na seguinte observação:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
Na neutralização de 20 mL de uma solução aquosa de ácido sulfúrico, !$ H_2SO_{4(aq)} !$, com concentração de 0,2 molL-1 , foi consumido certo volume de solução aquosa de hidróxido de sódio, NaOH(aq), previamente padronizada e com concentração de 0,5 molL-1 . Sabendo-se que a equação química, não balanceada, que representa a reação entre o ácido sulfúrico e o hidróxido de sódio, é apresentada a seguir, qual o volume, em mL, consumido da solução aquosa de NaOH?
!$ NaOH_{(aq)}+H_2SO_{4(aq)}→Na_2SO_{4(aq)}+H_2O_{(l)} !$
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O ácido etanoico ou ácido acético !$ \left(H_3CCOOH\right) !$ é obtido pela oxidação do etanol, na presença da bactéria Acetobacter aceti. Ele é comumente utilizado na preparação de perfumes, corantes, seda artificial, acetona e vinagre. Dessa forma, qual o volume aproximado de ácido etanoico que é necessário medir para preparar 500 mL de uma solução aquosa de ácido etanoico, com concentração de 0,600 molL-1 ?
Dados: densidade do ácido etanoico = 1,05 gcm-3 ; massa molar do ácido etanoico = 60,0 gmol-1 .
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O picnômetro é uma vidraria de laboratório de química usada para a determinação de:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
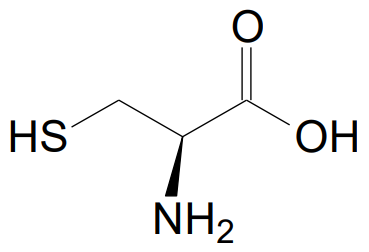
A cisteína é um aminoácido que contém o elemento químico enxofre em sua composição, e que é encontrado na β-queratina, a principal proteína das unhas, das peles e do cabelo.
Considerando a fórmula estrutural da cisteína apresentada, os valores da massa atômica do elemento químico enxofre e da massa molar da cisteína são, respectivamente:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O hipoclorito de sódio (NaClO) possui propriedades bactericida e alvejante, fazendo com que seja utilizado no processo de cloração de águas de piscinas. Ele é produzido pela reação do gás cloro !$ \left(Cl_2\right) !$ com hidróxido de sódio (NaOH), como mostra a equação a seguir.
!$ Cl_{2(g)}+2NaOH_{(aq)}→NaCl_{(aq)}+NaClO_{(aq)}+H_2O_{(l)} !$
Em um processo de produção do hipoclorito de sódio, reagiram 5 kg de hidróxido de sódio com uma quantidade suficiente de gás cloro e foram obtidos 3,72 kg do hipoclorito de sódio. Nesse processo, o rendimento aproximado foi de
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A pilha de iodo-lítio surgiu em 1967, nos Estados Unidos, e passou a ser utilizada como fonte de energia para aparelhos de marca-passo cardíaco, pois é capaz de funcionar continuamente por até dez anos. Ela é constituída, basicamente de lítio e iodo e pode ser representada por meio das semirreações 1 e 2, a seguir.
Semirreação 1: !$ Li_{(s)}→Li_{\ \ \ \ (aq)}^++1e^-\ Eº=+3,045V !$
Semirreação 2: !$ I_{2(s)}+2e^-→2I_{(aq)}^-\ Eº=+0,54V !$
Com base nos dados acima, tem-se o seguinte:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A análise elementar por combustão do glicerol, !$ C_3H_8O_3 !$, indicou a presença de 8,90 g de carbono. A massa da amostra de glicerol analisada é
Provas
Caderno Container