Foram encontradas 36.174 questões.
Observação: Caso necessário, utilize a Tabela Periódica.
A análise gravimétrica de cátions prata pode ser realizada por meio da precipitação desses cátions na forma de cloreto de prata. Se 215 mg de cloreto de magnésio forem adicionados em uma solução contendo nitrato de prata, sob agitação, a quantidade máxima de cloreto de prata que pode ser formada é
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
A epinefrina, ou adrenalina, tem fórmula molecular !$ C_9H_{13}NO_3 !$. A composição percentual em massa da epinefrina é
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
Ao se preparar uma solução aquosa de ácido clorídrico 0,100 molL-1 a partir da solução aquosa de ácido clorídrico concentrado, com teor de 37,5% em massa, deve-se considerar os seguintes procedimentos de segurança:
Provas
Observação: Caso necessário, utilize a Tabela Periódica.
O acetoaminofenol, também conhecido como paracetamol, é um fármaco usado como analgésico e antipirético, cuja fórmula estrutural é apresentada a seguir.
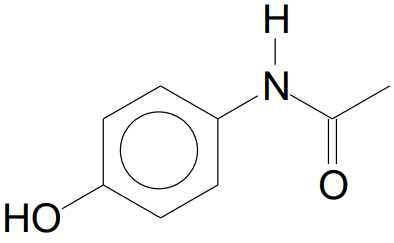
A fórmula molecular do acetoaminofenol é
Provas
Durante a pandemia do novo Coronavírus, o álcool foi amplamente utilizado na higienização da pele, superfícies e objetos. O álcool na concentração de 70% foi o mais utilizado, pois
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
O conceito de solubilidade ou coeficiente de solubilidade pode ser definido como a capacidade limite de dissolução de uma determinada substância (soluto) em outra (solvente) com a qual se misture de forma homogênea. A solubilidade de uma substância está diretamente ligada à quantidade de solvente disponível e à temperatura do sistema. A curva de solubilidade de um sal hipotético pode ser apresentada como mostrado na Figura 1.
Figura 1: Curva de solubilidade de um sal hipotético em água
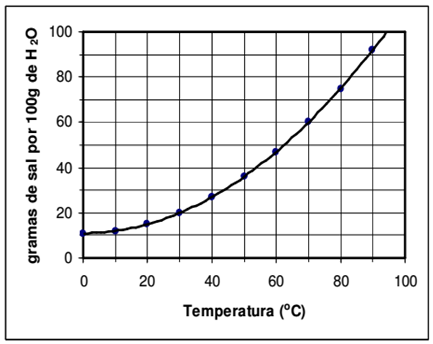
Disponível em: https://obqa.ufba.br Acesso em: 27 jan. 2022.
Considerando que, a 70°C, foram misturados 80g deste sal com 100 g de água, quando for atingido o equilíbrio
Provas
A estequiometria é a área da química que relaciona as quantidades de reagentes e produtos envolvidos em uma operação química e se baseia no princípio de que a soma das massas das substâncias reagentes em um recipiente fechado é igual à soma das massas dos produtos dessa reação.
Para se representar uma reação química, essa área utiliza equações, fórmulas, coeficientes estequiométricos adequados, além de relações intrínsecas a esse tema. Os cálculos estequiométricos podem relacionar as substâncias em quantidade de matéria (ou mol), número de partículas (moléculas, íons, átomos), massa ou volume, por exemplo.
Considere que de um determinado cilindro contendo 6,4 kg de gás metano foram removidas 18,06.1023 moléculas desse gás. Verifica se que (Dados: C = 12 g.mol-1; H = 1 g.mol-1):
Provas
"Houston, we have a problem!" Ao enviar a célebre mensagem em 13 de abril de 1970, o comandante da missão espacial Apollo 13, Jim Lovell, sabia que a sua vida e as dos seus dois companheiros estavam em risco já que um dos tanques de oxigênio (O2) da nave tinha acabado de explodir. Mesmo com o perigo iminente de os astronautas ficarem sem O2 para respirar, outra grande preocupação da NASA, a Agência Espacial responsável pela missão, era evitar que a atmosfera da espaçonave ficasse saturada com o gás carbônico (CO2) exalado pela equipe. Essa saturação poderia causar uma diminuição do pH do sangue da tripulação (chamada de acidemia sanguínea), já que o CO2 é um óxido ácido, que forma ácido carbônico quando em contato com água (CO2(g) + H2O(l) !$ arr !$ H2CO3(g)). Essa situação deveria ser evitada a qualquer custo, uma vez que ela, inicialmente, causa desorientações e desmaios, podendo evoluir até o coma ou mesmo a morte.
Normalmente, a presença de CO2 na atmosfera de uma espaçonave não é um problema. Para eliminá-lo, adaptados à ventilação, existem recipientes contendo hidróxido de lítio (LiOH), que é uma base capaz de absorver esse gás. Quimicamente falando, esse é um processo simples e lógico: remoção de um óxido ácido (CO2) da atmosfera da espaçonave através da reação com uma base (CO2(g) + 2 LiOH(s) !$ arr !$ Li2CO3(s) + H2O(l)). O problema, nesse caso, foi que os três astronautas tiveram de se refugiar numa parte da espaçonave chamada módulo lunar, que é pequena e preparada para duas pessoas. Depois de um dia e meio neste local, uma luz de alerta acendeu: o CO2 havia atingido um nível crítico, já que a quantidade de LiOH, calculada para dois astronautas, estava chegando ao final. Uma atitude improvisada, utilizando o LiOH do módulo de comando (outra área da espaçonave), salvou a vida de toda a tripulação.
PEREIRA, Luís Fernando. Química: Hidróxido de lítio salva astronautas. In: Folha de S.Paulo Folha Online Educação. São Paulo, 29 mai. 2003. Disponível em: https://www1.folha.uol.com.br/folha/educacao/ult305u12947.shtml. Acesso em: 27 jan. 2022. (Adaptado).
Uma alternativa com o mesmo efeito do LiOH seria a utilização de óxido de cálcio (CaO) para a remoção do CO2 emitido pela tripulação. De forma análoga à apresentada acima, o CaO pode reagir com o CO2 para formar o carbonato do metal alcalino terroso em questão.
Considerando os seguintes dados (C = 12 g.mol-1; Ca = 40 g.mol-1; O = 16 g.mol-1) e supondo, portanto, o uso do óxido de cálcio para a remoção do CO2 da atmosfera da espaçonave em questão, constata se que:
Provas
Por ser uma função de estado, a entalpia e, portanto, o valor de ΔH, independe do caminho entre os estados inicial e final. A variação de entalpia para um processo físico pode ser a soma das variações de dois ou mais processos separados. Do mesmo modo, a entalpia total de uma reação pode ser obtida pela soma das entalpias de reação dos passos em que a reação pode ser dividida. A entalpia da reação de hidrogenação do etino (C2H2(g) + 2 H2(g) !$ arr !$ C2H6(g)) pode ser obtida a partir da entalpia de combustão do etino -1300 kJ.mol-1, da entalpia de combustão do etano -1560 kJ.mol-1 e da entalpia de combustão do hidrogênio -286 kJ.mol-1.
Considerando as entalpias de combustão mencionadas acima, o valor para a entalpia da reação de hidrogenação do etino é:
Provas
Uma das primeiras etapas de uma análise química é a preparação da amostra a ser analisada. Tal preparação depende das características iniciais da amostra, como tamanho, pureza, umidade, dentre outras.
Amostras de sólidos de laboratório podem conter água que está em equilíbrio com a atmosfera. A presença dessas moléculas pode interferir na composição da amostra, a depender da umidade relativa do ar e da temperatura ambiente no momento da análise. Uma forma de driblar essa variabilidade na composição é a remoção da umidade dessas amostras sólidas a partir de processos de secagem, como aquecimento da amostra em estufa convencional ou a vácuo.
A água contida em sólidos pode se apresentar de duas formas: a) água essencial e b) água não essencial. Sobre esses dois tipos de “água” que podem estar presentes em sólidos, verifica se que:
Provas
Caderno Container