Foram encontradas 35.936 questões.
Uma das propriedades mais importantes da água é a sua capacidade de dissolver grande variedade de substâncias. Muitas
das reações químicas que acontecem no organismo do homem ou ao seu redor ocorrem devido às substâncias dissolvidas na
água. Considere que o técnico em química recebeu a tarefa de realizar alguns experimentos, ou seja, realizar algumas reações
químicas e anotar as observações diante de cada reação, observe:
1. Reação de uma solução de ácido clorídrico (HCl) com raspas de zinco.
2. Reação entre as soluções de carbonato de sódio (Na2CO3) e ácido bromídrico (HBr).
3. Reação entre as soluções de nitrato de prata (AgNO3) e cloreto de potássio (KCl). Sobre as observações anotadas, analise as afirmativas a seguir.
I. Na reação entre uma solução de ácido clorídrico com raspas de zinco ocorreu desprendimento de gás.
II. Na reação entre o carbonato de sódio e uma solução de ácido bromídrico ocorreu desprendimento de gás.
III. Na reação entre uma solução de nitrato de prata com uma solução de cloreto de potássio se formaram dois sais insolúveis.
Está correto o que se afirma em
1. Reação de uma solução de ácido clorídrico (HCl) com raspas de zinco.
2. Reação entre as soluções de carbonato de sódio (Na2CO3) e ácido bromídrico (HBr).
3. Reação entre as soluções de nitrato de prata (AgNO3) e cloreto de potássio (KCl). Sobre as observações anotadas, analise as afirmativas a seguir.
I. Na reação entre uma solução de ácido clorídrico com raspas de zinco ocorreu desprendimento de gás.
II. Na reação entre o carbonato de sódio e uma solução de ácido bromídrico ocorreu desprendimento de gás.
III. Na reação entre uma solução de nitrato de prata com uma solução de cloreto de potássio se formaram dois sais insolúveis.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A coleta de amostras de água se constitui em um dos elementos fundamentais no desenvolvimento de um programa de
controle da qualidade da água. Embora considerada uma atividade simples, alguns critérios técnicos, como a exigência de
pessoal treinado, devem ser rigorosamente observados no processo de amostragem, a fim de que as amostras sejam representativas do nível de qualidade que se pretende determinar. Sobre a coleta de amostras de água, marque V para as afirmativas verdadeiras e F para as falsas.
( ) A coleta de água tratada deve ser realizada diretamente da torneira, fazendo-se a desinfecção com hipoclorito de sódio a 10%.
( ) As amostras destinadas às análises físico-químicas devem ser acondicionadas em frascos de vidro neutro, devidamente limpos e secos; e identificadas, a fim de se evitar erros.
( ) As amostras coletadas para análise bacteriológica devem ser transportadas em caixas térmicas, em temperatura em torno de 25°C e o período de transporte deve ser de oito horas, sendo que o tempo para a realização das análises não deve exceder vinte e quatro horas.
( ) A coleta de água bruta deve ser realizada em ponto estratégico do manancial de captação ou, quando não é possível, na chegada da água bruta na Estação de Tratamento de Água (ETA).
A sequência está correta em
( ) A coleta de água tratada deve ser realizada diretamente da torneira, fazendo-se a desinfecção com hipoclorito de sódio a 10%.
( ) As amostras destinadas às análises físico-químicas devem ser acondicionadas em frascos de vidro neutro, devidamente limpos e secos; e identificadas, a fim de se evitar erros.
( ) As amostras coletadas para análise bacteriológica devem ser transportadas em caixas térmicas, em temperatura em torno de 25°C e o período de transporte deve ser de oito horas, sendo que o tempo para a realização das análises não deve exceder vinte e quatro horas.
( ) A coleta de água bruta deve ser realizada em ponto estratégico do manancial de captação ou, quando não é possível, na chegada da água bruta na Estação de Tratamento de Água (ETA).
A sequência está correta em
Provas
Questão presente nas seguintes provas
Para um determinado experimento, o técnico em química deverá preparar 100 mL de solução de sacarose 0,02 mol/L seguindo
os seguintes procedimentos:
• Determinar a massa de sacarose a ser pesada;
• Pesar a quantidade calculada em um béquer de 50 mL;
• Adicionar, aproximadamente, 20 mL de água destilada ao béquer contendo a sacarose e dissolver o sólido com o auxílio de um bastão de vidro;
• Transferir essa solução para um balão volumétrico de 100 mL “quantitativamente”;
• Efetuar, pelo menos, 3 lavagens do béquer e do bastão de vidro com, no máximo, 20 mL de água destilada em cada lavagem, transferindo sempre para o balão volumétrico;
• Completar o volume do balão volumétrico com água destilada até o traço de aferição; e
• Agitar o balão volumétrico para homogeneizar a solução.
(Dados: MM sacarose: 342 g/mol.)
Qual a massa de sacarose a ser pesada para o preparo da solução?
• Determinar a massa de sacarose a ser pesada;
• Pesar a quantidade calculada em um béquer de 50 mL;
• Adicionar, aproximadamente, 20 mL de água destilada ao béquer contendo a sacarose e dissolver o sólido com o auxílio de um bastão de vidro;
• Transferir essa solução para um balão volumétrico de 100 mL “quantitativamente”;
• Efetuar, pelo menos, 3 lavagens do béquer e do bastão de vidro com, no máximo, 20 mL de água destilada em cada lavagem, transferindo sempre para o balão volumétrico;
• Completar o volume do balão volumétrico com água destilada até o traço de aferição; e
• Agitar o balão volumétrico para homogeneizar a solução.
(Dados: MM sacarose: 342 g/mol.)
Qual a massa de sacarose a ser pesada para o preparo da solução?
Provas
Questão presente nas seguintes provas
O técnico em química precisa determinar a concentração de cálcio em uma amostra de 200 mL de uma água natural. Para tal
análise, ele utilizou o método da gravimetria por precipitação seguindo os seguintes passos:
1. Adicionou a solução contendo amostra excesso de ácido oxálico;
2. Adicionou, também, amônia para neutralizar o ácido e provocar a precipitação completa do cálcio;
3. O precipitado formado foi filtrado, utilizando um cadinho de filtração que ele encontrou sobre a bancada do laboratório;
4.O precipitado filtrado foi seco e calcinado; e
5. Após o resfriamento, o precipitado juntamente ao cadinho de filtração foi pesado e a massa de óxido de cálcio encontrada.
Após seguir cada passo para determinar a concentração de cálcio em determinada amostra, o técnico em química cometeu quantos erros?
1. Adicionou a solução contendo amostra excesso de ácido oxálico;
2. Adicionou, também, amônia para neutralizar o ácido e provocar a precipitação completa do cálcio;
3. O precipitado formado foi filtrado, utilizando um cadinho de filtração que ele encontrou sobre a bancada do laboratório;
4.O precipitado filtrado foi seco e calcinado; e
5. Após o resfriamento, o precipitado juntamente ao cadinho de filtração foi pesado e a massa de óxido de cálcio encontrada.
Após seguir cada passo para determinar a concentração de cálcio em determinada amostra, o técnico em química cometeu quantos erros?
Provas
Questão presente nas seguintes provas
Para avaliar a qualidade da água para consumo humano, um dos parâmetros monitorados é o teor de cloreto. Em um laboratório
de análises, o químico precisava determinar esse teor de cloreto por titulação com uma solução padrão de AgNO3. Para isso, o
profissional prosseguiu com a análise através dos procedimentos descritos a seguir:
1. Com uma pipeta de 50 mL, pipete esse volume de NaCl;
2. Transfira esse volume de NaCl para um erlenmeyer de 50 mL;
3. Titule lentamente com a solução padronizada de AgNO3 0,05 mol/L até que mude a cor de forma permanente; e
4. Anote o volume consumido de AgNO3. (Observação: volume gasto de AgNO3 na titulação: 1 mL.)
A partir da realização de todas as etapas e das observações experimentais, analise as afirmativas a seguir.
I. O teor de cloreto é 0,001 mol/L.
II. A equação da reação envolvida é Cl(aq)- + AgNO3(aq) → AgCl(s) + NO3 - (aq)
III. A quantidade de matéria, em mol, de nitrato de prata presente no volume consumido no processo é 0,05 mol.
Está correto o que se afirma em
1. Com uma pipeta de 50 mL, pipete esse volume de NaCl;
2. Transfira esse volume de NaCl para um erlenmeyer de 50 mL;
3. Titule lentamente com a solução padronizada de AgNO3 0,05 mol/L até que mude a cor de forma permanente; e
4. Anote o volume consumido de AgNO3. (Observação: volume gasto de AgNO3 na titulação: 1 mL.)
A partir da realização de todas as etapas e das observações experimentais, analise as afirmativas a seguir.
I. O teor de cloreto é 0,001 mol/L.
II. A equação da reação envolvida é Cl(aq)- + AgNO3(aq) → AgCl(s) + NO3 - (aq)
III. A quantidade de matéria, em mol, de nitrato de prata presente no volume consumido no processo é 0,05 mol.
Está correto o que se afirma em
Provas
Questão presente nas seguintes provas
A identificação de determinado grupo funcional é feita com o reagente de Jones, que consiste em uma solução de ácido
crômico e ácido sulfúrico. O ácido ascórbico, que é um álcool, é oxidado pelo reagente de Jones, resultando em uma mudança
de sua estrutura química. O teste de Jones com o ácido ascórbico é representado pela equação a seguir; analise-a.
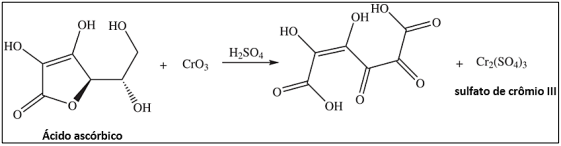
Considerando que uma massa de 200 g de ácido ascórbico (80% de pureza) sofre oxidação, qual a massa, em gramas, de sulfato de crômio III- Cr2(SO4)3 obtido?
(Considere a estequiometria da reação 1:1 / Dados: MM ácido ascórbico = 176 g/mol.)

Considerando que uma massa de 200 g de ácido ascórbico (80% de pureza) sofre oxidação, qual a massa, em gramas, de sulfato de crômio III- Cr2(SO4)3 obtido?
(Considere a estequiometria da reação 1:1 / Dados: MM ácido ascórbico = 176 g/mol.)
Provas
Questão presente nas seguintes provas
O manuseio e a conservação de reagentes químicos
exigem conhecimento sobre suas propriedades e
incompatibilidades para prevenir acidentes. Um técnico
precisa descartar um resíduo de ácido nítrico
concentrado (HNO3) e, separadamente, um resíduo de
acetona (CH3COCH3). Assinale a alternativa que
descreve a prática correta e segura para o manuseio e
descarte desses reagentes.
Provas
Questão presente nas seguintes provas
O modelo atômico atual, baseado na mecânica quântica,
descreve a distribuição dos elétrons em termos de
orbitais e números quânticos, superando as limitações do
modelo de Bohr. A combinação dos quatro números
quânticos define unicamente o estado de um elétron em
um átomo. Com base na distribuição eletrônica do íon Fe
3+(Z=26) em seu estado fundamental, assinale a
alternativa correta.
Provas
Questão presente nas seguintes provas
O gerenciamento de resíduos químicos, incluindo seu
armazenamento temporário e descarte final, é uma etapa
crítica da segurança e da gestão ambiental em um
laboratório. O conhecimento sobre a classificação e a
incompatibilidade química é fundamental. Assim, analise
as afirmativas a seguir.
I.Resíduos de ácidos fortes, como o ácido nítrico, e bases fortes, como o hidróxido de sódio, devem ser armazenados em recipientes separados e nunca misturados diretamente sem um procedimento de neutralização prévio, devido à reação de neutralização ser altamente exotérmica e potencialmente perigosa.
II.Solventes orgânicos halogenados (ex: clorofórmio) e não halogenados (ex: hexano) podem ser descartados no mesmo recipiente de resíduo, pois ambos são inflamáveis e o tratamento por incineração é o mesmo para ambos.
III.Pequenas quantidades de soluções aquosas contendo metais pesados, como sais de chumbo ou mercúrio, podem ser descartadas na pia com água corrente abundante, pois a diluição é um método de tratamento aceito pela legislação para reduzir a toxicidade a níveis seguros.
Está correto o que se afirma em:
I.Resíduos de ácidos fortes, como o ácido nítrico, e bases fortes, como o hidróxido de sódio, devem ser armazenados em recipientes separados e nunca misturados diretamente sem um procedimento de neutralização prévio, devido à reação de neutralização ser altamente exotérmica e potencialmente perigosa.
II.Solventes orgânicos halogenados (ex: clorofórmio) e não halogenados (ex: hexano) podem ser descartados no mesmo recipiente de resíduo, pois ambos são inflamáveis e o tratamento por incineração é o mesmo para ambos.
III.Pequenas quantidades de soluções aquosas contendo metais pesados, como sais de chumbo ou mercúrio, podem ser descartadas na pia com água corrente abundante, pois a diluição é um método de tratamento aceito pela legislação para reduzir a toxicidade a níveis seguros.
Está correto o que se afirma em:
Provas
Questão presente nas seguintes provas
Um Técnico de Laboratório recebe uma amostra de
efluente industrial desconhecido e é incumbido de
realizar uma análise completa. Na primeira etapa, ele
realiza testes de chama e reações de precipitação com
diferentes reagentes para identificar a presença ou
ausência de certos íons metálicos, como Cu2+, Pb2+ e Fe
3+ . Na segunda etapa, após identificar a presença de
cobre, ele utiliza a espectrofotometria de absorção
atômica para determinar a concentração exata de Cu2+
em mg/L. Considerando os princípios da Química
Analítica, as duas etapas do trabalho do técnico
correspondem, respectivamente, a quais tipos de
análise?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container