Foram encontradas 36.142 questões.
Em uma certa reação química, obteve-se como um dos produtos uma substância gasosa. Após análise, foi
comprovado que tinha em sua massa 80% de carbono e 20% de hidrogênio. Verificou-se também que 0,5 L do
gás, nas CNTP, pesava 670 mg. A partir desses valores, considerando a constante dos gases ideais como
sendo R = 0,082 L.atm/K.mol, conclui-se que o valor aproximado da massa molar do gás e sua fórmula
empírica e molecular, respectivamente, são
Provas
Questão presente nas seguintes provas
Considere os dados apresentados a seguir.
CH3CH2CHO(g) + H2 (g) -→ CH3CH2CH2OH(g)
Tabela - Dados das Energias de Ligação Médias para ligações Simples e Múltiplas
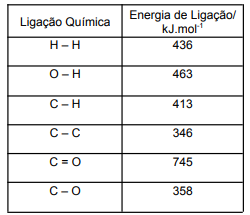
(Fonte: KOTZ, J. C., TREICHEL, P. M., WEAVER, G. C. Química Geral e Reações Químicas, v.1. São Paulo: Cengage Learning, 2010.)
Estima-se que o valor da entalpia para reação de hidrogenação do propanal é:
Provas
Questão presente nas seguintes provas
As reações químicas em um airbag envolvem a decomposição da azida de sódio para gerar o gás nitrogênio, o
qual infla o airbag. A reação principal envolve a azida de sódio, que se decompõe em sódio metálico e
nitrogênio gasoso, conforme a reação (equação 1). À medida que o gás nitrogênio produzido infla o airbag, o
sódio metálico vai sendo neutralizado por outras substâncias, conforme representado pela equação 2 a seguir.
NaN3 (s) → Na(s) + N2 (g) (Equação 1).
Na + KNO3 → K2O + Na2O + N2 (Equação 2).
Após o devido balanceamento das equações, ao se decompor 15 g de NaN3 , e sabendo que todo o sódio metálico formado na equação 1 será consumido na equação 2, a massa de N2 e o seu volume nas Condições Normais de Temperatura e Pressão (CNTP) obtidos, respectivamente, serão
NaN3 (s) → Na(s) + N2 (g) (Equação 1).
Na + KNO3 → K2O + Na2O + N2 (Equação 2).
Após o devido balanceamento das equações, ao se decompor 15 g de NaN3 , e sabendo que todo o sódio metálico formado na equação 1 será consumido na equação 2, a massa de N2 e o seu volume nas Condições Normais de Temperatura e Pressão (CNTP) obtidos, respectivamente, serão
Provas
Questão presente nas seguintes provas
Segundo John C. Kotz em seu livro Química Geral e Reações Químicas, nem todas as reações redox
envolvem o oxigênio, mas todas as reações de oxidação e redução envolvem a transferência de elétrons entre
as substâncias. Estas reações são importantes e têm muitas aplicações no nosso cotidiano, por exemplo, na
obtenção de metais nos processos industriais e em reações nos organismos vivos. Dada a equação a seguir,
SO4
2- (aq) + 2CH2O(aq) + 2H
+
(aq) → H2S(aq) + 2CO2
(g) + 2H2O(l), é correto afirmar que
Provas
Questão presente nas seguintes provas
As propriedades físicas e químicas dos compostos estão ligadas a suas estruturas. Considerando a relevância
de se entender as estruturas de Lewis dos compostos, para que se possa prever a geometria tridimensional
das moléculas e dos íons, e tendo como base o modelo de repulsão dos pares de elétrons da camada de
valência (VSEPR em inglês) e a geometria dos compostos e dos íons, assinale a opção correta.
Provas
Questão presente nas seguintes provas
As funções de onda, obtidas pela resolução da equação de Schrödinger para átomos hidrogenóides são
especificadas por valores de três números, denominados números quânticos, n, l e ml. Sobre estes números
quânticos, conclui-se que o número quântico
Provas
Questão presente nas seguintes provas
As funções inorgânicas - ácidos, base, sais e óxidos - são grupos de compostos químicos que compartilham
propriedades e características semelhantes. Elas são estudadas para entender as propriedades e reações das
substâncias químicas. Considerando esses grupos de compostos inorgânicos e, levando em consideração a
teoria de Arrhenius, é correto afirmar que
Provas
Questão presente nas seguintes provas
A partir do estudo das Propriedades Periódicas, observa-se que as configurações eletrônicas dos átomos estão
relacionadas a algumas das propriedades físicas e químicas dos elementos e que essas propriedades sofrem
modificações ao longo dos grupos e períodos da Tabela Periódica. Levando em consideração a informação
anterior e observando as espécies atômicas A = [Kr] 5s
1 e B = [Kr] 4d
10 5s
2 5p
5
, conclui-se que
Provas
Questão presente nas seguintes provas
Considerando que a criação do modelo atômico de Bohr foi uma resposta direta às limitações dos modelos
anteriores, especialmente ao modelo atômico de Rutherford, a contribuição mais significativa daquele modelo
em relação ao de Rutherford foi que
Provas
Questão presente nas seguintes provas
Um laboratório analisou o extrato aquoso de um solo contaminado, próximo a um lixão, onde foram
descartadas pilhas usadas. Na aplicação da marcha analítica de cátions, observou-se o seguinte:
1. Adição de HCl diluído: formou-se precipitado branco parcialmente solúvel em água quente.
2. Filtrado acidificado + H₂S (meio ácido): formou-se precipitado amarelo.
3. Novo filtrado + NH₄Cl/NH₄OH: não houve precipitado. Em seguida, com a solução amoniacal, borbulhou-se H₂S e formou-se precipitado preto.
De acordo com o exposto, são identificados, respectivamente, em (1), (2) e (3),
1. Adição de HCl diluído: formou-se precipitado branco parcialmente solúvel em água quente.
2. Filtrado acidificado + H₂S (meio ácido): formou-se precipitado amarelo.
3. Novo filtrado + NH₄Cl/NH₄OH: não houve precipitado. Em seguida, com a solução amoniacal, borbulhou-se H₂S e formou-se precipitado preto.
De acordo com o exposto, são identificados, respectivamente, em (1), (2) e (3),
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container