Foram encontradas 358 questões.
A adição de fluoreto à água potável utilizada para abastecimento de cidades é uma ação em benefício da saúde pública.
O esmalte dos dentes é constituído por hidroxiapatita — Ca5(PO4)3OH —, que pode se dissolver caso ocorra a seguinte reação:
Ca5(PO4)3OH (s) \( \rightleftharpoons \) 5 Ca2+ (aq) + 3 PO4 3- (aq) + OH- (aq).
mineralização \( \rightleftharpoons \) desmineralização
A estabilidade da hidroxiapatita é influenciada pelo pH da saliva e pela concentração de íons fluoreto presentes, entre outros fatores. A presença de íons fluoreto interfere no equilíbrio mineralização/desmineralização, pela formação de uma nova substância, a fluorapatita. Esta substância se diferencia da hidroxiapatita pela ausência do grupo OH e presença do átomo de F, o que a torna menos suscetível que a hidroxiapatita ao ataque ácido. A presença de íon fluoreto na água potável modifica o esmalte do dente, que passa a ser formado por uma mistura de hidroxiapatita com fluorapatita.
Considerando as informações acima e que a constante de equilíbrio da reação CaF2 (s) \( \rightleftharpoons \) Ca2+ (aq) + 2 F- (aq), a 25 ºC, seja igual a 4,0 × 10-11, julgue os itens que se seguem.
Considere-se que a água de abastecimento de determinada cidade possua 75 mg/L de carbonato de cálcio. Dessa forma, a companhia de abastecimento dessa cidade pode adicionar flúor à água, na forma de fluoreto, obtendo uma concentração desse íon de 2 × 10-5 mol/L, sem que ocorra a precipitação de CaF2.
Provas
A adição de fluoreto à água potável utilizada para abastecimento de cidades é uma ação em benefício da saúde pública.
O esmalte dos dentes é constituído por hidroxiapatita — Ca5(PO4)3OH —, que pode se dissolver caso ocorra a seguinte reação:
Ca5(PO4)3OH (s) \( \rightleftharpoons \) 5 Ca2+ (aq) + 3 PO4 3- (aq) + OH- (aq).
mineralização \( \rightleftharpoons \) desmineralização
A estabilidade da hidroxiapatita é influenciada pelo pH da saliva e pela concentração de íons fluoreto presentes, entre outros fatores. A presença de íons fluoreto interfere no equilíbrio mineralização/desmineralização, pela formação de uma nova substância, a fluorapatita. Esta substância se diferencia da hidroxiapatita pela ausência do grupo OH e presença do átomo de F, o que a torna menos suscetível que a hidroxiapatita ao ataque ácido. A presença de íon fluoreto na água potável modifica o esmalte do dente, que passa a ser formado por uma mistura de hidroxiapatita com fluorapatita.
Considerando as informações acima e que a constante de equilíbrio da reação CaF2 (s) \( \rightleftharpoons \) Ca2+ (aq) + 2 F- (aq), a 25 ºC, seja igual a 4,0 × 10-11, julgue os itens que se seguem.
A interferência do flúor na mineralização do esmalte dos dentes ocorre unicamente por meio de um processo físico.
Provas
A adição de fluoreto à água potável utilizada para abastecimento de cidades é uma ação em benefício da saúde pública.
O esmalte dos dentes é constituído por hidroxiapatita — Ca5(PO4)3OH —, que pode se dissolver caso ocorra a seguinte reação:
Ca5(PO4)3OH (s) \( \rightleftharpoons \) 5 Ca2+ (aq) + 3 PO4 3- (aq) + OH- (aq).
mineralização \( \rightleftharpoons \) desmineralização
A estabilidade da hidroxiapatita é influenciada pelo pH da saliva e pela concentração de íons fluoreto presentes, entre outros fatores. A presença de íons fluoreto interfere no equilíbrio mineralização/desmineralização, pela formação de uma nova substância, a fluorapatita. Esta substância se diferencia da hidroxiapatita pela ausência do grupo OH e presença do átomo de F, o que a torna menos suscetível que a hidroxiapatita ao ataque ácido. A presença de íon fluoreto na água potável modifica o esmalte do dente, que passa a ser formado por uma mistura de hidroxiapatita com fluorapatita.
Considerando as informações acima e que a constante de equilíbrio da reação CaF2 (s) \( \rightleftharpoons \) Ca2+ (aq) + 2 F- (aq), a 25 ºC, seja igual a 4,0 × 10-11, julgue os itens que se seguem.
O esmalte do dente modificado pela presença de fluoreto é formado por Ca5(PO4)3OH e Ca5(PO4)3F.
Provas
A adição de fluoreto à água potável utilizada para abastecimento de cidades é uma ação em benefício da saúde pública.
O esmalte dos dentes é constituído por hidroxiapatita — Ca5(PO4)3OH —, que pode se dissolver caso ocorra a seguinte reação:
Ca5(PO4)3OH (s) \( \rightleftharpoons \) 5 Ca2+ (aq) + 3 PO4 3- (aq) + OH- (aq).
mineralização \( \rightleftharpoons \) desmineralização
A estabilidade da hidroxiapatita é influenciada pelo pH da saliva e pela concentração de íons fluoreto presentes, entre outros fatores. A presença de íons fluoreto interfere no equilíbrio mineralização/desmineralização, pela formação de uma nova substância, a fluorapatita. Esta substância se diferencia da hidroxiapatita pela ausência do grupo OH e presença do átomo de F, o que a torna menos suscetível que a hidroxiapatita ao ataque ácido. A presença de íon fluoreto na água potável modifica o esmalte do dente, que passa a ser formado por uma mistura de hidroxiapatita com fluorapatita.
Considerando as informações acima e que a constante de equilíbrio da reação CaF2 (s) \( \rightleftharpoons \) Ca2+ (aq) + 2 F- (aq), a 25 ºC, seja igual a 4,0 × 10-11, julgue os itens que se seguem.
Alimentos ácidos provocam a desmineralização do esmalte dos dentes.
Provas
O declínio da mortalidade infantil na Inglaterra, na segunda metade do século XIX, foi atribuído ao simples e eficaz poder de limpar da água com sabão. A partir da Revolução Industrial, no fim do século XVIII, as pessoas passaram a migrar para as cidades em busca de trabalho nas fábricas. Condições miseráveis acompanharam o rápido crescimento da população urbana. Os moradores da cidade não tinham uma fonte de gordura para a produção de sabão. O combustível dos pobres urbanos era a hulha, cuja produção de cinzas não era uma boa fonte de álcali, necessário para saponificar a gordura. Assim, o sabão não poderia ser feito em casa. Era preciso comprá-lo, a preço inacessível para os operários. Os padrões de higiene caíram e a imundície das moradias contribuiu para alta taxa de mortalidade infantil.
Considerando o texto acima, julgue os próximos itens.
Se uma solução de NaOH, utilizada como fonte de álcali para produção de sabão, apresentar fração em massa de 50% e densidade, a 15 ºC, de 1,5 g/mL, então, sua concentração em quantidade de matéria será, nessa temperatura, superior a 18 mol/L.
Provas
O declínio da mortalidade infantil na Inglaterra, na segunda metade do século XIX, foi atribuído ao simples e eficaz poder de limpar da água com sabão. A partir da Revolução Industrial, no fim do século XVIII, as pessoas passaram a migrar para as cidades em busca de trabalho nas fábricas. Condições miseráveis acompanharam o rápido crescimento da população urbana. Os moradores da cidade não tinham uma fonte de gordura para a produção de sabão. O combustível dos pobres urbanos era a hulha, cuja produção de cinzas não era uma boa fonte de álcali, necessário para saponificar a gordura. Assim, o sabão não poderia ser feito em casa. Era preciso comprá-lo, a preço inacessível para os operários. Os padrões de higiene caíram e a imundície das moradias contribuiu para alta taxa de mortalidade infantil.
Considerando o texto acima, julgue os próximos itens.
A equação abaixo representa corretamente uma reação de saponificação.
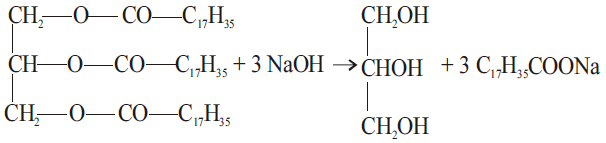
Provas
O declínio da mortalidade infantil na Inglaterra, na segunda metade do século XIX, foi atribuído ao simples e eficaz poder de limpar da água com sabão. A partir da Revolução Industrial, no fim do século XVIII, as pessoas passaram a migrar para as cidades em busca de trabalho nas fábricas. Condições miseráveis acompanharam o rápido crescimento da população urbana. Os moradores da cidade não tinham uma fonte de gordura para a produção de sabão. O combustível dos pobres urbanos era a hulha, cuja produção de cinzas não era uma boa fonte de álcali, necessário para saponificar a gordura. Assim, o sabão não poderia ser feito em casa. Era preciso comprá-lo, a preço inacessível para os operários. Os padrões de higiene caíram e a imundície das moradias contribuiu para alta taxa de mortalidade infantil.
Considerando o texto acima, julgue os próximos itens.
Na limpeza, a ação do sabão é explicada pela formação de uma emulsão coloidal provocada pela presença, em sua constituição, de um grupo apolar, que dissolve as gorduras, e outro polar, que é solúvel em água.
Provas
A água potável de boa qualidade é fundamental para a saúde e o bem-estar humanos. Nos países em desenvolvimento, estima-se que 80% das doenças e mais de um terço das mortes estão associadas à utilização e ao consumo de águas contaminadas. Nos grandes centros urbanos, em que a água é tratada pelas companhias de saneamento básico, pessoas com boas condições econômicas optam por consumir água mineral comercial em vez de água de abastecimento filtrada. As tabelas abaixo mostram alguns dados constantes no rótulo de uma garrafa de água mineral.
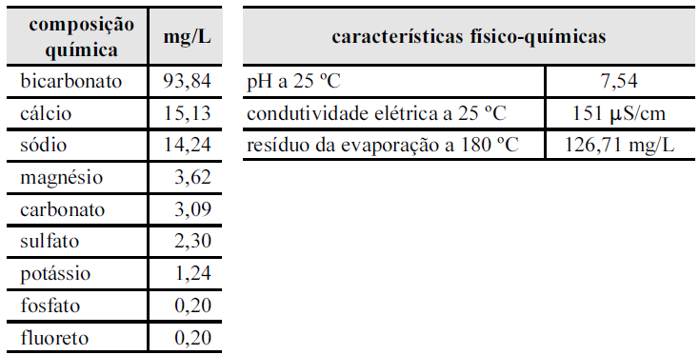
Tendo como referência essas informações, julgue os itens a seguir.
Para uso científico, nos laboratórios, a água deve ser isenta de sais. Nesse caso, para a maioria das aplicações, a decantação é um processo adequado para purificá-la.
Provas
A água potável de boa qualidade é fundamental para a saúde e o bem-estar humanos. Nos países em desenvolvimento, estima-se que 80% das doenças e mais de um terço das mortes estão associadas à utilização e ao consumo de águas contaminadas. Nos grandes centros urbanos, em que a água é tratada pelas companhias de saneamento básico, pessoas com boas condições econômicas optam por consumir água mineral comercial em vez de água de abastecimento filtrada. As tabelas abaixo mostram alguns dados constantes no rótulo de uma garrafa de água mineral.

Tendo como referência essas informações, julgue os itens a seguir.
A água mineral referida no texto, à pressão de 1 atm, atingirá o ponto de ebulição a uma temperatura superior a 100 ºC.
Provas
A água potável de boa qualidade é fundamental para a saúde e o bem-estar humanos. Nos países em desenvolvimento, estima-se que 80% das doenças e mais de um terço das mortes estão associadas à utilização e ao consumo de águas contaminadas. Nos grandes centros urbanos, em que a água é tratada pelas companhias de saneamento básico, pessoas com boas condições econômicas optam por consumir água mineral comercial em vez de água de abastecimento filtrada. As tabelas abaixo mostram alguns dados constantes no rótulo de uma garrafa de água mineral.

Tendo como referência essas informações, julgue os itens a seguir.
A condutividade elétrica relaciona-se com a mobilidade dos íons, como portadores de cargas na solução, e depende da concentração desses íons na solução.
Provas
Caderno Container