Foram encontradas 80 questões.
Com base na Lei nº 13.869/2019 (Lei de Abuso de Autoridade), na Lei nº 11.343/2006 (Lei Antidrogas) e na Lei nº 11.340/2006 (Lei “Maria da Penha”), assinale a alternativa correta.
Provas
A respeito do erro, com base no Código Penal, é correto afirmar que:
Provas
Considere que João foi tomou posse no cargo de perito oficial. Apesar de ter se dedicado por longos anos para ser aprovado no concurso público, como houve um lapso temporal considerável entre a sua aprovação e a nomeação, está inseguro quanto a alguns aspectos práticos relacionados à ordenação que o Código de Processo Penal estabelece para a realização de exames de corpo e delito e perícias em geral, motivo pelo qual convida o seu colega de trabalho, Mário, para tomar um café. Mário ocupa o cargo há vinte anos e é notoriamente reconhecido por seus colegas como um profundo conhecedor dos detalhes técnicos do assunto.
Com base nessa situação hipotética, Mário poderá explicar, de forma correta, a João que
Provas
TABELA PERIÓDICA
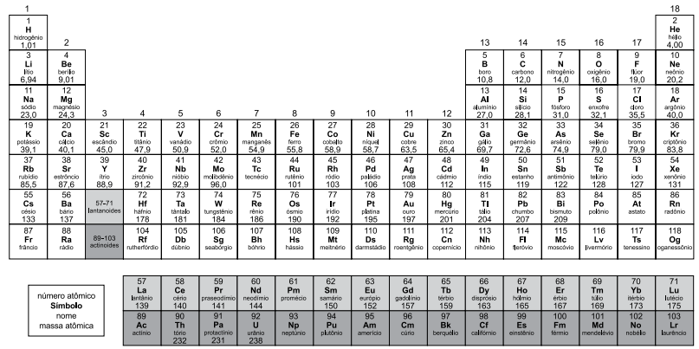
Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
O composto orgânico de fórmula molecular C12H14O4 é produzido industrialmente a partir da reação representada na equação a seguir.
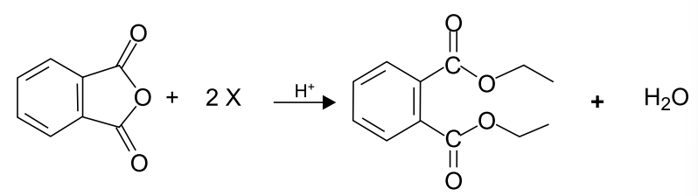
!$ 2\quad X \quad \overset{H^+}{\overrightarrow{calor}}\quad Y+H_2O !$
O composto Y resultante dessa reação é um
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
Uma reação química nas condições padrão é representada pela equação termoquímica genérica:
!$ A(s)→B(s)+C(g) !$ !$ ∆H^o>0 !$
Essa reação
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
Os compostos representados pelas fórmulas unitárias LiF, CsI, A!$ l !$N e CaO apresentam estrutura cristalina cúbica de face centrada.
Entre esses compostos, o que apresenta o menor valor de energia reticular e o que apresenta o maior valor de energia reticular são, respectivamente,
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
A reação do composto As2 S5 sólido com uma solução concentrada de HNO3 resulta na formação do gás NO2 , de água e dos íons SO42– e AsO43– em solução.
Nessa reação, a participação de 1 mol de As2S5 resulta na formação de de moléculas de água e envolve a participação de de elétrons.
As lacunas são preenchidas, correta e respectivamente, por
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
Para a determinação da concentração de uma solução de ácido sulfúrico, foi transferida com uma pipeta volumétrica uma alíquota de 20 mL dessa solução para um erlenmeyer. Nessa alíquota de solução foram adicionados 100 mL de água destilada e 4 gotas de solução do indicador fenolftaleína.
Foi realizada a titulação da solução contida no erlenmeyer, usando-se uma solução de hidróxido de sódio com concentração 0,110 mol/L. O volume do titulante empregado nessa titulação foi igual a 20,2 mL.
A concentração da solução de ácido sulfúrico correspondeu a
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
A reação representada pela equação a seguir ocorre em uma única etapa estabelecendo-se equilíbrio entre reagente (R) e produto (P).
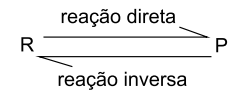
A energia da reação direta é igual a – 100kJ/mol e a energia de ativação da reação direta é igual a 140 kJ/mol. Com a adição de um catalisador, a energia de ativação da reação direta diminui 60 kJ/mol, fazendo com que a energia de ativação da reação inversa seja igual a
Provas
TABELA PERIÓDICA

Notas: Os valores de massas atômicas estão apresentados com três algarismos significativos. Não foram atribuídos valores às massas atômicas de elementos artificiais ou que tenham abundância pouco significativa na natureza. Informações adaptadas da tabela IUPAC 2016.
O composto H3BO3 (massa molar = 61,6 g/mol) é um sólido branco cristalino que, ao ser solubilizado em água, forma o ácido bórico, um ácido monoprótico, que em dada temperatura apresenta Ka = 5 x 10–10. Nessa condição de temperatura, usando-se um balão volumétrico de 100 mL e água destilada para se preparar uma solução de ácido bórico com pH = 5,0, a massa de H3BO3 que deve ser pesada é igual a
Provas
Caderno Container