Foram encontradas 130 questões.
Assinale a opção que contém a ORDEM CRESCENTE CORRETA do valor das seguintes grandezas:
I. Comprimento de onda do extremo violeta do arco-íris.
II. Comprimento de onda do extremo vermelho do arco-íris.
III. Comprimento da cadeia de carbonos na molécula de acetona no estado gasoso.
IV. Comprimento da ligação química entre o hidrogênio e o oxigênio dentro de uma molécula de água.
Provas
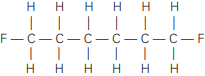
Qual das substâncias a seguir (I a V), nas condições ambiente e sob iluminação branca, terá uma tonalidade mais intensa na sua cor?
I.
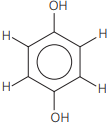
II.
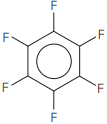
III.
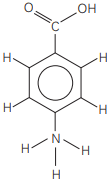
IV.
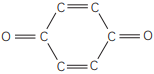
V.
Provas
Qual das opções a seguir é a CORRETA?
Provas
Um átomo de hidrogênio com o elétron inicialmente no estado fundamental é excitado para um estado com número quântico principal (n) igual a 3. Em correlação a este fato qual das opções abaixo é a CORRETA?
Provas
Fazendo-se borbulhar gás cloro através de 1,0 litro de uma solução de hidróxido de sódio, verificou-se ao final do experimento que todo hidróxido de sódio foi consumido, e que na solução resultante foram formados 2,5 mol de cloreto de sódio. Considerando que o volume da solução não foi alterado durante todo o processo, e que na temperatura em questão tenha ocorrido apenas a reação correspondente à seguinte equação química, não balanceada, !$ OH^– (aq) + Cl_2 (g)\rightarrow Cl^– (aq) + ClO^–_3 (aq) + H_2O(l) !$, qual deve ser a concentração inicial do hidróxido de sódio?
Provas
Considere os valores das seguintes variações de entalpia !$ (ΔH) !$ para as reações químicas representadas pelas equações I e II, onde (graf) significa grafite.
I. !$ C(graf) + O_2 (g) \rightarrow CO_2 (g); ΔH(298 K; 1 atm) = – 393 kJ !$
II. !$ CO(g) + 1/2O_2 (g) \rightarrow CO_2 (g); ΔH(298 K; 1 atm) = – 283 kJ !$
Com base nestas informações e considerando que todos !$ ΔH !$ se referem à temperatura e pressão citadas acima, assinale a opção CORRETA:
Provas
Assinale a opção ERRADA dentre as relacionadas a seguir:
Provas
Na figura a seguir, o balão A contém 1 litro de solução aquosa 0,2 mol/L em KBr, enquanto o balão B contém 1 litro de solução aquosa 0,1 mol/L de !$ FeBr_3 !$ . Os dois balões são mantidos na temperatura de 25°C. Após a introdução das soluções aquosas de KBr e de !$ FeBr_3 !$ as torneiras !$ T_A !$ e !$ T_B !$ são fechadas, sendo aberta a seguir a torneira !$ T_C !$ . As seguintes afirmações são feitas a respeito do que será observado após o estabelecimento do equilíbrio.

I. A pressão osmótica das duas soluções será a mesma.
II. A pressão de vapor da água será igual nos dois balões.
III. O nível do líquido no balão A será maior do que o inicial.
IV. A concentração da solução aquosa de !$ FeBr_3 !$ no balão B será maior do que a inicial.
V. A molaridade do KBr na solução do balão A será igual à molaridade do !$ FeBr_3 !$ no balão B.
Qual das opções abaixo contém apenas as afirmações CORRETAS?:
Provas
Qual das opções a seguir contém a equação química CORRETA que representa uma reação que poderá ocorrer com o ouro (Au) nas condições ambientes?
Provas
São feitas as seguintes afirmações a respeito das contribuições do pesquisador francês A. L. Lavoisier (1743- 1794) para o desenvolvimento da ciência:
I) Desenvolvimento de um dos primeiros tipos de calorímetros.
II) Participação na comissão responsável pela criação do sistema métrico de medidas.
III) Proposta de que todos os ácidos deveriam conter pelo menos um átomo de oxigênio.
IV) Escolha do nome oxigênio para o componente do ar atmosférico indispensável para a respiração humana.
V) Comprovação experimental da conservação de massa em transformações químicas realizadas em sistemas fechados.
Qual das opções abaixo contém a(s) afirmação(ções) CORRETA(S)?:
Provas
Caderno Container