Foram encontradas 48 questões.
Dadas as reações,
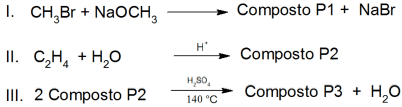
a respeito dos compostos P1, P2 e P3, é correto afirmar que
Provas
O EDTA é um dos agentes de complexação mais importante em química analítica, pois vários elementos da tabela periódica podem ser determinados quantitativamente pelo EDTA. Ele pode ser utilizado como descolorante para cabelos, na fabricação de pães e derivados na indústria alimentícia, durante tratamento endodôntico e como anticoagulante. A figura mostra a estrutura do EDTA.
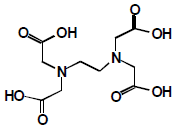
Dadas as afirmativas sobre esse agente complexante,
I. O EDTA pode ser utilizado em volumetria de complexação pelo método de titulação direta.
II. O EDTA pode ser utilizado em volumetria de complexação pelo método de titulação indireta.
III. O EDTA possui as funções orgânicas ácidos carboxílicos e aminas.
IV. O EDTA possui apenas um valor de constante de ionização ácida, Ka.
verifica-se que estão corretas apenas
Provas

Provas
Um ácido de fórmula química genérica representada por H3X, forma uma solução saturada em água através da seguinte reação de equilíbrio:
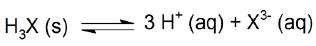
Sabendo que essa solução a 25 ºC apresenta o pH = 3, então o produto de solubilidade (KPS) do ácido H3X a 25 ºC é igual a
Provas
O processo de fermentação dos açúcares presentes no caldo extraído da cana-de-açúcar converte esses açúcares em etanol e baixas concentrações de outros compostos de menor interesse industrial. O principal método de recuperação do etanol formado consiste em submeter essa mistura a um processo de destilação, mas, devido à formação de uma solução azeotrópica, o etanol não pode ser produzido com elevada pureza. O azeótropo formado é uma mistura de etanol contendo, aproximadamente, 4% de água em massa; portanto, a fração molar do etanol nessa solução é:
(Dado: H = 1 g.mol-1, C = 12 g.mol-1, O = 16 g.mol-1).
Provas
A decomposição do peróxido de hidrogênio ocorre de acordo com a equação 2H2O2 → 2H2O + O2↑. Levando em consideração a relação estequiométrica dessa reação, dadas as afirmativas,
(Dado: H = 1 g.mol-1; O = 16 g.mol-1)
I. 2 mols de peróxido de hidrogênio produz 44,8 litros de oxigênio nas CNTP.
II. 68 g de peróxido de hidrogênio produz 32 g de oxigênio.
III. 4 mols de peróxido de hidrogênio produz 1,204 x 1024 moléculas de oxigênio.
IV. 1 mol de peróxido de hidrogênio produz 22,4 litros de oxigênio nas CNTP.
verifica-se que estão corretas apenas
Provas
Uma amostra de água de piscina utilizada para treinos de atletas de natação foi enviada a um laboratório para análise. Uma das medidas a ser avaliada é a do pH, pois o controle de acidez da piscina é essencial para a qualidade da água. Como não tinha disponível no momento um medidor de pH eletrônico, o técnico utilizou uma solução diluída de NaOH 0,002 mol.L-1 para titular 25 mL da amostra de água e obteve como volume médio gasto na titulação 12,5 mL. Em relação ao procedimento, dadas as afirmativas,
I. O NaOH nessa titulação é chamado de titulante.
II. O NaOH nessa titulação é chamado de titulado.
III. A concentração de íons H+ na amostra é 0,001 mol.L-1.
verifica-se que está(ão) correta(s)
Provas
Provas
Um técnico em química é designado para a padronização de uma solução de hidróxido de sódio pelo método volumétrico de titulação ácido-base. Uma alíquota da solução a ser padronizada é transferida para um frasco de Erlenmeyer, na qual são adicionadas gotas de solução indicadora de fenolftaleína, sendo em seguida titulada. Qual das vidrarias é tipicamente utilizada para se determinar com precisão o volume de solução ácida necessária no ponto de equivalência da titulação?
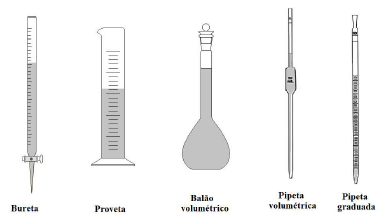
Provas
O ácido fluorídrico (HF) é comercializado, geralmente, como uma solução aquosa a 40% em massa. Esse ácido é produzido pela reação do mineral fluorita (CaF2) com ácido sulfúrico concentrado sob aquecimento, sendo que o HF formado está na forma gasosa e deve ser absorvido em água para formar uma solução aquosa. Qual a massa, em gramas, de solução aquosa de ácido fluorídrico a 40%, que é formada quando 147 gramas de ácido sulfúrico reagem completamente nessa reação?
(Dado: H = 1 g.mol-1, O = 16 g.mol-1, F = 19 g.mol-1, S = 32 g.mol-1, Ca = 40 g.mol-1)
Provas
Caderno Container