Foram encontradas 4.057.604 questões.
Disciplina: Engenharia de Telecomunicações
Banca: CESPE / CEBRASPE
Orgão: UDESC
Um sistema de posicionamento angular de uma antena rastreadora automática é descrito pela função de transferência contínua a seguir.
\(G(s) = \dfrac{s}{(s+2) 5}\)
Esse sistema, que é linear e invariante no tempo, será controlado por um compensador digital implementado em um microcontrolador, utilizando amostragem periódica com frequência de amostragem fs.
A partir do cenário apresentado, julgue os itens a seguir.
Se a frequência fs for menor que o dobro da maior frequência presente no sinal de saída do sistema, poderá ocorrer aliasing, causando distorções irreversíveis na reconstrução do sinal.
Provas
Um sistema de posicionamento angular de uma antena rastreadora automática é descrito pela função de transferência contínua a seguir.
\(G(s) = \dfrac{s}{(s+2) 5}\)
Esse sistema, que é linear e invariante no tempo, será controlado por um compensador digital implementado em um microcontrolador, utilizando amostragem periódica com frequência de amostragem fs.
A partir do cenário apresentado, julgue os itens a seguir.
Para aplicar o critério de Nyquist à função de transferência em malha aberta, basta verificar se o diagrama envolve o ponto crítico (−1,0).
Provas
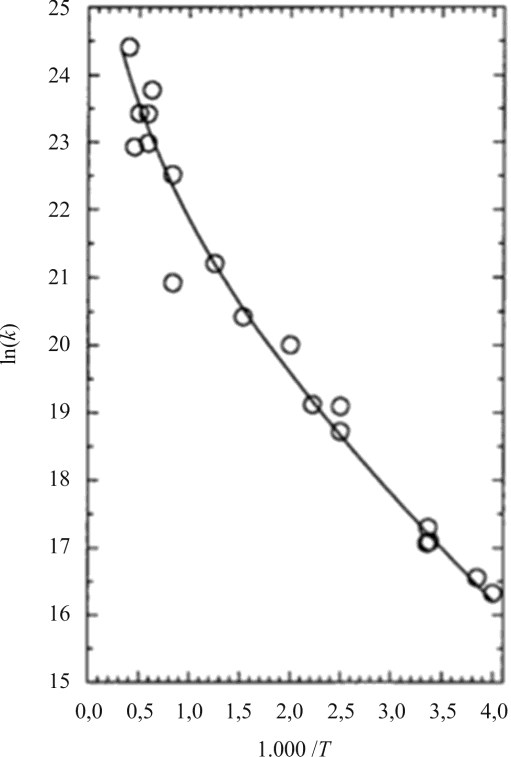
J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Nos resultados experimentais apresentados no gráfico, a constante de velocidade k obedece à lei usual de Arrhenius em toda a faixa de temperaturas do experimento.
Provas

J. Am. Chem. Soc. v. 120, n.º 26, 1968 (com adaptações).
O gráfico anterior diz respeito a um experimento que trata da dependência da constante de velocidade (k) de uma reação química em relação à temperatura absoluta (T) na reação de combustão do formaldeído. A lei usual de Arrhenius estabelece que \(k (T) = Ae^{−E_o/RT}\), em que \(E_o\) representa a energia de ativação constante, \(R\), a constante universal dos gases, e \(A\), o fator pré-exponencial. Mais recentemente, Aquilanti e Mundim generalizaram a teoria de Arrhenius por meio da equação \(k (T) = A\left(1 − d\dfrac{RT}{E_o} \right)^{1/d}\). O gráfico do tipo Arrhenius é uma representação \(ln (k) × \dfrac{1.000}{T}\).
Com base nessas informações e nas leis da cinética química, julgue os itens subsecutivos.
Pela teoria usual de Arrhenius, a energia de ativação de uma reação química é constante, mas, segundo a teoria de Aquilanti-Mundim, ela varia com a temperatura.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
O valor do potencial-padrão da célula eletroquímica em questão é menor que 0,3 V.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
A variação da energia livre de Gibbs-padrão (\( \Delta Gº \)) para a reação em apreço é negativa, com valor inferior a −45 kJ/mol, o que indica que a reação é espontânea nas condições-padrão.
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
A constante de equilíbrio K para a reação em tela é da ordem de 107, o que indica que o equilíbrio é fortemente deslocado para a formação dos produtos (Fe3+ e I−).
Provas
Nas condições-padrão (25 °C, 1 mol/L e 1 bar), a termodinâmica das células galvânicas relaciona a energia livre de Gibbs-padrão (\(ΔGº\)), o potencial-padrão da célula (\(Eº_{cel}\)) e a constante de equilíbrio (K) por \(ΔGº = nFEº_{cel}\) , ou \(ΔGº = −RT\ ln\ K\), em que n representa a quantidade de matéria de elétrons transferidos na reação balanceada, a constante de Faraday é F = 96.500 C/mol, a constante dos gases é R = 8,31 J∙mol−1∙K−1 e a temperatura é T = 298 K.
A tabela a seguir apresenta os potenciais-padrão de redução a 25 °C.

A partir dessas informações, e considerando a convenção da IUPAC e que a reação
2 Fe2+(aq) + I2(s) ⇌ 2 Fe3+(aq) + 2 I−(aq)
ocorra em uma célula eletroquímica, julgue os itens que se seguem.
Considerando-se a reação em comento, se o sistema em equilíbrio for perturbado por um aumento na concentração de I2, o equilíbrio se deslocará para a direita, no sentido de formação de Fe3+ e I−.
Provas
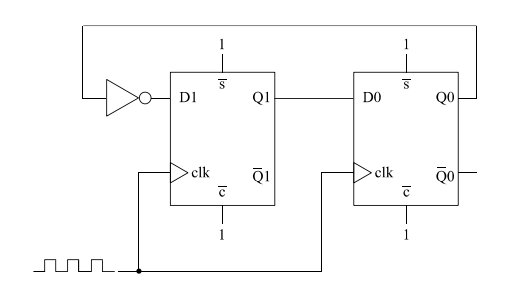
O circuito precedente utiliza dois flip-flops tipo D, ambos acionados por borda de subida do sinal de relógio (clk). Nesse circuito, quaisquer controles assíncronos (PRESET/CLEAR), se existentes, estão configurados de modo a permitir operação contínua. Em relação ao circuito mostrado, julgue o item a seguir.
As informações presentes no circuito permitem inferir que os estados das saídas (Q1, Q0), observados imediatamente após cada borda de subida do relógio, evoluem de forma cíclica, conforme a seguinte a sequência.
00 → 10 → 11 → 01 → 00 → ...
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
A entropia de Boltzmann-Gibbs é definida por SBG = kBlnΩ, em que Ω representa o número de microestados acessíveis de um sistema fechado e kB, uma constante de proporcionalidade. Para sistemas independentes A e B, o número de microestados do sistema combinado fatoriza da seguinte forma: ΩA + B = ΩAΩ B . Em 1988, Tsallis propôs uma generalização, a entropia de Tsallis (Sq), que, para sistemas independentes, satisfaz Sq(A + B) = Sq(A) + Sq(B) + (1 − q) Sq(A)Sq(B), com q real. Com base nessas informações e nas leis da termodinâmica química, julgue os seguintes itens.
Considerando-se a entropia de Tsallis, caso os sistemas A e B sejam colocados em contato, a entropia do sistema final (A + B) não será aditiva, independentemente do valor do parâmetro q.
Provas
Caderno Container