Foram encontradas 37.192 questões.
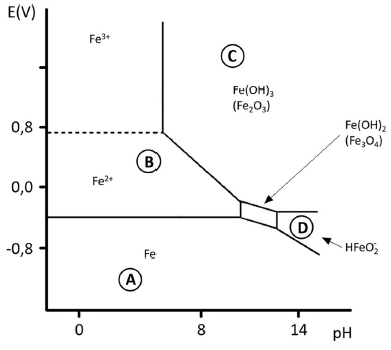
A partir da figura precedente, que apresenta um diagrama de Pourbaix simplificado para o sistema Fe – H2O, julgue o item a seguir.
Um diagrama de Pourbaix representa graficamente as possíveis fases termodinamicamente estáveis de um sistema eletroquímico aquoso, permitindo verificar a tendência de um metal sofrer corrosão nesse meio. Para o diagrama em questão, as letras A, B, C e D representam respectivamente regiões de imunidade, corrosão, passividade e transpassividade.
Provas
Considerando a cinética dos processos corrosivos, julgue o item a seguir.
Em uma pilha de corrosão eletroquímica composta pelo eletrólito e por anodo e catodo feitos de metais diferentes, além da ligação elétrica entre eles, a taxa de corrosão é calculada com base na comparação dos potenciais eletroquímicos dos metais constituintes do anodo e do catodo.
Provas
Com relação aos materiais gasosos e líquidos, julgue o item seguinte.
As partículas dos materiais gasosos apresentam alta velocidade, e os choques entre elas são inelásticos.
Provas
Com relação aos materiais gasosos e líquidos, julgue o item seguinte.
Os materiais gasosos ocupam todo o espaço disponível e têm movimento livre.
Provas
Com relação aos materiais gasosos e líquidos, julgue o item seguinte.
Apenas as partículas de materiais gasosos contêm energia cinética, razão por que se diferenciam das partículas de materiais líquidos.
Provas
Devido ao crescente interesse na exploração e no consumo de petróleo, houve um aumento da contaminação de aquíferos por hidrocarbonetos monoaromáticos, como os BTEX (benzeno, tolueno, etilbenzeno e xileno). O benzeno, por exemplo, é bastante tóxico ao meio ambiente e aos animais, e a Organização Mundial da Saúde (OMS) estabeleceu um limite máximo de 10 !$ \mu !$g/L de benzeno em água de abastecimento público, enquanto, no Brasil, o Ministério da Saúde estabeleceu uma concentração máxima de 5 !$ \mu !$g/L de benzeno em água para consumo.
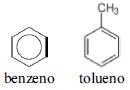
Considerando as informações apresentadas, as fórmulas estruturais do benzeno e do tolueno, mostradas anteriormente, e MH = 1,0 g/mol, MC = 12,0 g/mol e MO = 16,0 g/mol, julgue o item a seguir.
A queima de 46 kg de tolueno, em uma reação de combustão completa, produz mais de 150 kg de gás carbônico.
Provas
Acerca de estequiometria, julgue o item que se segue.
As bases fundamentais da estequiometria são a lei das proporções definidas, a lei das proporções múltiplas e a lei das proporções equivalentes.
Provas
Acerca de estequiometria, julgue o item que se segue.
Em uma reação química, o reagente limitante serve de base para o cálculo do rendimento teórico.
Provas
- Química InorgânicaSubstância e mistura: substância simples, substância composta e mistura. Alotropia
Considerando-se que os óxidos são compostos inorgânicos com diversas aplicações na indústria química, julgue o item subsequente.
A matéria divide-se em substâncias puras, que podem ser homogêneas ou heterogêneas, e misturas, que se subdividem em elementos ou compostos.
Provas
Considerando-se que os óxidos são compostos inorgânicos com diversas aplicações na indústria química, julgue o item subsequente.
Em nomenclatura inorgânica, a terminação ico indica nox menor, e a terminação oso designa nox maior.
Provas
Caderno Container