Foram encontradas 35.936 questões.
A Base Nacional Comum Curricular (BNCC) é um documento de caráter normativo que define o conjunto orgânico e progressivo de aprendizagens essenciais que todos os alunos devem desenvolver ao longo das etapas e modalidades da Educação Básica. Tendo por base a BNCC, analise as afirmações a seguir, sobre o currículo de química no ensino médio.
I. A construção dos currículos de química das escolas brasileiras passa a ser pautada no desenvolvimento de competências, tendo como referência a Base Nacional Curricular Comum.
II. Com a aprovação da BNCC, os conteúdos de química ministrados nas escolas brasileiras passam a ter uniformidade, garantindo que todos os estudantes possam desenvolver o aprendizado de maneira igualitária, independentemente de sua região ou situação econômica.
III. A inserção dos Itinerários Formativos, inclusive da formação técnica e profissional, poderá promover o aprofundamento em qualquer uma das áreas de conhecimento previstas na BNCC, possibilitando o desenvolvimento de conteúdos interdisciplinares.
IV. O núcleo obrigatório da BNCC garante a oferta da disciplina de química nos três anos do ensino médio sem redução de carga horária.
Em relação ao que é previsto na BNCC, estão corretas as afirmativas:
Provas
Identifique os tipos de reações a seguir:
I. CH3-CH2-(CH3)2C-Cl + OH-!$ \rightarrow !$CH3-CH2-(CH3)2C-OH + Cl-
II. CH3-CH2-(CH3)2C-OH + H2SO4 !$ \rightarrow !$CH3-CH=C(CH3)2 + H2O + H2SO4
III. III. CH3-CH2-CH2-Cl + OH- \rightarrow CH3-CH2-CH2-OH + Cl-
IV. CH3-CH2-CH=CH2 + HBr \rightarrow CH3-CH2-CH(Br)-CH3
V. HOOC-(CH2)4-COOH + H2N-(CH2)6-NH2 !$ \rightarrow !$ nH2O + [-NH-(CH2)6-NH-CO-(CH2)4-CO-]n
As reações expostas são, respectivamente:
Provas
Segundo o engenheiro e epistemólogo francês, Jean-Louis Le Moigne, em seus mais distintos significados um modelo pode ser: um desenho, um diagrama, um esboço, uma ilustração, um objeto concreto, uma estrutura matemática (modelo simbólico), um software de computador, uma cópia de alguma coisa (modelo icônico). No sentido epistemológico o modelo pode ser equiparado a qualquer estrutura, seja concreta ou abstrata, que visa de algum modo representar aspectos de uma determinada realidade, fato ou coisa, ou fenômeno, mas sem nunca a alcançar completamente. Sobre as limitações de modelos explicativos, identifique os modelos atômicos nas afirmações abaixo:
I. Não explica as conclusões do experimento de Geiger–Marsden que consiste em um feixe de partículas alfa, normalmente executado em uma folha de ouro muito fina em uma câmara evacuada.
II. Não explica a natureza elétrica da Matéria.
III. Não explica o espectro de raia, formado por elementos multieletrônicos.
IV. Não está em acordo com a teoria do eletromagnetismo, que aponta que toda partícula com carga elétrica submetida a uma aceleração origina a emissão de uma onda eletromagnética. As limitações apresentadas acima são, respectivamente, dos modelos atômicos:
Provas
Uma solução de ácido HX de concentração 0,01mol/L foi colocada para a medição do seu potencial hidrogênio iônico. Sabendo que a constante de ionização do HX é 1,0 x 10-8 (0,00000001), o valor da medida será próximo de:
Provas
Por definição, uma solução tampão resiste a variações no pH decorrentes da diluição ou da adição de ácidos ou bases. Os químicos empregam as soluções tampão para manter o pH de soluções sob níveis predeterminados relativamente constantes.
Um estudante misturou 200mL de solução de ácido HX de concentração 0,1mol/L com 300mL de solução do sal de sódio desse ácido (NaX) que tinha concentração de 0,2mol/L. Sabendo que a constante de ionização do ácido HX é 0,000003. Qual o valor do pH da solução formada?
Provas
Quimicamente, a cloroquina (CQ) e a hidroxicloroquina (HCQ) pertencem à classe das 4-aminoquinodinas. Elas têm estrutura central aromática comum, com um cloro na posição 7, ligada às respectivas cadeias laterais básicas. A forma molecular da cloroquina é: C18H26CIN3, com massa molar de 319,9 g/mol. Já a hidroxicloroquina tem massa molar de 335,9 g/mol
.
A CQ e a HCQ são administradas como difosfato e sulfato, respectivamente, em suas formas racêmicas.
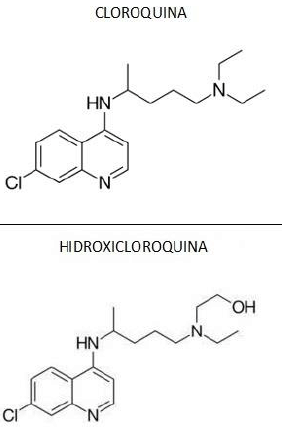
Sobre o medicamento citado acima, marque o que for correto.
Provas
Um mol de uma dada substância é aquecido de 80 °C para 110 °C, sem alterar o seu estado físico. Baseado nos seus conhecimentos de termodinâmica, analise as afirmativas abaixo:
I. A equação !$ \triangle H '= \int_{80}^{110} c_p dT !$ pode ser usada para calcular a variação da entalpia associado ao aquecimento de um mol da substância.
II. Se a substância for um líquido ou sólido, o processo de aquecimento terá praticamente o mesmo gasto energético a volume constante e a pressão constante.
III. Se a substância for um gás ideal, o processo de aquecimento a pressão constante gastará mais energia que o processo de aquecimento a volume constante.
Assinale a alternativa que contém a análise correta.
Provas
O dióxido de nitrogênio (NO2) é uma molécula intermediária na produção industrial de ácido nítrico (HNO3), que é muito aplicado na produção de fertilizantes.
O dióxido de nitrogênio existe em equilíbrio com o tetróxido de nitrogênio (N2O4), segundo a reação:
!$ 2 NO_2(g) \rightleftarrows N_2 O_4(g)\,\,\,\,\,\triangle = -57,23 KJ/mol !$
Para aumentar o rendimento do dióxido de nitrogênio na reação, segundo o princípio de Le Châtelier, deve-se:
Provas
“Na última semana, os consumidores sentiram pesar no bolso o preço do gás de cozinha. O valor médio do botijão de 13 kg subiu de R$ 85,27 para R$ 85,63 entre os dias 6 e 12 de junho. Considerando todo o país, o maior preço do produto foi registrado na região Centro-Oeste, onde consumidores chegaram a pagar R$ 125 por um botijão.”
(Disponível em: https://jovempan.com.br/noticias/
brasil/ gas-de-cozinha-atinge-maior-preco-em-2021-e-deve-ficar-ainda-mais-caro-entenda-o-reajuste-da-petrobras.html. Acessado em 28/09/2021)
Supondo que todo o GLP presente no botijão seja somente butano e está totalmente na forma líquida, e que o preço do botijão de gás seja de R$ 125,00, para uma família que teve um gasto mensal com a fatura de gás de R$ 55,77, qual a quantidade de energia que foi liberada, em quilojoules, na queima do gás butano?
A reação de combustão completa do butano (não balanceada):
C4H10(g)→CO2(g)+H2O !$ \triangle H_C^{ \circ} = 2.808 KJ/ mol !$
Provas
A amônia ou amoníaco é um composto químico que na temperatura ambiente é um gás incolor, tóxico e corrosivo quando há presença de umidade. Esse gás, além de altamente perigoso no caso de inalado, também é inflamável. Muito utilizado na refrigeração e em processos de absorção em combinação com a água, além de seu uso na agricultura e em produtos de limpeza.
A amônia, ao reagir com a água origina os íons amônio e hidroxila, segundo o seguinte equilíbrio químico:
!$ NH_3(g) + H_2O( \ell) \rightleftarrows NH_4^+ (aq) + OH^- (aq) !$
Com relação à amônia e a sua reação com água, analise os seguintes itens:
I. A geometria molecular da amônia é piramidal.
II. A amônia é dita como base de Bronsted-Lowry na reação com a água.
III. NH4+ é a base conjugada da amônia.
Assinale a alternativa que contém a análise correta.
Provas
Caderno Container