Foram encontradas 35.936 questões.
A variação de entalpia, associada à formação de um cristal iônico sólido a partir de seus íons no estado gasoso, é conhecida como energia reticular. Essa energia é difícil de ser medida diretamente, mas pode ser calculada de forma indireta, utilizando-se a Lei de Hess, a partir de outras transformações, cuja variação de entalpia é conhecida. Esse caminho para a determinação da energia reticular é conhecido como ciclo de Born-Haber. O diagrama a seguir mostra as etapas desse ciclo para o cloreto de sódio (!$ NaC\ell !$).
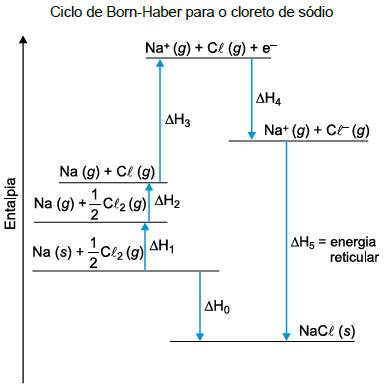
Nesse diagrama, a sublimação do sódio metálico, a primeira energia de ionização do elemento sódio e a afinidade eletrônica do elemento cloro correspondem, respectivamente, aos valores de
Provas
A tabela mostra valores de solubilidades em água, expressas em g de soluto por 100 g de solvente, em duas temperaturas, de dois compostos iônicos empregados como fertilizantes agrícolas.
| Composto | Solubilidade em água (em gsoluto/100 gsolvente) | |
| 25º C | 80º C | |
| (NH4)2SO4 | 76 | 94 |
| !$ KC \ell !$ | 36 | 51 |
Uma mistura foi preparada pela dissolução de 400 g de sulfato de amônio e 400 g de cloreto de potássio em 1 kg de água à temperatura de 80 ºC, originando uma mistura homogênea límpida e insaturada. Ao ser resfriada à temperatura ambiente de 25 ºC, observou-se que a mistura resultante
Provas
O limão “Tahiti”, por não apresentar sementes e ter suco abundante, com elevado teor de ácido cítrico [C3H5O(COOH)3]2, pode ser fonte desse ácido puro obtido no estado sólido. A primeira etapa dessa obtenção consiste na precipitação do ácido cítrico presente no suco do limão, como citrato de cálcio {Ca3[C3H5O(COO)3]2}, por adição de solução aquosa saturada de hidróxido de cálcio [Ca(OH)2] ao suco, conforme a reação:
2C3H5O(COOH)3 (aq) + 3Ca(OH)2 (aq) →
→ {Ca3[C3H5O(COO)3]2} (s) + 6H2O (!$ \ell !$)
Considere que:
– nessa reação foram obtidos 640 g de citrato de cálcio;
– as massas molares do citrato de cálcio e do ácido cítrico são, respectivamente, 498 g/mol e 192 g/mol;
– o rendimento da reação é 100%;
– cada limão “Tahiti” apresenta em média 2,5 g de ácido cítrico.
De acordo com as informações, o número de limões “Tahiti” necessários para obter os 640 g de citrato de cálcio foi próximo de
Provas
O cátion Ba2+ pode apresentar toxicidade aos humanos, dependendo de sua concentração e forma química. Por exemplo, BaSO4 é pouco tóxico, sendo usado como contraste radiológico, por ser insolúvel em solução aquosa, enquanto BaCO3 e Ba(NO3)2 são muito tóxicos, pois liberam Ba2+ no organismo. Em um laboratório foram feitos dois testes de solubilidade para identificar o conteúdo de três frascos não rotulados que poderiam ser de Ba(NO3)2, BaCO3 ou BaSO4. Os resultados dos dois testes de solubilidade são apresentados a seguir.
| Frasco | Teste I: Adição de H2O destilada à temperatura ambiente | Teste II: |
| 1 | Insolúvel, não houve | Insolúvel, não houve |
| 2 | Insolúvel, não houve liberação de gás | Solúvel, houve liberação |
| 3 | Solúvel, não houve liberação de gás | Solúvel, não houve |
Considerando os ensaios realizados, indique quais são os compostos contidos nos frascos 1, 2 e 3, respectivamente.
| Frascos | ||
| 1 | 2 | 3 |
Provas
Para o monitoramento ambiental no entorno de um posto de gasolina, coletou-se uma amostra de solo que foi submetida de forma integral à análise de naftaleno, um composto presente na gasolina. A concentração encontrada foi de 2,0 mg de naftaleno por kg de solo úmido. Sabendo que essa amostra de solo contém 20% de água, qual é o resultado dessa análise por kg de solo seco?
Provas
O hidróxido de alumínio !$ (A\ell (OH)_3) !$, ao precipitar em solução aquosa, forma um sólido gelatinoso que pode ser usado como agente floculante no tratamento de água. Essa precipitação pode ocorrer pela adição de um hidróxido solúvel a uma solução aquosa ácida contendo um sal de alumínio solúvel, como o !$ A\ell C\ell_3 !$. Entretanto, adicionando-se excesso de hidróxido ao meio, há a formação de íons !$ A\ell (OH)_4^- !$, espécie solúvel em água, e o precipitado se solubiliza novamente. Dessa forma, dependendo do pH do meio, uma dentre as espécies !$ A\ell (OH)_4^- (aq) !$, !$ A\ell^{3+} (aq) !$ e !$ A\ell^{3+} (aq) !$ estará presente na solução em quantidade maior que as demais, como exemplificado no esquema.
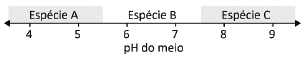
A alternativa que mostra corretamente qual das espécies estará em quantidade maior que as duas outras em cada faixa de pH é:
Provas
Um marcador radioativo (24Na) foi injetado em um ponto de um cano de água subterrâneo e, na sequência, com um detector sobre o solo, foi medida a radioatividade ao longo do percurso do cano. A figura a seguir esquematiza o local de injeção do marcador e o perfil da radioatividade detectada ao longo do cano.
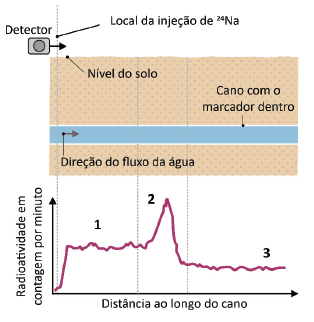
Assinale a alternativa que melhor explica o perfil da radioatividade.
Provas
Cálculos renais, conhecidos popularmente por “pedras nos rins”, consistem principalmente em oxalato de cálcio, CaC2O4, espécie cuja constante de solubilidade (Kps) é de aproximadamente 2 × 10−9. Os íons oxalato, presentes em muitos vegetais, reagem com os íons cálcio para formar oxalato de cálcio, que pode gradualmente se acumular nos rins. Supondo que a concentração de íons cálcio no plasma sanguíneo seja de cerca de 5 × 10−3 mol/L, qual seria a concentração mínima, em mol/L, de íons oxalato para que CaC2O4 precipitasse?
Provas
As reações de hidrólise de ésteres, quando realizadas em meio aquoso, podem ser catalisadas pela adição de ácido, sendo a reação mais lenta em meios próximos da neutralidade.
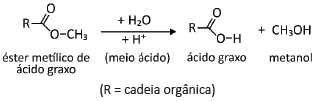
Duas reações idênticas para a hidrólise desse éster foram realizadas nas mesmas condições, variando apenas o pH do meio: uma delas foi conduzida em pH=2 e outra em pH=6. Qual dos seguintes diagramas representa de forma mais adequada a quantidade de ácido graxo formada em função do tempo de reação para as hidrólises em pH=2 e pH=6?
Provas
Oxigênio (O2) e ozônio (O3) estão em constante processo de consumo e produção na estratosfera, como representado pelas equações químicas a seguir. As reações I e II ilustram etapas da produção de ozônio a partir de oxigênio, e a reação III mostra a restauração de oxigênio a partir de ozônio.
| Reação | !$ \Delta H !$ (kcal/mol de O2) | |
| I | O2 → 2O | -118 |
| II | 2O2 + 2O → 2 O3 | !$ \Delta H_{II} !$ |
| III | 2O3 → 3 O2 | +21 |
O !$ \Delta H_{II} !$, relacionado à reação II, pode ser calculado a partir dos dados fornecidos para as reações I e III. O valor de !$ \Delta H_{II} !$, em kcal/mol de O2 consumido, é igual a:
Provas
Caderno Container