Foram encontradas 35.976 questões.
Quando ferro metálico é mergulhado em uma solução de ácido clorídrico, ocorre a seguinte reação:
Fe + 2HC\( \ell \) → FeC\( \ell \)2 + H2 \( \Delta H \) = -88 kJ/mol
Considerando o volume molar dos gases igual a 25 L/mol e que em um experimento realizado à temperatura ambiente foram liberados 7,04 kJ de energia, o volume de gás hidrogênio produzido nesse experimento foi de
Provas
O fenômeno da condutividade elétrica de soluções foi explorado pelo químico Svante August Arrhenius em sua tese de doutorado de 1884, intitulada “Pesquisas sobre a Condutividade Galvânica”. Segundo Arrhenius, para que uma substância seja condutora de eletricidade em meio aquoso, deve ser capaz de se dissolver e liberar ou produzir cargas elétricas. Esse comportamento químico é observado nas substâncias
Provas
O ponto de ebulição das substâncias está relacionado com o tipo de interação existente entre suas moléculas e com a massa molecular. O quadro apresenta substâncias com massas moleculares próximas e suas respectivas fórmulas estruturais.
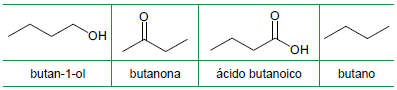
A ordem crescente de temperaturas de ebulição das substâncias apresentadas no quadro é
Provas
Acefato é o nome de um inseticida de fórmula molecular C4H10NO3PS (M = 183 g/mol), indicado para aplicação em culturas de algodão, soja e feijão. A formulação recomendada para uso é de 0,75 a 1 kg dissolvido em 300 a 400 L de água. Assim, a concentração em mol/L da solução mais diluída desse inseticida é igual a
Provas
Os modelos atômicos elaborados ao longo do tempo buscavam explicar fenômenos naturais, alguns dos quais reproduzidos experimentalmente. O modelo proposto por Dalton em 1803, apesar de não explicar muitos dos fenômenos observados na época, contribuiu com a consolidação da
Provas
O ânion fenolato, empregado na produção de corantes, é formado na ionização do fenol em solução aquosa, conforme representado abaixo:
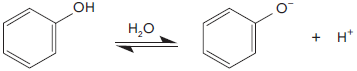
Considere um processamento no qual houve a dissolução completa de 0,01 mol de fenol em água para formar 1 L de solução a 20 °C. Nessa temperatura, a constante de acidez do fenol é igual a 10−10.
Atingido o equilíbrio químico da ionização, a concentração de ânion fenolato, em mol/L, na solução, é aproximadamente igual a:
Provas
O ácido iodídrico, utilizado na higienização de instrumentos médicos, dentre outras aplicações, é produzido a partir da seguinte reação química:
2 I2 + N2H4 → 4 HI + N2
Em um processo de produção industrial, ao adicionar 254 kg de I2 e 80 kg de N2H4, verifica-se o consumo completo do reagente limitante.
A massa de reagente em excesso, que não foi consumida, em quilogramas, tem valor igual a:
Provas
Em um estudo de cinética química, foram realizados os experimentos W, X, Y e Z, nos quais o gás hidrogênio foi obtido a partir da reação química entre níquel e ácido clorídrico, conforme representado abaixo.
Ni(s) + 2HCL (aq) \( \rightarrow \) Nicl2 (aq) + H2 (g)
Em cada experimento, foram alteradas tanto a concentração do ácido clorídrico quanto a temperatura do sistema, mantendo-se a massa de níquel e o volume de solução do ácido constantes. Observe o gráfico:
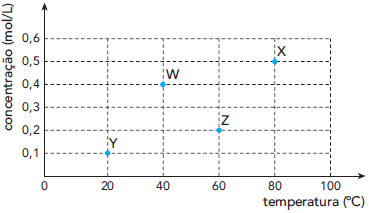
A maior velocidade inicial de formação de gás hidrogênio foi verificada no seguinte experimento:
Provas
O ácido fólico é uma das vitaminas do complexo B. A acidez dessa molécula é determinada pela ionização dos diferentes átomos de hidrogênio em função do pH do meio. Observe sua fórmula estrutural:
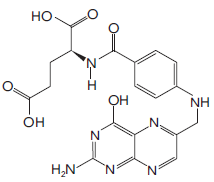
Considere um dado valor de pH, para o qual apenas os hidrogênios das carboxilas do ácido fólico se ionizam.
Nessa situação, a carga do ânion formado é igual a:
Provas
Duas das principais etapas do tratamento de água para abastecimento humano envolvem a filtração e a decantação do material particulado presente na água. Recentemente, devido ao excesso de esgoto doméstico presente no rio Guandu, onde fica a estação de tratamento de água do Rio de Janeiro, foi necessário acrescentar uma etapa complementar de filtração por carvão ativado. Essa nova etapa destina-se à remoção de compostos orgânicos, que afetam o cheiro e o sabor da água e que não são removidos pelo tratamento convencional. Um exemplo desses compostos é a geosmina, que tem a seguinte fórmula estrutural:
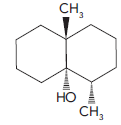
A filtração complementar baseia-se na formação de interações intermoleculares entre a geosmina e o carvão ativado, que é composto basicamente por átomos de carbono.
As interações com o carvão ativado no processo de filtração são decorrentes da presença, na molécula de geosmina, do seguinte segmento de cadeia:
Provas
Caderno Container