Foram encontradas 35.976 questões.
- Química CinéticaTransformações Químicas
- Química InorgânicaSoluções e Substâncias Inorgânicas
- Química InorgânicaReações Inorgânicas
No processo de Claus usado na recuperação de enxofre do gás natural e do petróleo, o sulfeto de hidrogênio reage com dióxido de enxofre, para formar enxofre elementar e água, de acordo com a seguinte equação química:
2 H2S(g) + SO2(g) → 3 S(s) + 2 H2O(l)
A partir da equação precedente, indique a alternativa que apresente o redutor e o oxidante.
Provas
Suponhamos que você tenha uma amostra de 100 mL de água do mar que apresenta uma concentração de NaCl de 0,550 mol/L. Você transfere 10 mL dessa amostra para um balão volumétrico de 100 mL e completa até o traço de aferição com água destilada. Após misturar a amostra diluída, você então transfere 5 mL dessa amostra para outro balão de 100 mL e completa com água destilada. Calcule a concentração, em mol/L de NaCl na amostra final de 100 mL.
Provas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaFunções Oxigenadas: Álcool, Fenol e Enol
- Química OrgânicaFunções Oxigenadas: Cetona, Aldeído, Éter, Éster, Ácido Carboxílico etc.
A estrutura abaixo é o fármaco Doxorrubicina, que é utilizado em um nanofármaco na forma peguilhada para alguns tipos de câncer de ovário. Podemos dizer que, em relação a sua estrutura, as funções orgânicas indicadas pelos números 1, 2, 3 e 4 são, respectivamente,
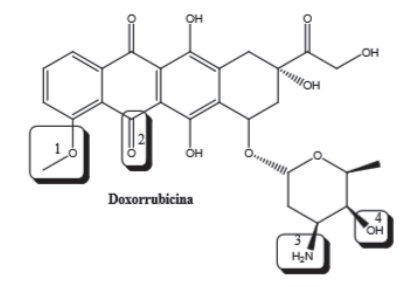
Provas
O superóxido de potássio é utilizado como purificador de ar em ambientes fechados habitáveis, porque esse composto reage com dióxido de carbono e libera oxigênio, de acordo com a seguinte equação química:
4 KO2(s) + 2 CO2(g) → 2 K2CO3(s) + 3 O2(g)
Tendo como referência a reação acima, assinale a alternativa que apresente o volume exato de O2 liberado nas condições normais de temperatura e pressão (CNTP), para a reação de 28,4 g de KO2 (volume molar dos gases (CNTP) = 22,4 L)
Provas
Já foram tentadas várias maneiras de produzir biocombustíveis, com algumas mais bem-sucedidas que outras. Um método que não funcionou é tratar a biomassa bacteriana com soluções aquosas de hipoclorito de sódio (NaClO) para tentar digerir as biomoléculas complexas presentes. Em uma tentativa para pesquisar mais esse processo, uma solução é preparada dissolvendo-se 45,0 g de NaClO em água suficiente para produzir exatamente 750 mL de solução. Assinale a alternativa que indique corretamente o valor da concentração dessa solução em mol/L.
Provas
A matriz de transporte do Brasil está centrada em rodovias, sendo que a principal fonte de energia dos veículos que utilizam esse modal é derivada do petróleo. No entanto, grande parte desse combustível fóssil é constituído por moléculas de cadeias carbônicas muito longas, inviáveis para o uso como combustíveis automotores. As refinarias, assim, contornam esse problema transformando as cadeias longas em moléculas menores pertencentes à fração mais consumida, por meio de um processo químico chamado
Provas
O geraniol é um álcool terpênico insolúvel em água naturalmente encontrado nos óleos essenciais de citronela, gerânio, limão e rosas, entre outras espécies vegetais. Sua molécula contém um grupo funcional álcool, dois carbonos terciários e 18 átomos de hidrogênio.
Considere as estruturas de vários compostos que possuem odores característicos.
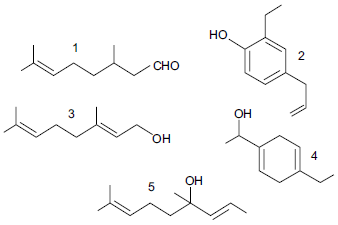
Com base nas informações do texto, o geraniol é representado pela estrutura
Provas
O flúor-18 (18F) é um radioisótopo utilizado em diagnósticos de câncer, com meia-vida igual a 110 minutos, produzido a partir da reação entre núcleos de neônio (20Ne) e o isótopo X, conforme a equação a seguir:
\( ^{20}_{10} Ne + X \rightarrow ^{18}_{9}F+ ^{4}_{2}\alpha \)
O isótopo X e a porcentagem de 18F que resta após 5,5 horas de sua produção são, respectivamente,
Provas
O hipoclorito de sódio (NaC\( \ell \)O) apresenta propriedades bactericidas por promover a oxidação de proteínas, lipídeos e carboidratos existentes nas células bacterianas. A equação mostra a reação entre a glicina e o íon hipoclorito (C\( \ell \)O–).
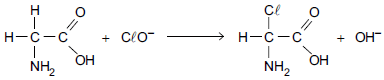
Nessa reação, verifica-se que o átomo de carbono do glicina é pelo íon hipoclorito e o átomo de cloro tem seu número de oxidação alterado de para .
As lacunas do texto são preenchidas, respectivamente, por:
Provas
Segundo a teoria das colisões efetivas, para que uma reação ocorra é necessário que as moléculas dos reagentes colidam umas com as outras com orientação espacial adequada e energia mínima. Assim, qualquer alteração no meio reacional que interfira nesses dois fatores modifica a velocidade da reação. A figura mostra o sistema reacional gasoso 1 submetido a modificações que proporcionaram os sistemas 2 e 3.
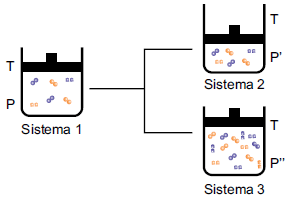
Considerando que as moléculas existentes nesses sistemas reajam entre si, as relações entre as velocidades (V) das reações dos sistemas 1 e 2 e dos sistemas 1 e 3 são, respectivamente,
Provas
Caderno Container