Foram encontradas 35.976 questões.
Os elementos químicos presentes no grupo 2 da tabela periódica são conhecidos como metais alcalino-terrosos.
Nesse grupo, o elemento que apresenta o maior raio atômico tem como símbolo
Provas
No estado fundamental, a distribuição eletrônica dos átomos de enxofre corresponde a
1s2 2s2 2p6 3s2 3p4
O número de elétrons na camada de valência desses átomos corresponde a
Provas
A estrutura espacial do DNA foi descrita inicialmente por Watson e Crik e pode ser imaginada como duas sequências de alfa-hélices próximas, uma a outra, e mantidas juntas a partir de interações químicas ( vide Figura 1).
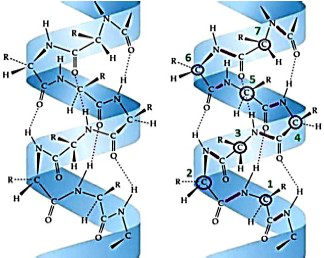
Figura 1 - Alfa-hélice e suas interações
Com base no texto anterior e em vossos conhecimentos atualizados, pode-se afirmar que as interações que aparecem pontilhadas na Figura1 se referem a
Provas
Um determinado descongestionante nasal contém como princípio ativo um composto denominado tecnicamente de fenilpropanolamina. A característica principal desse reagente químico é ser cancerígeno. Assim, é recomendável a utilização da solução fisiológica de cloreto de sódio.
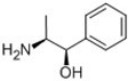
De acordo com o texto exposto e da estrutura fornecida, é correto afirmar que as funções orgânicas presentes na molécula do composto são
Dado: Fórmula estrutural do princípio ativo
Provas
Um analista de laboratório químico dispõe de uma solução de N(OH)2 cujo rótulo apresenta os dados que seguem: 10 g do soluto, solubilizado em 110 g do solvente (H2O). Ao lado dessas informações aparece escrito o teor de OH-= 1,09 %(m/m). A partir dos valores apresentados, é correto afirmar que a concentração expressa em mol L-1 e em título, %(m/m), em termos do composto N(OH)2, são, respectivamente
Dados: MMN= 226 g mol -1; dsolução= 1,00001 g cm-3; T= 20,0 ºC.
Provas
Os carregadores de bateria de celulares fornecem energia, na forma de corrente contínua, para dar carga às mesmas, quando ligados a fonte alternada. Por sua vez, a bateria carregada permite o funcionamento desses aparelhos. Essa mesma energia, estocada na bateria do celular, pode ser utilizada para promover outras reações químicas, quando associada a um par de eletrodos mergulhados numa solução iônica de íons não inertes, em uma cuba eletrolítica. Neste sentido, é correto afirmar que se está a falar das possibilidades de conversão da energia elétrica da rede
Provas
Os experimentos apresentados abaixo, para a reação redox entre permanganato e oxalato de potássio em meio de ácido sulfúrico, apresentaram diferentes resultados; vide quadro 1.
|
QUADRO 1 |
|
|
Resultados experimentais, para cada uma das reações levadas a termo |
|
| I |
T= 10 ºC, resfriamento prévio, mais excesso de MnO4- ; não reage |
| II |
T= 25 ºC, aquecimento prévio, sem excesso de MnO4-; não reage |
| III |
T= 60 ºC, aquecimento prévio, mais excesso de MnO4-; reage |
| IV |
T= 90 ºC, aquecimento prévio, mais excesso de MnO4-; não reage (C2O4-2 decompõe a 90 ºC) |
Os potenciais padrões para as semirreações são dados a seguir: Eº MnO4-/Mn2+= 1,51 V e Eº H2C2O4/CO2= -0,46 V; e a equação para o cálculo do ΔG = -nFΔE.
Reação a ser avaliada, frente às diferentes condições experimentais, é apresentada abaixo, já balanceada:
2 MnO4- + 5 C2O4-2 + 16 H+ !$ \leftrightarrows !$ 2 Mn2+ + 10 CO2 + 8 H2O – (conduzida em meio fortemente ácido de H2SO4 2 mol L-1)
A partir das considerações e condições experimentais apresentadas anteriormente, para a realização das reações de I a IV, é correto afirmar que a condição efetiva é devida ao fato da reação redox
Provas
Leia o texto para responder a questão.
Uma solução aquosa de hidróxido de rubídio (RbOH) de concentração expressa em molar (mol L-1) foi preparada e necessitou ser quantificada. Para a quantificação da base, um analista titulou uma massa do padrão primário hidrogenoftalato de potássio (HF K; MM= 200 g mol-1) usando como indicador a fenolftaleína.
De acordo com o texto e os dados fornecidos a seguir, obtidos da titulação, é correto afirmar que a concentração analítica do RbOH, expresso em mol L-1, é
Dados: número de mol do HFKusado na titulação = 1,05x10-4 mol; Vgasto na titulação = 9,95 mL
Provas
Os experimentos realizados com tubos de raios catódicos permitiram evidenciar que os átomos contêm partículas subatômicas com cargas negativas ou elétrons e permitiu a um determinado cientista, à época, a proposição de que tais partículas encontravam-se dispersas em meio as cargas positivas. De posse do texto anterior é correto afirmar que o propositor de tal modelo atômico foi
Provas
O ácido acético (CH3COOH) é um ácido orgânico fraco (Ki~ 1,79 x 10-5) a 35 ºC. Este ácido, em sendo diluído em água, à mesma temperatura, permite a intensificação do brilho do filamento de uma lâmpada incandescente. O contato elétrico da lâmpada à solução aquosa, para permitir a passagem de corrente elétrica pelo sistema, é feito a partir de eletrodos de cobre, previamente conectados à energia elétrica (E= 220 V / 50 Hz). Assim, de acordo com o explanado, é correto afirmar que a quantidade relativa das espécies CH3COO- e H+ do ácido (expressa em %) em solução aumenta com o favorecimento da
Provas
Caderno Container