Foram encontradas 36.278 questões.
O índice de deficiência de hidrogênio (IDH) é um dado bastante
útil para a previsão da estrutura de um composto orgânico. Para
um composto de fórmula genérica CaHbNcOdXe (em que X
representa um halogênio), o IDH pode ser medido por meio da
seguinte expressão:
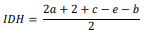
O composto que possui IDH igual a 4 é o
O composto que possui IDH igual a 4 é o
Provas
Questão presente nas seguintes provas
Os primeiros relatos sobre o uso da pólvora se deram entre os chineses na Idade Média. A composição clássica desse material contém nitrato de potássio, carvão vegetal (carbono) e enxofre. Quando reagem entre si, esses compostos produzem nitrogênio gasoso, gás carbônico, carbonato de potássio e sulfato de potássio sólidos, além de grande quantidade de energia.
A soma dos menores inteiros que balanceiam corretamente a reação descrita é igual a
Provas
Questão presente nas seguintes provas
A análise química elementar ocorre tanto em nível qualitativo
como em nível quantitativo. Durante um processo de análise
procedeu-se à combustão completa de 18,0mg de uma
determinada substância orgânica formada somente por carbono,
hidrogênio e oxigênio. Nesse processo, foram obtidos 39,6mg de
gás carbônico e 21,6mg de água.
A fórmula molecular da referida substância orgânica é
A fórmula molecular da referida substância orgânica é
Provas
Questão presente nas seguintes provas
A Classificação Periódica dos Elementos é uma das mais
importantes ferramentas para o trabalho de químicos, sendo
construída a partir de padrões que se repetem periodicamente.
Observe a tabela a seguir, na qual uma propriedade periódica X é apresentada, com unidade de medida adequada, para três elementos químicos.
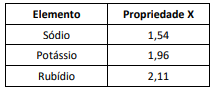
A propriedade representada por X é
Observe a tabela a seguir, na qual uma propriedade periódica X é apresentada, com unidade de medida adequada, para três elementos químicos.

A propriedade representada por X é
Provas
Questão presente nas seguintes provas
No século XVIII as transformações químicas foram atreladas a um
“princípio material da inflamabilidade”, que ficou conhecido
como flogisto. Assim, segundo esse princípio, em reações como a
combustão de matéria orgânica ou a queima de metais, ocorria a
liberação de flogisto, indicada pela presença de luz e calor.
Atualmente tais processos podem ser classificados como reações de
Atualmente tais processos podem ser classificados como reações de
Provas
Questão presente nas seguintes provas
Uma das regras de ligação química mais conhecidas é a chamada
regra do octeto, na qual cada átomo tende a ficar com oito
elétrons em sua camada de valência. No entanto, elementos a
partir do terceiro período, por possuírem orbitais vazios, podem
acomodar uma quantidade maior de elétrons, ocorrendo a
chamada “expansão do octeto”. Isso ocorre, por exemplo, em
moléculas como SF4, BrF3 e XeF4.
Para essas moléculas, as geometrias espaciais são, respectivamente,
Para essas moléculas, as geometrias espaciais são, respectivamente,
Provas
Questão presente nas seguintes provas
Considere os seguintes tipos de misturas:
I. mistura de sais existentes na água do mar;
II. mistura dos gases nitrogênio e oxigênio componentes do ar atmosférico;
III. mistura de água e areia;
IV. mistura de sal e iodo.
Assinale a opção que apresenta corretamente o número da mistura e seu respectivo método de separação.
I. mistura de sais existentes na água do mar;
II. mistura dos gases nitrogênio e oxigênio componentes do ar atmosférico;
III. mistura de água e areia;
IV. mistura de sal e iodo.
Assinale a opção que apresenta corretamente o número da mistura e seu respectivo método de separação.
Provas
Questão presente nas seguintes provas
Base é uma classificação dada às substâncias
inorgânicas que, em contato com a água, liberam íons
hidroxila, de acordo com a teoria de Arrhenius. Atente para
as afirmações a seguir e assinale com V as verdadeiras e
com F as falsas.
( ) Em contato com ácidos, as bases reagem por reação de neutralização, formando sal e água como produtos.
( ) As bases sofrem ionização em água, liberando íons hidroxila (OH – ).
( ) Na ionização em água, as bases aumentam a concentração de íons (OH – ).
( ) As soluções básicas são caracterizadas por valor de pH acima de 7.
A sequência correta, de cima para baixo é:
( ) Em contato com ácidos, as bases reagem por reação de neutralização, formando sal e água como produtos.
( ) As bases sofrem ionização em água, liberando íons hidroxila (OH – ).
( ) Na ionização em água, as bases aumentam a concentração de íons (OH – ).
( ) As soluções básicas são caracterizadas por valor de pH acima de 7.
A sequência correta, de cima para baixo é:
Provas
Questão presente nas seguintes provas
A combustão completa do pentano ocorre segundo a
reação, representada pela seguinte equação química não
balanceada:
C5H12(g) + O2(g) → CO2(g) + H2O(g)
Atente para as seguintes afirmações referentes às relações dos volumes dos reagentes consumidos e dos produtos obtidos.
I. A relação entre os volumes de C5H12(g) consumido e de CO2(g) obtido é de 2:5.
II. A relação entre os volumes de O2(g) consumido e de CO2(g) obtido é de 8:5.
III. A relação entre os volumes de C5H12(g) consumido e de H2O(g) obtido é de 1:6.
É correto o que se afirma em
C5H12(g) + O2(g) → CO2(g) + H2O(g)
Atente para as seguintes afirmações referentes às relações dos volumes dos reagentes consumidos e dos produtos obtidos.
I. A relação entre os volumes de C5H12(g) consumido e de CO2(g) obtido é de 2:5.
II. A relação entre os volumes de O2(g) consumido e de CO2(g) obtido é de 8:5.
III. A relação entre os volumes de C5H12(g) consumido e de H2O(g) obtido é de 1:6.
É correto o que se afirma em
Provas
Questão presente nas seguintes provas
A tabela periódica organiza os elementos químicos
em uma ordem crescente de número atômico. As
propriedades químicas e físicas dos elementos que variam
periodicamente são chamadas de propriedades periódicas.
Relacione corretamente essas propriedades periódicas com
seus respectivos significados, numerando os parênteses de
acordo com a seguinte indicação:
1. eletronegatividade; 2. energia de ionização; 3. afinidade eletrônica; 4. eletropositividade.
( ) Energia liberada quando um elétron adicional é acrescentado a um átomo no estado gasoso.
( ) Energia mínima necessária para remover um elétron de um átomo ou íon no estado gasoso.
( ) Tendência do átomo em doar elétrons durante as ligações químicas.
( ) Tendência que um átomo tem de atrair elétrons para si em uma ligação química em uma molécula isolada.
A sequência correta, de cima para baixo, é:
1. eletronegatividade; 2. energia de ionização; 3. afinidade eletrônica; 4. eletropositividade.
( ) Energia liberada quando um elétron adicional é acrescentado a um átomo no estado gasoso.
( ) Energia mínima necessária para remover um elétron de um átomo ou íon no estado gasoso.
( ) Tendência do átomo em doar elétrons durante as ligações químicas.
( ) Tendência que um átomo tem de atrair elétrons para si em uma ligação química em uma molécula isolada.
A sequência correta, de cima para baixo, é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container