Foram encontradas 35.936 questões.
O químico responsável pelo laboratório realizou
a preparação de uma solução aquosa de cloreto de
cálcio (CaCl₂), utilizando um balão volumétrico de 250
mL. Inicialmente, foi medida a quantidade necessária
do sal, utilizando uma balança analítica. O sólido foi
dissolvido com parte da água destilada em um béquer
e, em seguida, transferido quantitativamente para o
balão volumétrico, completando-se o volume até a
marca com mais água.
Analise as afirmativas abaixo com base na situação descrita.
1. O cloreto de cálcio é um composto iônico, formado por ligações entre cátions cálcio (Ca2+) e ânions cloreto (Cl–).
2. O balão volumétrico não é a vidraria adequada para preparar soluções com concentração conhecida e exatidão.
3. A solubilidade do sal em água é uma propriedade físico-química que depende da temperatura e da polaridade do solvente.
4. A escolha do reagente e sua quantidade correta são fundamentais para garantir a concentração molar desejada na solução.
5. A estrutura da matéria no estado líquido do CaCl₂ apresenta uma rede cristalina organizada por forças eletrostáticas.
Assinale a alternativa que indica todas as afirmativas corretas.
Analise as afirmativas abaixo com base na situação descrita.
1. O cloreto de cálcio é um composto iônico, formado por ligações entre cátions cálcio (Ca2+) e ânions cloreto (Cl–).
2. O balão volumétrico não é a vidraria adequada para preparar soluções com concentração conhecida e exatidão.
3. A solubilidade do sal em água é uma propriedade físico-química que depende da temperatura e da polaridade do solvente.
4. A escolha do reagente e sua quantidade correta são fundamentais para garantir a concentração molar desejada na solução.
5. A estrutura da matéria no estado líquido do CaCl₂ apresenta uma rede cristalina organizada por forças eletrostáticas.
Assinale a alternativa que indica todas as afirmativas corretas.
Provas
Questão presente nas seguintes provas
No ensino de Ciências, a distinção entre
fenômenos físicos e químicos é introdutória ao estudo das
reações. Analise os processos abaixo:
Derretimento de um cubo de gelo. Queima de um pedaço de papel. Evaporação da água do mar. Enferrujamento de um prego de ferro.
Derretimento de um cubo de gelo. Queima de um pedaço de papel. Evaporação da água do mar. Enferrujamento de um prego de ferro.
Assinale a alternativa que agrupa corretamente apenas os processos classificados como Fenômenos Químicos (onde há alteração na estrutura íntima da matéria e formação de novas substâncias):
Provas
Questão presente nas seguintes provas
Em um recipiente foram colocados óleo, água e
sal. Esse sistema apresenta:
Provas
Questão presente nas seguintes provas
Observe a figura abaixo:
Fonte: PUTVINSKIS, Rodrigo. Do seu jeito: Química: área de Ciências da Natureza e suas Tecnologias: volume único: Ensino médio. 1. ed. São Paulo: Ática, 2024.
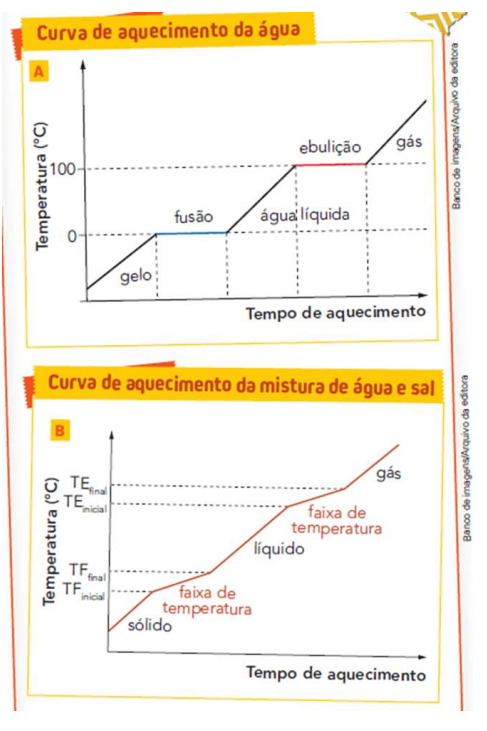
Na figura, são apresentados diagramas com as curvas de aquecimento, que mostram a variação da temperatura em função do tempo para uma substância pura, a água, e para uma mistura de água e sal.
De acordo com esses diagramas, podemos inferir:
I. No diagrama A, durante a fusão e a ebulição, as temperaturas permanecem constantes ao longo de todo o intervalo de tempo em que ocorre a mudança de estado físico. Por se tratar de uma substância pura, a água funde-se a 0 °C e entra em ebulição a 100 °C. Essas temperaturas não se alteram até que toda a substância tenha completado a mudança de estado. Por isso, a curva de aquecimento da água apresenta dois patamares bem definidos.
II. No diagrama B, tal como no diagrama A, formam-se patamares constantes de temperatura durante a fusão e a ebulição, mesmo se tratando de uma mistura de água e sal.
A partir da análise dos itens, é possível AFIRMAR que:

Fonte: PUTVINSKIS, Rodrigo. Do seu jeito: Química: área de Ciências da Natureza e suas Tecnologias: volume único: Ensino médio. 1. ed. São Paulo: Ática, 2024.
Na figura, são apresentados diagramas com as curvas de aquecimento, que mostram a variação da temperatura em função do tempo para uma substância pura, a água, e para uma mistura de água e sal.
De acordo com esses diagramas, podemos inferir:
I. No diagrama A, durante a fusão e a ebulição, as temperaturas permanecem constantes ao longo de todo o intervalo de tempo em que ocorre a mudança de estado físico. Por se tratar de uma substância pura, a água funde-se a 0 °C e entra em ebulição a 100 °C. Essas temperaturas não se alteram até que toda a substância tenha completado a mudança de estado. Por isso, a curva de aquecimento da água apresenta dois patamares bem definidos.
II. No diagrama B, tal como no diagrama A, formam-se patamares constantes de temperatura durante a fusão e a ebulição, mesmo se tratando de uma mistura de água e sal.
A partir da análise dos itens, é possível AFIRMAR que:
Provas
Questão presente nas seguintes provas
O estudo das variações na composição do ar (tipos de
gases e suas proporções), da temperatura e de eventos
atmosféricos, como ventos, relâmpagos e formação de
nuvens, torna-se mais organizado quando a atmosfera é
dividida em camadas. Essa divisão não é absoluta,
havendo áreas de transição, chamadas de pausas. A camada em questão situa-se aproximadamente entre 16
e 50 quilômetros de altitude. Nela concentra-se quase
todo o ozônio da atmosfera, formando a chamada
camada de ozônio. A temperatura média nessa camada
é de aproximadamente − 3 °C. O ar é bastante rarefeito e
praticamente livre de fenômenos como ventos fortes e
nuvens de chuva, permitindo o uso de balões
meteorológicos e, em sua porção inferior, o voo de
alguns aviões comerciais.
Fonte: JORNADAS: Novos caminhos: Ciências: 6º ano / obra coletiva; editora responsável Daniela Teves Nardi. − 1. ed. − São Paulo: Saraiva Educação S.A., 2022.
Essa camada é a:
Fonte: JORNADAS: Novos caminhos: Ciências: 6º ano / obra coletiva; editora responsável Daniela Teves Nardi. − 1. ed. − São Paulo: Saraiva Educação S.A., 2022.
Essa camada é a:
Provas
Questão presente nas seguintes provas
Em um laboratório analítico, a rastreabilidade
das medições é assegurada por meio de uma
cadeia de autenticação que liga o resultado
analítico aos padrões de referência
internacionais. Qual das alternativas melhor
descreve o principal objetivo da rastreabilidade
na prática analítica?
Provas
Questão presente nas seguintes provas
Durante uma titulação ácido-base, utiliza-se um
indicador para determinar o ponto final da
reação. Sobre os indicadores, assinale a
alternativa correta.
Provas
Questão presente nas seguintes provas
Em um experimento de espectrofotometria
UV/VIS para determinação de um analito, foram
obtidas cinco leituras da absorbância: 0,312;
0,328; 0,319; 0,327; 0,315. Considere que o erro
entre leituras pode ser constituído por erro
aleatório e erro sistemático. Qual das afirmações
a seguir descreve adequadamente as
características de cada tipo de erro?
Provas
Questão presente nas seguintes provas
Qual é a função principal de um padrão de
verificação (PV) em laboratório analítico?
Provas
Questão presente nas seguintes provas
Durante uma titulação ácido-base, uma bureta de
50 mL foi utilizada para entregar 25,00 mL de
titulante, com leitura inicial de 0,00 mL e leitura
final de 25,12 mL. Considerando que a bureta
possui resolução de 0,01 mL e que o trajeto entre
leituras é confiável, qual é a incerteza associada
ao volume titulante utilizado?
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container