Foram encontradas 36.279 questões.
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Observe as estruturas dos ácidos abaixo:
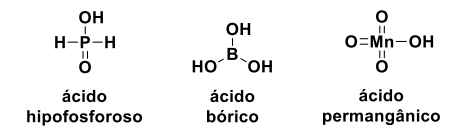
Sobre esses ácidos, analise as seguintes afirmações:
1. O ácido hipofosforoso possui três hidrogênios ionizáveis.
2. No ácido permangânico, o número de oxidação do Mn é +7.
3. O ácido bórico possui hibridação sp2 e geometria trigonal plana.
4. Devido à presença do metal, o ácido permangânico é o mais fraco.
Estão corretas, apenas:
Provas
Um estudante do curso de química elaborou um trabalho sobre os óxidos. Dentre outros materiais preparados para a apresentação, havia uma tabela com as classificações dos óxidos, exemplos e reações:
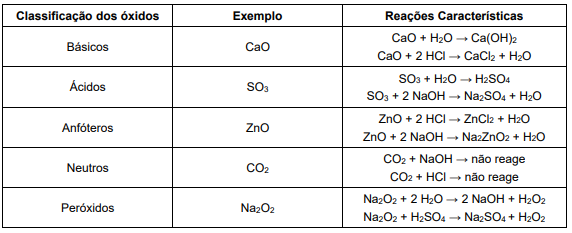
Ao observar a tabela, o professor precisou explicar ao estudante que um exemplo estava errado e não correspondia à classificação sugerida. A categoria cujo exemplo está incorreto é a dos óxidos:
Provas
Usado para a limpeza de peças e ferramentas, o ácido muriático é uma solução impura de ácido clorídrico e pode ser encontrado em lojas de materiais de construção. Com o objetivo de determinar a concentração de um lote desse produto em termos de porcentagem de HCl (m/V), um químico reagiu uma alíquota de 50mL do ácido muriático comercial com carbonato de cálcio em excesso, conforme a reação:
![]()
Nesse experimento, o volume coletado de CO2 foi 6,15L a 27ºC e 1 atm. Qual é a porcentagem de HCl (m/V) na amostra de ácido muriático?
Massas molares (g/mol): H = 1; C = 12; O = 16; Cl = 35,5; Ca = 40
Provas
A amônia (NH3) é uma substância muito utilizada para a produção de fertilizantes. Uma maneira de se obter a amônia é a partir da reação:
![]()
Considere que, em uma indústria química, são colocados em um reator 60kg de NaOH, 66kg de (NH4)2SO4 e água suficiente para solubilizar os reagentes. A reação ocorre até que um dos reagentes seja completamente consumido. Considerando as CNTP, o volume obtido de NH3(g) é:
Massas molares (g/mol): H = 1; O = 16; N = 14; Na = 23; S = 32
Provas
A produção de ferro metálico para solda pode ser realizada a partir da reação entre alumínio metálico e óxido férrico, de acordo com a reação abaixo:
![]()
Considerando que essa reação tem um rendimento de 90%, calcule a massa de alumínio necessária para a produção de 11,2 kg de ferro para solda.
Massas molares (g/mol): O = 16; Al = 27; Fe = 56.
Provas
Uma indústria química é especializada na produção de sais de cromato (CrO4 2- ). Uma das reações envolvidas no processo é mostrada abaixo:
![]()
A reação não está balanceada. Faça o balanceamento, considerando os menores inteiros como coeficientes reacionais. A soma desses coeficientes é igual a:
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química InorgânicaReações InorgânicasCálculo Estequiométrico
O elemento mercúrio é o único metal líquido à temperatura ambiente. Considere uma amostra de 400mL de mercúrio. Quantos átomos do metal, aproximadamente, estão presentes nessa amostra?
Dados: densidade Hg(l) = 13,6 kg/dm3 ; massa molar Hg = 200 g/mol; considere o número de Avogadro = 6 x 1023
Provas
Quando a temperatura é 227ºC, a reação entre os gases PCl3 e Cl2, que forma o produto também gasoso PCl5, tem sua constante de equilíbrio expressa em termos de concentrações molares igual a 3400.
![]()
Considere que a reação acima está em equilíbrio e que as concentrações de PCl3 e Cl2 são 1,0 x 10-3 molL-1 e 1,0 x 10-2 molL-1 , respectivamente. Nessas condições, a pressão de PCl5 no equilíbrio será:
Provas
Uma amostra de água contém íons chumbo (Pb2+) dissolvidos com a concentração igual a 1,0 x 10-4 molL-1 . Para realizar a precipitação desses cátions, adiciona-se progressivamente NaCl sólido. Determine a concentração mínima de íons cloreto (em molL-1 ) a partir da qual se iniciará o processo de precipitação de PbCl2.
Dado: Kps (PbCl2) = 1,6 x 10-5
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSubstâncias Inorgânicas: dissociação iônica e ionização, conceitos de ácido-base
Considere os dados da tabela abaixo:
![]()
De acordo com os dados acima, o ânion que atua como base mais forte é:
Provas
Caderno Container