Foram encontradas 36.174 questões.
A determinação de pH de amostras de água com uso de
pHmetro e eletrodo de vidro é uma técnica amplamente
utilizada em laboratórios de química analítica e ambiental. No entanto, com base em diversos fatores podem
afetar a precisão do resultado dessas análises químicas,
é correto considerar que
Provas
Questão presente nas seguintes provas
Durante a análise de água por ICP-OES, a amostra é
convertida em aerossol e introduzida em um plasma de
argônio a alta temperatura.
Nesse meio, ocorre excitação dos átomos presentes, que emitem radiação ao retornarem ao estado fundamental, o que permite
Nesse meio, ocorre excitação dos átomos presentes, que emitem radiação ao retornarem ao estado fundamental, o que permite
Provas
Questão presente nas seguintes provas
Um resíduo líquido destinado a descarte de um laboratório químico consiste em uma solução aquosa de piridina
(C5
H5
N) com concentração 5,0 x 10–4
mol/L.
Considerando que a constante Kb da piridina é aproximadamente 2 x 10–9 , o pH dessa solução é, aproximadamente,
Considerando que a constante Kb da piridina é aproximadamente 2 x 10–9 , o pH dessa solução é, aproximadamente,
Provas
Questão presente nas seguintes provas
Na determinação da demanda bioquímica de oxigênio (DBO5) a amostra de água é incubada em condições específicas
por um período de 5 dias. O teor de oxigênio na amostra é determinado em dois momentos: antes da incubação, oxigênio
dissolvido inicial (OD0) e após a incubação, oxigênio dissolvido final (OD5).
As determinações de OD0 e de OD5 podem ser feitas pelo método Winkler, um método titulométrico. Esse método baseia-se nas reações representadas nas equações a seguir.
2Mn2+(aq) + 4OH− (aq) + O2 (aq) → 2MnO(OH)2 (s)
2MnO(OH)2 (s) + 2I− (aq) + 4H+(aq) → Mn2+ (aq) + I2 (aq) + 3H2 O (l)
I2 (aq) + 2S2 O3 2−(aq) → 2I−(aq) + S4 O6 2−(aq)
No método Winkler, o agente titulante é uma solução padrão de e o indicador é . As lacunas são preenchidas, correta e respectivamente, por
As determinações de OD0 e de OD5 podem ser feitas pelo método Winkler, um método titulométrico. Esse método baseia-se nas reações representadas nas equações a seguir.
2Mn2+(aq) + 4OH− (aq) + O2 (aq) → 2MnO(OH)2 (s)
2MnO(OH)2 (s) + 2I− (aq) + 4H+(aq) → Mn2+ (aq) + I2 (aq) + 3H2 O (l)
I2 (aq) + 2S2 O3 2−(aq) → 2I−(aq) + S4 O6 2−(aq)
No método Winkler, o agente titulante é uma solução padrão de e o indicador é . As lacunas são preenchidas, correta e respectivamente, por
Provas
Questão presente nas seguintes provas
Existem algumas formas para medir indiretamente o
estresse biótico de uma planta quando submetida ao
ataque de pragas ou à aplicação de um defensivo
agrícola. Uma forma interessante é a avaliação da
atividade de enzima peroxidase em um extrato vegetal
dessa planta. Conhecendo essa atividade, sabe-se que
quanto maior ela for, maior é a existência de combate às
chamadas formas reativas de oxigênio, e, portanto, maior
o estresse biótico devido ao combate à radicais livres
que prejudicam a saúde da planta. Uma das formas de
quantificar a atividade de peroxidase é pela reação do
guaiacol com peróxido de hidrogênio (H2O2), catalisada
pela enzima peroxidase do extrato vegetal, formando o
tetrahidroguaiacol (guaiacol.4H2O), cuja coloração
castanha pode ser monitorada em espectrofotômetro a
470 nm, e é diretamente proporcional ao aumento de
absorbância. Um ensaio foi realizado em cubeta de
quartzo com volume igual a 5,0 ml por um período de
120 segundos, com o resultado sendo apresentado na
tabela a seguir:
Reação:

Com base na reação, na equação, e na tabela, determine a atividade aproximada de peroxidase observada no ensaio, em (µmol de tetrahidroguaiacol gerado.min-1).
Reação:

Com base na reação, na equação, e na tabela, determine a atividade aproximada de peroxidase observada no ensaio, em (µmol de tetrahidroguaiacol gerado.min-1).
Provas
Questão presente nas seguintes provas
Para realizar a análise de Carbono Orgânico no solo,
pode-se utilizada a técnica de titulação de Dicromato de
Potássio (K2Cr2O7) em excesso com Sulfato Ferroso
(FeSO4). Para isso, pesa-se 0,5000 g de solo, coloca-se
em um frasco erlenmeyer, e adiciona-se 10,0 ml de
solução de K2Cr2O7 1,25 mol.l-1 (reagente limitante), e
20,0 ml de Ácido Sulfúrico concentrado (H2SO4)
(reagente em excesso). Aquece-se a solução com
cuidado por um minuto em Bico de Bunsen a 150°C,
deixa-se esfriar, e coloca-se a mistura em uma proveta
com água destilada de forma a completar 100,0 ml de
volume total. Então, após decantar o solo após aguardar
30 minutos, coletam-se 50,0 ml do sobrenadante em
outro erlenmeyer, adicionam-se 3 gotas de indicador
ortofenantrolina (que se torna vermelho na presença de
íons Fe2+), e realiza-se a titulação com FeSO4
1,0 mol.l-1, com Ácido Sulfúrico em excesso. Em um
ensaio, observou-se na titulação o uso de um volume
consumido de 27,0 ml de solução de FeSO4 até a
viragem do indicador. Para esse ensaio, o solo analisado
tinha uma porcentagem em massa de carbono orgânico
igual a aproximadamente
Reações: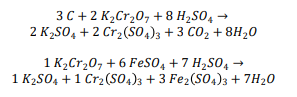
Reações:
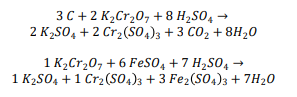
Provas
Questão presente nas seguintes provas
Para medir a quantidade de fósforo presente em uma
amostra de solo, primeiramente pesam-se 5,0000
gramas de solo (TFSA) e adicionam-se 50,0 ml de
solução ácida extratora Mehlich (0,05 mol.l-1 de HCl e
0,025 mol.l-1 de H2SO4). Após 24 horas, retiram-se 5,0 ml
do sobrenadante e adicionam-se 45,0 ml de uma solução
padronizada de ácido ascórbico (vitamina C) e
heptamolibdato de amônio, que desenvolve coloração
azul em 680 nm em espectrofotômetro com absorbância
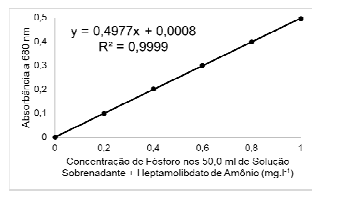
linearmente proporcional à concentração de fósforo. A
curva-padrão para os 50,0 ml totais de solução
sobrenadante + heptamolibdato de amônio é
apresentada a seguir. Para uma amostra, observou-se
uma leitura de absorbância de 0,350 no
espectrofotômetro. Qual é a concentração de fósforo
presente nesse solo?

Provas
Questão presente nas seguintes provas
Para realizar a medida do teor de nitrogênio em uma
amostra de solo, inicialmente pesa-se 0,5000 de solo,
adicionam-se 1,0 ml de Peróxido de Hidrogênio (H2O2)
com porcentagem mássica 30%, e 2,0 ml de Ácido
Sulfúrico (H2SO4) concentrado, todos em excesso.
Espera-se esfriar e, então transfere-se para um tubo
adequado junto com 0,7 g de uma mistura de digestão,
levando ao bloco digestor por 2500C por 20 minutos e
depois a 3750C por duas horas, até que a solução clareie.
Após esfriar, transfere-se quantitativamente a solução
com auxílio de um pouco de água destilada até um
frasco de destilação. Adiciona-se vagarosamente 10,0 ml
de Hidróxido de Sódio (NaOH) a 10 mol.l-1 dentro do
frasco de destilação e liga-se o aparelho. Destila-se até
obter 35,0 ml de destilado, dentro de um frasco
erlenmeyer já com 5,0 ml de solução indicadora de Ácido
Bórico (H3BO3). Todo o nitrogênio da amostra de solo
está presente na forma de Hidróxido de Amônio (NH4OH)
no destilado. Então, realiza-se a titulação do destilado
com H2SO4 0,025 mol.l-1. Na titulação, necessitou-se de
um volume de 20,0 ml de Ácido Sulfúrico até se observar
a viragem de cor do indicador. A porcentagem de
nitrogênio em massa que existe nesse solo é
aproximadamente
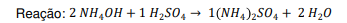
Provas
Questão presente nas seguintes provas
Para realizar a análise da concentração de cálcio e
magnésio em uma amostra de solo, pesam-se 5,0000
gramas de terra fina seca ao ar (TFSA) e adicionam-se
50,0 ml de solução extratora de cloreto de potássio 1,00
mol.l-1, assim como na análise de acidez devido ao
alumínio. Após agitar e deixar um dia de repouso, retira-se o sobrenadante e filtra-se, realizando posteriormente
uma diluição 1:12 neste para a análise de cálcio e 1:36
para a análise de magnésio, utilizando como solvente
uma solução de 34,2 mmol.l-1 de cloreto de estrôncio
(SrCl2) e 200 mmol.l-1 de ácido clorídrico (HCl), que terá
a finalidade de reduzir efeitos de interferência de outros
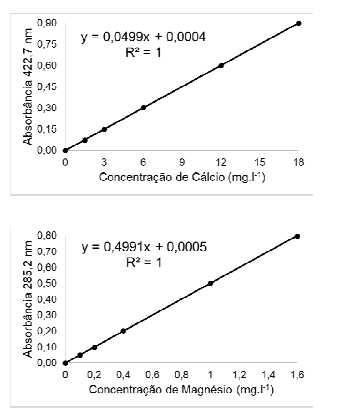
íons. A análise das amostras é realizada por
espectrometria de absorção atômica, onde as
curvas-padrão do equipamento constam nos gráficos a
seguir. Para uma dada amostra de solo, obtiveram-se as
leituras de absorbância de 0,350 para o Cálcio e de
0,650 para o Magnésio. A concentração desses dois
elementos químicos no solo é igual a

Provas
Questão presente nas seguintes provas
Para analisar a acidez relativa à presença de alumínio no
solo, dada em centimols de carga equivalentes de íons
H+
, é necessário executar a seguinte técnica: Pesam-se
5,0000 gramas de amostra de Terra Fina Seca ao Ar
(TFSA) e adicionam-se 50,0 ml de solução extratora de
KCl na concentração de 1,00 mol por litro. No dia
seguinte, coletam-se 25,0 ml do sobrenadante,
adicionam-se 3 gotas de fenolftaleína, e realiza-se
titulação utilizando na bureta uma solução de 2,5
centimols por litro de hidróxido de sódio (NaOH). Após
realizar a titulação de uma amostra, a fenolftaleína virou
de transparente para rosa após a adição de 3,0 ml dessa
solução de NaOH. Com base nisso, a acidez relativa à
presença de alumínio no solo é igual a
Reação: H+ + Na0H → Na+ + H20
Reação: H+ + Na0H → Na+ + H20
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container