Foram encontradas 36.167 questões.
A proporcionalidade em reações químicas é a relação constante entre as massas dos reagentes e as massas dos produtos, o que é estabelecido pela Lei de Proust. Nas representações de reações químicas é sempre discriminada essa proporcionalidade.
Considere a seguinte reação:
1 H2SO4 + 2 NaOH → 1 Na2SO4 + 2 H2O
As massas de H2SO4 e de NaOH necessárias para que essa reação mantenha a proporcionalidade indicada serão, respectivamente, em g, iguais a
Considere a seguinte reação:
1 H2SO4 + 2 NaOH → 1 Na2SO4 + 2 H2O
As massas de H2SO4 e de NaOH necessárias para que essa reação mantenha a proporcionalidade indicada serão, respectivamente, em g, iguais a
Provas
Questão presente nas seguintes provas
As substâncias químicas apresentam diversas propriedades, sendo o pH uma delas. Essa propriedade permite
diferenciar as substâncias em ácidas, neutras ou básicas, conforme o valor de pH que elas apresentam. Sua
determinação pode ser feita por aparelho específico, ou
por meio de indicadores que têm a propriedade de mudar
a cor conforme o pH da substância. Esse é o caso do
papel indicador universal, que permite a determinação do
pH conforme a cor.
A seguir a representação de uma fita de papel indicador universal:
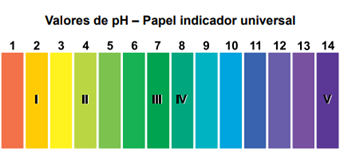
(Disponível em: https://cursoparalaunam.com/indicadores-y-ph/ Adaptado)
Considere a realização de um teste de pH utilizando o papel indicador universal com as substâncias NaOH, HNO3 e H2 O. Nesse caso, os prováveis números que podem representar essas substâncias, respectivamente, são
A seguir a representação de uma fita de papel indicador universal:

(Disponível em: https://cursoparalaunam.com/indicadores-y-ph/ Adaptado)
Considere a realização de um teste de pH utilizando o papel indicador universal com as substâncias NaOH, HNO3 e H2 O. Nesse caso, os prováveis números que podem representar essas substâncias, respectivamente, são
Provas
Questão presente nas seguintes provas
O gás sulfídrico (H2S), como é popularmente conhecido, ocorre naturalmente no petróleo cru, no gás natural, em gases vulcânicos e em mananciais de águas termais, caracterizado pelo cheiro de ovo podre. Ocorre, também, como resultado da degradação bacteriana de matéria orgânica em condições anaeróbicas, em ambientes aquáticos. No ambiente, esse gás é convertido em dióxido de enxofre (SO2), um poluente com origem em fontes antropogênicas. A reação química, não balanceada, desse processo é indicada a seguir:
X H2S + Y O2 → W H2O + K SO2
Para a reação química apresentada ficar balanceada, os valores de X, Y, W e K devem ser, respectivamente,
X H2S + Y O2 → W H2O + K SO2
Para a reação química apresentada ficar balanceada, os valores de X, Y, W e K devem ser, respectivamente,
Provas
Questão presente nas seguintes provas
Qual a soma dos menores números inteiros que fazem o CORRETO balanceamento da reação química a seguir?
\(KMnO_{4} + H_{2}O_{2} + H_{2}SO_{4} \rightarrow K_{2}SO_{4} + MnSO_{4} + H_{2}O + O_{2}\)
Provas
Questão presente nas seguintes provas
Sobre reações químicas, avaliar se as afirmativas são
certas (C) ou erradas (E) e assinalar a sequência
correspondente.
( ) São essencialmente transformações de energia nas quais a energia estocada nas ligações químicas é transferida para novas ligações formadas. Nessas transferências, os elétrons mudam de um nível energético para outro.
( ) Em muitas reações, os elétrons passam de um átomo ou uma molécula para outro átomo ou molécula. Essas reações, conhecidas como reações de oxidação-redução (também conhecidas como oxirredução ou reações redox), são de grande importância nos organismos vivos.
( ) São essencialmente transformações de energia nas quais a energia estocada nas ligações químicas é transferida para novas ligações formadas. Nessas transferências, os elétrons mudam de um nível energético para outro.
( ) Em muitas reações, os elétrons passam de um átomo ou uma molécula para outro átomo ou molécula. Essas reações, conhecidas como reações de oxidação-redução (também conhecidas como oxirredução ou reações redox), são de grande importância nos organismos vivos.
Provas
Questão presente nas seguintes provas
Algumas misturas podem ser classificadas como
homogêneas ou heterogêneas dependendo das
condições em que se encontram, como proporção
dos componentes, temperatura e agitação.
Admitindo que todas as misturas a seguir estejam
em temperatura ambiente (25°C) e sob pressão de 1
atm, qual delas pode ser considerada homogênea ou
heterogênea, dependendo das condições?
Provas
Questão presente nas seguintes provas
A tabela abaixo fornece a temperatura de fusão e a temperatura de ebulição de algumas substâncias químicas sob pressão de 1 atm. Indique a única substância da tabela que se encontra no estado líquido a 20 °C:
Provas
Questão presente nas seguintes provas
O potencial-padrão de redução de um metal indica quão facilmente ele se reduz (ganha elétrons), sendo um valor
de referência usado para prever reações redox, montar pilhas eletroquímicas e avaliar o comportamento
eletroquímico das substâncias. A tabela a seguir fornece os potenciais-padrão de redução de alguns metais comuns.
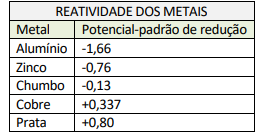
Assinale a alternativa que apresenta os metais mais adequados para a construção de uma pilha de alta voltagem, considerando sua viabilidade prática:

Assinale a alternativa que apresenta os metais mais adequados para a construção de uma pilha de alta voltagem, considerando sua viabilidade prática:
Provas
Questão presente nas seguintes provas
Em um recipiente de 1 litro, foram misturados 12 mols de X2 e 13 mols de Y2. Depois de algum
tempo, o sistema atingiu o equilíbrio e o número de mols de XY3 medido foi 8.
Considerando a seguinte reação: X2 + 3Y2 ⇆ 2XY3, o valor da constante de equilíbrio Kc (mol-2 .L2 ) da reação é:
Considerando a seguinte reação: X2 + 3Y2 ⇆ 2XY3, o valor da constante de equilíbrio Kc (mol-2 .L2 ) da reação é:
Provas
Questão presente nas seguintes provas
Em relação aos Modelos Atômicos, analise as informações:
I Com a descoberta do elétron, Thomson verificou a existência de partículas menores que o átomo, isto é, existem partículas subatômicas. Para Thomson, o átomo era uma esfera positiva com elétrons negativos incrustados, ou seja, não havia núcleo nem níveis de energia.
II Uma importante contribuição do modelo de Rutherford foi considerar o átomo constituído de uma estrutura altamente compactada de prótons e elétrons.
III Supondo que 1 nêutron apresenta massa 1 kg, a massa de um átomo com 11 prótons, 12 nêutrons e 11 elétrons seria de 34 kg.
IV No modelo atômico atual, os elétrons têm caráter corpuscular e de onda simultaneamente.
As informações corretas são apenas:
I Com a descoberta do elétron, Thomson verificou a existência de partículas menores que o átomo, isto é, existem partículas subatômicas. Para Thomson, o átomo era uma esfera positiva com elétrons negativos incrustados, ou seja, não havia núcleo nem níveis de energia.
II Uma importante contribuição do modelo de Rutherford foi considerar o átomo constituído de uma estrutura altamente compactada de prótons e elétrons.
III Supondo que 1 nêutron apresenta massa 1 kg, a massa de um átomo com 11 prótons, 12 nêutrons e 11 elétrons seria de 34 kg.
IV No modelo atômico atual, os elétrons têm caráter corpuscular e de onda simultaneamente.
As informações corretas são apenas:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container