Foram encontradas 36.167 questões.
A figura a seguir apresenta a fórmula estrutural de um alcaloide:

A molécula contém os grupos funcionais pertencentes às funções orgânicas
Provas
A equação a seguir representa esquematicamente uma reação orgânica:
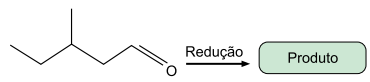
O produto dessa reação apresenta o grupo funcional característico da função orgânica
Provas
A formação do smog fotoquímico é devida
Provas
A entalpia de formação de um composto orgânico de fórmula C5 H5 OH é:
\(\Delta H_f^{\circ} = -277 \dfrac{\text{kJ}}{\text{mol}}\)
Considere as seguintes equações termoquímicas:
\(\begin{align*} 2\text{CO}_2\text{(g)} & \rightarrow 2\text{CO}\text{(g)} + \text{O}_2\text{(g)} & \Delta H^{\circ} &= +566 \, \text{kJ} \\ 2\text{CO}\text{(g)} & \rightarrow \text{C}\text{(s)} + \text{CO}_2\text{(g)} & \Delta H^{\circ} &= -173 \, \text{kJ} \\ \text{H}_2\text{(g)} + {1}/{2} \text{O}_2\text{(g)} & \rightarrow \text{H}_2\text{O}(\ell) & \Delta H^{\circ} &= -286 \, \text{kJ} \end{align*}\)
A entalpia-padrão da combustão completa do composto C5 H5 OH é
Provas
O composto CH3 NH2 interage com a água de acordo com a equação a seguir:
CH3 NH2 (g) + H2O (l) ⇄ CH3 NH3 + (aq) + OH– (aq)
Kb = 3,5 x 10–4
Qual será o pH aproximado de uma solução CH3 NH2 com concentração de 0,2 mol/L?
Dados: no equilíbrio, a concentração de CH3 NH3 + é muito menor do que 0,2 mol/L; (0,7)1/2 = 0,8 e log 0,8 = –0,096.
Provas
O estudo cinético da reação da equação a seguir foi feito em temperatura constante:
\(NH_4^+ (aq) + NO^-_2 (aq) → N_2(g) + 2H_2O(l)\)
Os resultados das velocidades iniciais da reação (Vi) estão apresentados na seguinte tabela:
| [NH4+] (mol.L-1) |
[NO2-] (mol.L-1) |
Vi = Δ[NO2-]/Δt (mol.L-1.s-1) |
|---|---|---|
| 0,0092 | 0,098 | 3,32 x 10-7 |
| 0,0092 | 0,049 | 1,66 x 10-7 |
| 0,0488 | 0,196 | 4,51 x 10-6 |
| 0,0244 | 0,196 | 2,25 x 10-6 |
Com base nesse estudo cinético, é correto afirmar que a constante da equação de velocidade (rapidez) dessa reação (k) apresenta as unidades
Provas
A concentração de nitrato nessa solução é igual a
Provas
A concentração da solução preparada, em quantidade de matéria, é de, aproximadamente,
Provas
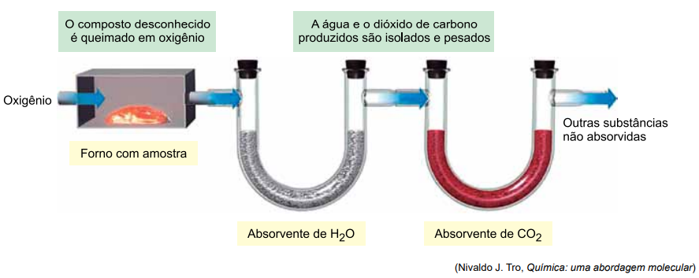
Uma amostra constituída por 2 x 10–2 mols dessa substância foi analisada, e foram formados 8 x 10–2 mols de CO2 e 6 x 10–2 mols de H2O. A quantidade de oxigênio na amostra foi determinada indiretamente e correspondeu à mesma quantidade em mols de hidrogênio na substância.
A massa molar, em gramas, que corresponde a um mol dessa substância é
Provas
O tricloreto de arsênio (AsCl3 ) é preparado por meio da reação apresentada na equação a seguir:
4As2 O3 (s) + 3S2 Cl2 (g) + 9Cl2 (g) → 8AsCl3 (g) + 6SO2 (g)
Ao serem misturados, em condições adequadas para a reação, 2,7 mols de cada um dos reagentes, a quantidade máxima de tricloreto de arsênio que poderá ser formada é igual a
Provas
Caderno Container