Foram encontradas 36.167 questões.
Uma célula galvânica (pilha) é representada pelo diagrama
a seguir, segundo as convenções da IUPAC (União Internacional de Química Pura e Aplicada):
Pt(s)│Cr3+ (aq), Cr2+ (aq)||Cu2+ (aq)│Cu (s)
Nessa célula galvânica, nas condições-padrão,
Pt(s)│Cr3+ (aq), Cr2+ (aq)||Cu2+ (aq)│Cu (s)
Nessa célula galvânica, nas condições-padrão,
Provas
Questão presente nas seguintes provas
A amônia e o oxigênio estabelecem, em compartimento
fechado com pressão de 1 atm e 50 ºC, o equilíbrio reacional representado na equação a seguir:
4 NH3 (g) + 3 O2 (g) ⇄ 2N2 (g) + 6H2 O(l)
Assinale a alternativa que apresenta corretamente a expressão que permite calcular a constante desse equilíbrio (Kc).
4 NH3 (g) + 3 O2 (g) ⇄ 2N2 (g) + 6H2 O(l)
Assinale a alternativa que apresenta corretamente a expressão que permite calcular a constante desse equilíbrio (Kc).
Provas
Questão presente nas seguintes provas
A teoria da ligação de valência (TLV) é um modelo que
explica a formação de ligações químicas entre átomos.
De acordo com essa teoria, os orbitais atômicos do
átomo central formam um conjunto de orbitais híbridos
que participam da ligação química.
No composto BF3, o conjunto de orbitais híbridos formado ao redor do átomo central de B é o
No composto BF3, o conjunto de orbitais híbridos formado ao redor do átomo central de B é o
Provas
Questão presente nas seguintes provas
A figura a seguir representa a fórmula estrutural de uma molécula orgânica:
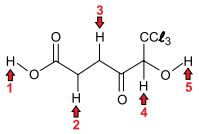
Nessa molécula, o átomo de hidrogênio que apresenta maior caráter ácido é indicado pela seta de número
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
A cassiterita, a bauxita e a hematita são minérios amplamente
explorados no Brasil, desempenhando um papel fundamental
na economia e na indústria nacional. Na metalurgia extrativa,
tecnologias avançadas são empregadas para transformar
esses minerais em materiais de alto valor, utilizando processos como a redução em altos-fornos, nos quais o coque atua
como agente redutor, e a eletrólise, que emprega coque como
eletrodo, essencial para a obtenção de materiais com elevada
pureza. Dessa forma, a exploração e o processamento desses
recursos garantem o abastecimento da indústria nacional e a
exportação para mercados globais.
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
A cassiterita, a bauxita e a hematita são minérios amplamente
explorados no Brasil, desempenhando um papel fundamental
na economia e na indústria nacional. Na metalurgia extrativa,
tecnologias avançadas são empregadas para transformar
esses minerais em materiais de alto valor, utilizando processos como a redução em altos-fornos, nos quais o coque atua
como agente redutor, e a eletrólise, que emprega coque como
eletrodo, essencial para a obtenção de materiais com elevada
pureza. Dessa forma, a exploração e o processamento desses
recursos garantem o abastecimento da indústria nacional e a
exportação para mercados globais.
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
O cobalto-60 é um radioisótopo muito empregado na área
médica e tecnológica. A sua produção é feita em reator nuclear
a partir do bombardeamento de partículas sobre um alvo constituído cobalto-59 de acordo com a reação nuclear representada na equação a seguir:
\({}^{59}_{27}\text{Co} + x \rightarrow {}^{60}_{27}\text{Co}\)
O cobalto-60 emite radiação gama (γ) de alta energia e decai
para o níquel-60 estável com a emissão de uma partícula radioativa conforme a equação a seguir:
\({}^{59}_{27}\text{Co} \rightarrow {}^{60}_{28}\text{Ni} + w + \gamma\)
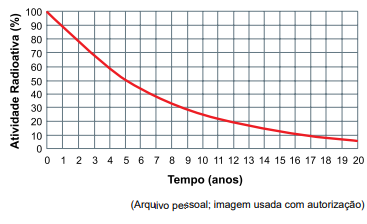
O seguinte gráfico apresenta a curva de decaimento radioativo
de uma fonte radioativa de cobalto-60:
Provas
Questão presente nas seguintes provas
Leia o texto a seguir para responder à questão:
O cobalto-60 é um radioisótopo muito empregado na área
médica e tecnológica. A sua produção é feita em reator nuclear
a partir do bombardeamento de partículas sobre um alvo constituído cobalto-59 de acordo com a reação nuclear representada na equação a seguir:
\({}^{59}_{27}\text{Co} + x \rightarrow {}^{60}_{27}\text{Co}\)
O cobalto-60 emite radiação gama (γ) de alta energia e decai
para o níquel-60 estável com a emissão de uma partícula radioativa conforme a equação a seguir:
\({}^{59}_{27}\text{Co} \rightarrow {}^{60}_{28}\text{Ni} + w + \gamma\)
O seguinte gráfico apresenta a curva de decaimento radioativo
de uma fonte radioativa de cobalto-60:

Provas
Questão presente nas seguintes provas
A hidroxiapatita (Ca10(PO4
)
6
(OH)2
) pode ser obtida
por meio da equação não balanceada representada
a seguir:
Ca(NO3 ) 2 (aq) + KH2 PO4 (aq) + NaOH (aq) →
Ca10(PO4 ) (OH)2 (aq) + KNO3 (aq) + NaNO3 (aq) + H2 O(l)
A soma dos coeficientes estequiométricos dos reagentes da equação balanceada que resulta na formação de 1 mol de hidroxiapatita é igual a
Ca(NO3 ) 2 (aq) + KH2 PO4 (aq) + NaOH (aq) →
Ca10(PO4 ) (OH)2 (aq) + KNO3 (aq) + NaNO3 (aq) + H2 O(l)
A soma dos coeficientes estequiométricos dos reagentes da equação balanceada que resulta na formação de 1 mol de hidroxiapatita é igual a
Provas
Questão presente nas seguintes provas
Uma análise química, realizada em uma mufla com
um cadinho aberto, empregou 6,36 g de uma amostra
constituída de uma mistura anidra de óxido de cálcio
(CaO) e carbonato de sódio (Na2
CO3
, massa molar
de 106,0 g/mol). Após aquecimento até 850 ºC, todo o
carbonato de sódio se decompôs, formando óxido de
sódio sólido e dióxido de carbono (CO2
, massa molar de
44 g/mol) gasoso. O óxido de cálcio não reagiu. Após
resfriamento em dessecador, a massa do conteúdo do
cadinho era de 5,04 g.
O percentual de carbonato de sódio na mistura era igual a
O percentual de carbonato de sódio na mistura era igual a
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container