Foram encontradas 36.167 questões.
Considere uma situação prática de eletrodeposição utilizada em processos industriais para recobrimento metálico, na qual se deseja calcular o tempo necessário para a deposição de uma massa conhecida de zinco sob corrente constante. Sabendo que a constante de Faraday é 9,65x104 C.mol–1, para a deposição de 2,0 mg de zinco metálico, o tempo necessário, em minutos, utilizando corrente de 10 mA, é de, aproximadamente,
Provas
Observe os dados de entalpia de formação (ΔH\( _f^º \)) da tabela a seguir:
| Composto | ΔH\( _f^º \) (kJ.mol–1) |
| C₂H₅OH(\( ℓ \)) | -278 |
| CO₂(g) | -394 |
| H₂O(\( ℓ \)) | -286 |
É correto afirmar que a entalpia padrão da reação de combustão completa do etanol (ΔH\( _f^º \)), em kJ.mol–1, é
Provas
- Sistemas de EquilíbrioSistemas Homogêneos: Solubilidade dos Sais, Hidrólise dos Sais e Curvas de Titulação.
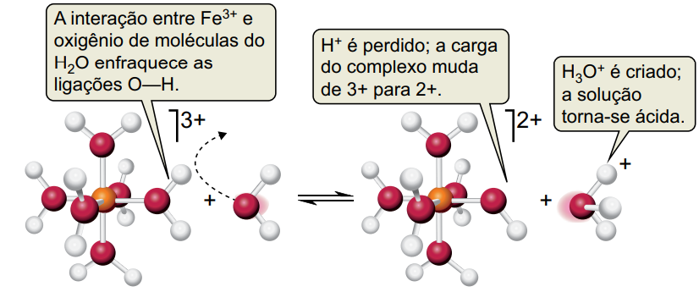
Considere a figura que mostra o mecanismo da reação de íons metálicos hidratados com a água, o exemplo é para o íon [Fe(H2O)6]3+, e a tabela de constantes de acidez (Ka) para cátions metálicos em solução aquosa, a 25 °C a seguir:
Figura
Tabela
| cátion | Ka |
|---|---|
| Zn2+ | 2,5x10–10 |
| Ni2+ | 2,5x10–11 |
| Cr2+ | 1,6x10–4 |
(Brown, T. L.; LeMay Jr, H. E.; Bursten, B. E.; Burdge, J. R. Química, a ciência central, 2005)
De acordo com a tabela e o mecanismo apresentado na figura, conclui-se que os íons metálicos hidratados se comportam como __________ e a solução que apresenta maior pH é a que contém os íons hidratados __________.
As lacunas são preenchidas, correta e respectivamente, por:
Provas
Analise as eletronegatividades dos elementos a seguir:
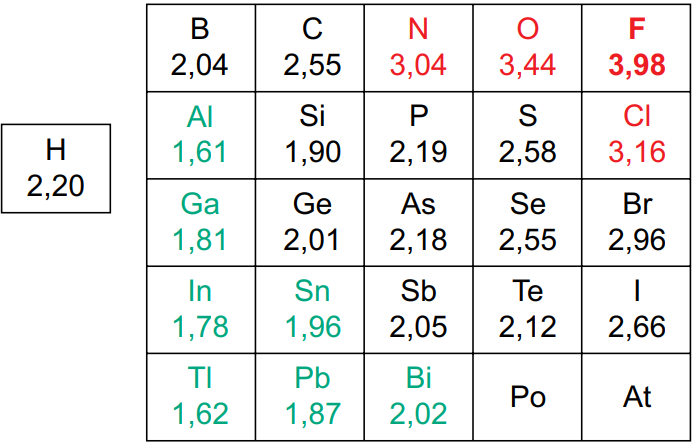
Nesse contexto, a menor polaridade ocorre para a ligação química do elemento hidrogênio com o elemento
Provas
Observe o esquema a seguir que representa a obtenção de um aldeído partindo do metilbenzeno:
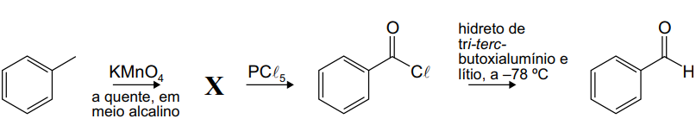
Nesse esquema, X possui a função orgânica
Provas
Observe a imagem a seguir:
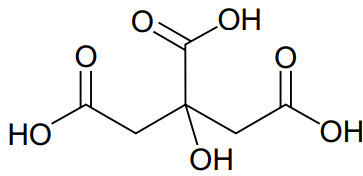
Ácido cítrico
Considerando que na formulação de 200 g de um xampu foi utilizado 0,5%, em massa, de ácido cítrico (M = 192 g.mol–1), o volume mínimo, em mL, de NaOH 0,10 mol.L–1 que deve ser utilizado para neutralizar completamente o ácido cítrico contido em 10,0 g de xampu é de, aproximadamente,
Provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Ácido clorídrico pró-análise possui concentração de 36,5% em massa e densidade 1,20 g.cm–3. Para preparar 1,0 L de solução diluída de ácido clorídrico, HC\( ℓ \), de concentração 1,0 mol.L–1, deve ser utilizado o volume do ácido pró-análise de, aproximadamente,
Provas
Para determinar a pureza em carbonato de cálcio, CaCO₃, no mineral calcita, uma amostra de 2,00 g desse mineral foi submetida a aquecimento para decomposição do carbonato de cálcio. O resíduo da decomposição da amostra apresentou massa igual a 1,34 g. Considerando que a impureza da amostra não se decompôs nas condições do aquecimento e que todo o carbonato de cálcio da amostra se transformou em CaO e CO₂, o percentual de carbonato de cálcio nessa amostra de calcita era igual a
Provas
A aviação é responsável por aproximadamente 2% de todas as emissões globais de dióxido de carbono (CO₂), liberando 880 milhões de toneladas desse gás na atmosfera todos os anos. Considerando que o volume molar de qualquer gás nas condições ambientais de temperatura e pressão (CATP) é 25 L.mol–1, o volume, em m3, de CO₂ que corresponde à quantidade liberada anualmente pela aviação, nas CATP, é de, aproximadamente,
Provas
Considere o texto e a figura a seguir:
As células solares de hoje, feitas de silício, ainda geram resíduos, mas as da próxima geração tecnológica, com outro mineral, a perovskita (CaTiO3 ), talvez sejam totalmente recicláveis. Em laboratório, após repetidos processos de reciclagem, os dispositivos mostraram eficiência e estabilidade semelhantes à dos novos.
(Disponível em: https://revistapesquisa.fapesp.br/celulas-solares-reciclaveis/)
Esta figura representa a célula unitária da perovskita, que contém uma fórmula unitária:
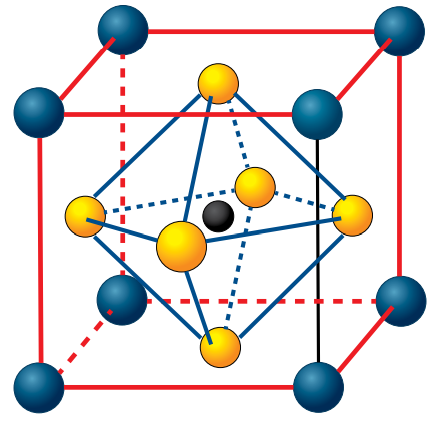
(Disponível em: https://www.electricalelibrary.com/2024/11/21/perovskita-o-novo-material-da-energia-solar/)
Considerando as informações apresentadas, é correto afirmar que o número de oxidação do titânio na perovskita e a posição que o oxigênio ocupa na sua célula unitária são
Provas
Caderno Container