Foram encontradas 36.167 questões.
O fenol (C6H5OH) é um ácido fraco que apresenta pKa = 10. Ao interagir com a água estabelece o equilíbrio representado na equação:
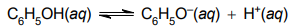
O valor do pH de uma solução aquosa de fenol com concentração 0,01 mol/L e a força intermolecular mais intensa que a molécula de fenol apresenta com a água são:
O valor do pH de uma solução aquosa de fenol com concentração 0,01 mol/L e a força intermolecular mais intensa que a molécula de fenol apresenta com a água são:
Provas
Questão presente nas seguintes provas
Os metais ferro, alumínio e estanho são obtidos a partir de diferentes minérios e métodos de produção.
Assinale a alternativa que apresenta a associação correta entre metal, minério e método de produção.
Assinale a alternativa que apresenta a associação correta entre metal, minério e método de produção.
Provas
Questão presente nas seguintes provas
O íon dicromato 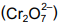 reage com o íon sulfito
reage com o íon sulfito 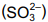 em meio ácido, formando íons crômio (III) e íons sulfato
em meio ácido, formando íons crômio (III) e íons sulfato 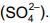
Na reação global, para cada 1 mol de íons dicromato, a quantidade em mol de íons H+ que participam é igual a
Na reação global, para cada 1 mol de íons dicromato, a quantidade em mol de íons H+ que participam é igual a
Provas
Questão presente nas seguintes provas
A figura representa a célula unitária de um composto cristalino, que apresenta a estrutura típica da Perovskita.
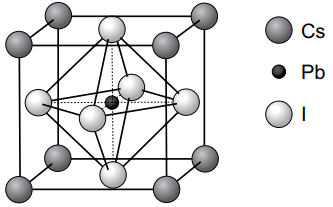
(https://pt.dsisolar.com/info/introduction-to-perovskite-solar-cell-63415141.html Adaptado)
Esse composto é um sólido __________ e tem fórmula unitária ___________.
As lacunas são preenchidas, correta e respectivamente, por

(https://pt.dsisolar.com/info/introduction-to-perovskite-solar-cell-63415141.html Adaptado)
Esse composto é um sólido __________ e tem fórmula unitária ___________.
As lacunas são preenchidas, correta e respectivamente, por
Provas
Questão presente nas seguintes provas
O nitrogênio forma diversos óxidos que interagem na atmosfera de forma variada. A seguir são dadas as equações termoquímicas envolvendo espécies nitrogenadas.

A variação da entalpia da reação 4 é igual a

A variação da entalpia da reação 4 é igual a
Provas
Questão presente nas seguintes provas
Na combustão de 0,01 mol de um composto orgânico constituído apenas por carbono, hidrogênio e oxigênio foram formados 0,12 mol de CO2 e 0,08 mol de H2O. Descobriu-se, por meio de outras técnicas analíticas, que a massa de oxigênio nesse composto corresponde ao dobro de massa de hidrogênio que ele contém.
A fórmula mínima desse composto é
A fórmula mínima desse composto é
Provas
Questão presente nas seguintes provas
A figura representa, esquematicamente, o poder de penetração das três principais emissões radioativas naturais em três diferentes materiais. 1 2 3 papel aço chumbo
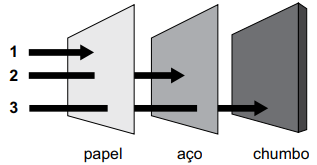
(Arquivo pessoal; imagem usada com autorização)
As emissões radioativas 1, 2 e 3 são, respectivamente,

(Arquivo pessoal; imagem usada com autorização)
As emissões radioativas 1, 2 e 3 são, respectivamente,
Provas
Questão presente nas seguintes provas
A molécula de oxigênio (O2) apresenta comportamento paramagnético, sendo atraída por campos magnéticos, o que indica a presença de elétrons desemparelhados em sua estrutura.
A explicação para o comportamento paramagnético da molécula de oxigênio é dada pela teoria
A explicação para o comportamento paramagnético da molécula de oxigênio é dada pela teoria
Provas
Questão presente nas seguintes provas
A figura representa um diagrama das entalpias envolvidas na formação de uma solução aquosa a partir de um soluto sólido iônico cristalino.
A entalpia de solução (∆Hsol) é o resultado da soma da entalpia de rede cristalina (∆HL) e a entalpia de hidratação (∆Hhid)
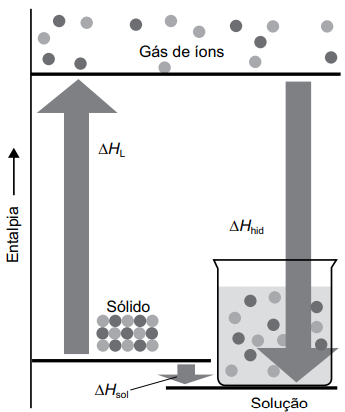
(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
A tabela apresenta os valores, em módulo, de entalpia de rede (∆HL) e entalpia de hidratação (ΔHhid) de alguns sais.
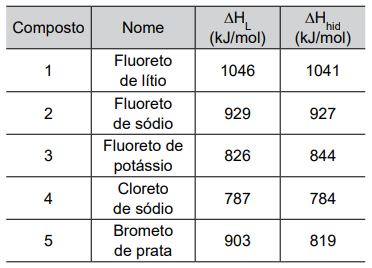
(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
O diagrama de energia da figura é compatível ao processo de dissolução do composto
A entalpia de solução (∆Hsol) é o resultado da soma da entalpia de rede cristalina (∆HL) e a entalpia de hidratação (∆Hhid)

(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
A tabela apresenta os valores, em módulo, de entalpia de rede (∆HL) e entalpia de hidratação (ΔHhid) de alguns sais.

(ATKINS, Peter; LORETTA, Jones, LAVERMAN, Leroy. Princípios de Química: questionando a vida moderna e o meio Ambiente. 2. ed. Porto Alegre: Bookman, 2006)
O diagrama de energia da figura é compatível ao processo de dissolução do composto
Provas
Questão presente nas seguintes provas
A Teoria da Repulsão dos Pares de Elétrons da Camada de Valência (Valence Shell Electron Pair Repulsion ou VSEPR) é utilizada para prever a geometria molecular com base na repulsão entre pares de elétrons ao redor do átomo central.
A representação AX3E2 (em que E representa par de elétrons não ligados) corresponde a uma molécula polar com formato de T, e um exemplo dessa molécula é:
A representação AX3E2 (em que E representa par de elétrons não ligados) corresponde a uma molécula polar com formato de T, e um exemplo dessa molécula é:
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container