Foram encontradas 35.978 questões.
No século V a.C., o filósofo grego Empédocles afirmou
que tudo era formado por quatro elementos: água, terra,
fogo e ar. Já Leucipo e Demócrito defendiam que a
matéria era composta por partículas indivisíveis
chamadas átomos. Com o avanço da ciência e da
experimentação, estudiosos como Torricelli e Boyle
ampliaram esse conhecimento. No início do século XIX,
John Dalton retomou as ideias de Demócrito e Leucipo e
propôs um modelo atômico para explicar a constituição
da matéria.
Fonte: Usberco, João; Philippe Spitaleri. Identidade Saraiva: Química:
área de Ciências da Natureza e suas Tecnologias: volume único:
Ensino médio. 1. ed. São Paulo: Saraiva, 2024.
De acordo com o modelo atômico proposto por Dalton,
julgue os itens a seguir como Verdadeiros (V) ou Falsos
(F):
(__)Toda matéria é constituída por átomos, definidos como esferas rígidas e divisíveis que podem ser criadas e destruídas.
(__)A combinação de átomos nem sempre ocorre em uma proporção de números inteiros, originando substâncias diferentes.
(__)Os átomos de diferentes elementos químicos apresentam propriedades distintas.
Assinale a alternativa com a sequência CORRETA de cima para baixo.
(__)Toda matéria é constituída por átomos, definidos como esferas rígidas e divisíveis que podem ser criadas e destruídas.
(__)A combinação de átomos nem sempre ocorre em uma proporção de números inteiros, originando substâncias diferentes.
(__)Os átomos de diferentes elementos químicos apresentam propriedades distintas.
Assinale a alternativa com a sequência CORRETA de cima para baixo.
Provas
Questão presente nas seguintes provas
Os polímeros são substâncias macromoleculares que podem ser produzidas pela natureza (madeira, óleo lubrificante, cortiça, etc.) ou podem ser obtidos artificialmente pela união sequenciada de pequenas moléculas, chamadas monômeros. Existem quatro grupos distintos:
I. Termorrígidos.
II. Termoplásticos.
III. Elastômeros.
IV. Elastômeros-Termostáticos.
Quantos dos itens está(ão) CORRETO(S)?
Provas
Questão presente nas seguintes provas
Os ácidos podem ser classificados como hidrácidos, que
são aqueles que não possuem oxigênio na molécula, e
os oxiácidos são aqueles que possuem oxigênio na
molécula. Uma das características dos ácidos é a de
reagirem com os carbonatos e bicarbonatos, produzindo
efervescência em virtude do desprendimento de:
Provas
Questão presente nas seguintes provas
Titulação volumétrica é o processo de adição de
volumes discretos de um reagente, geralmente com o
auxílio de uma bureta, para quantificar o analito na
amostra.
As afirmativas I, II, III e IV relacionam-se com as
características e uso das buretas.
I. Consistem de um tubo cilíndrico uniformemente calibrado em toda sua extensão de escala e possuem uma torneira na sua extremidade inferior.
II. A lubrificação dificulta o manuseio de buretas cujas torneiras são de vidro esmerilhado.
III. Recomenda-se verificar a presença de bolhas de ar retidas no seu interior, antes de iniciar a análise.
IV. A leitura do menisco é feita de forma relativa, sempre considerando a parte inferior do menisco.
Assinale a alternativa em que (todas) a(s) afirmativa(s) está(ão) CORRETA(S):
I. Consistem de um tubo cilíndrico uniformemente calibrado em toda sua extensão de escala e possuem uma torneira na sua extremidade inferior.
II. A lubrificação dificulta o manuseio de buretas cujas torneiras são de vidro esmerilhado.
III. Recomenda-se verificar a presença de bolhas de ar retidas no seu interior, antes de iniciar a análise.
IV. A leitura do menisco é feita de forma relativa, sempre considerando a parte inferior do menisco.
Assinale a alternativa em que (todas) a(s) afirmativa(s) está(ão) CORRETA(S):
Provas
Questão presente nas seguintes provas
Considere que um técnico em química preparou uma
solução de NaOH 0,100 mol/L e padronizou-a utilizando o
biftalato de potássio (KHC8H4O4) e fenolftaleína como
indicador. Na Tabela a seguir encontram-se as medidas de
massa de biftalato de potássio e as medidas de volume
gasto de NaOH 0,100 mol/L, obtidas pelo técnico, para a
triplicata de análise.

Dados: equação da reação: NaOH(aq) + HOOCC6H4COOK(aq) → NaOOCC6H4COOK(aq) + H2O(liq) NaOH = 40,00 g/mol; KHC8H4O4 = 204, 2 g/mol
Considerando a análise realizada, assinale a alternativa que apresenta a concentração média (C) da solução de NaOH, o seu fator de correção (FC), o titulado e o titulante, respectivamente.

Dados: equação da reação: NaOH(aq) + HOOCC6H4COOK(aq) → NaOOCC6H4COOK(aq) + H2O(liq) NaOH = 40,00 g/mol; KHC8H4O4 = 204, 2 g/mol
Considerando a análise realizada, assinale a alternativa que apresenta a concentração média (C) da solução de NaOH, o seu fator de correção (FC), o titulado e o titulante, respectivamente.
Provas
Questão presente nas seguintes provas
Na Titulação de Neutralização são utilizadas
substâncias indicadoras que sinalizam o ponto final da
análise, em função da mudança da cor devida à mudança
de pH do meio. Sobre os indicadores assinale a alternativa
CORRETA:
Provas
Questão presente nas seguintes provas
Ao medirmos o pH de uma solução salina, em muitos
casos não encontraremos o valor “neutro” (pH = 7,0), e sim
valores de pH< 7,0 ou pH>7. Este comportamento pode ser
explicado pela Teoria ácido-base de Bronsted-Löwry que
afirma que o íon pode ser um ácido ou uma base. Durante
uma aula experimental de química, o professor pediu para
que os alunos preparassem 5 soluções salinas, de
concentração 0,100 mol/L, utilizando água destilada e
cada um dos sais a seguir.
I. Iodeto de sódio
II. Brometo de amônio
III. Cianeto de potássio
IV. Fluoreto de amônio
V. Acetato de metilamônio
Dados: Constantes de Acidez e de Basicidade em temperatura igual 25 °C:

Assinale a alternativa que apresenta os sais que produzirão soluções com valores de pH<7.
I. Iodeto de sódio
II. Brometo de amônio
III. Cianeto de potássio
IV. Fluoreto de amônio
V. Acetato de metilamônio
Dados: Constantes de Acidez e de Basicidade em temperatura igual 25 °C:

Assinale a alternativa que apresenta os sais que produzirão soluções com valores de pH<7.
Provas
Questão presente nas seguintes provas
Em 1909 Fritz Haber e seu assistente Robert Le
Rossignol demonstraram seu processo de produzir amônia
a partir de nitrogênio do ar e prover, desse modo, uma
fonte abundante de compostos para a agricultura e para os
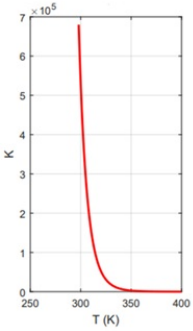
armamentos. O gráfico a seguir relaciona a temperatura
(em Kelvin) com os valores da constante de equilíbrio (K)
para a reação de síntese de amônia.
N2(g) + 3 H2(g) ⇆ 2 NH3(g)
Leia as afirmativas a seguir:
I- A produção de amônia será reduzida com o aumento da temperatura.
II- A reação é endotérmica no sentido direto da reação.
III- A constante de equilíbrio em termos de pressões parciais é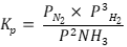
IV- A velocidade da reação será aumentada com o aumento da temperatura.
V- A adição de mais N à reação desloca o equilíbrio para a direita, produzindo mais amônia.
É CORRETO o que se afirma em:
N2(g) + 3 H2(g) ⇆ 2 NH3(g)

Leia as afirmativas a seguir:
I- A produção de amônia será reduzida com o aumento da temperatura.
II- A reação é endotérmica no sentido direto da reação.
III- A constante de equilíbrio em termos de pressões parciais é
IV- A velocidade da reação será aumentada com o aumento da temperatura.
V- A adição de mais N à reação desloca o equilíbrio para a direita, produzindo mais amônia.
É CORRETO o que se afirma em:
Provas
Questão presente nas seguintes provas
Após a filtração, um precipitado gravimétrico é
aquecido até que sua massa se torne constante. Esse
procedimento remove o solvente e qualquer espécie volátil
arrastada com o precipitado. Em algumas situações os
precipitados também são calcinados para decompor o
sólido e para formar um composto de composição
conhecida.
Fonte: SKOOG, D.; WEST, D.; HOLLER, F. J. e CROUCH, S. Fundamentos de Química Analítica. Tradução da 9. ed. Norte-Americana. São Paulo: Cengage Learning, 2014.
Sobre os processos de secagem e calcinação, podemos afirmar, exceto:
Fonte: SKOOG, D.; WEST, D.; HOLLER, F. J. e CROUCH, S. Fundamentos de Química Analítica. Tradução da 9. ed. Norte-Americana. São Paulo: Cengage Learning, 2014.
Sobre os processos de secagem e calcinação, podemos afirmar, exceto:
Provas
Questão presente nas seguintes provas
É possível determinar níquel (Ni) com dimetilglioxima
(DMG) em amostras de sal através da precipitação do
níquel como um complexo vermelho-alaranjado de DMG,
que é então filtrado, seco e pesado. Considere que um
analista pesou uma massa de 0,2930 g de uma amostra de
sal. Na etapa de filtração foi utilizado um papel de filtro
faixa preta de massa igual a 0,8787 g. Após as etapas de
filtração, lavagem e secagem, a massa medida do papel
de filtro foi igual a 1,1676 g.
Qual é a porcentagem de Ni na amostra?
Dados: dimetilglioximato de níquel - Ni[C4H6(NOH)(NO)]2 = 288,9 g/mol, Ni - 58,6 g/mol.
Qual é a porcentagem de Ni na amostra?
Dados: dimetilglioximato de níquel - Ni[C4H6(NOH)(NO)]2 = 288,9 g/mol, Ni - 58,6 g/mol.
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container