Foram encontradas 13.432 questões.
Uma amostra de 25 mL de ácido acético comercial será titulada com solução padronizada de NaOH. A tabela a seguir reúne dados sobre alguns indicadores disponíveis no laboratório:
|
Indicador |
pH Faixa de viragem | Cor forma ácida |
Cor Forma básica |
|
Vermelho congo |
3,0 – 5,2 | azul |
alaranjado |
|
Alaranjado de metila |
4,4 – 6,2 | vermelho |
amarelo |
|
Azul de bromotimol |
6,0 – 7,6 | amarelo |
azul |
|
Fenolftaleína |
8,0 – 9,6 | Incolor |
vermelho |
|
Azul de timol |
8,0 – 9,6 | Incolor |
azul |
Sabendo que o pH do ponto de equivalência nesse tipo de titulação é 9,2, pode-se afirmar que os indicadores recomendados são
Provas
Um técnico precisa de uma pequena quantidade de clorofórmio isento de etanol para uso em procedimentos analíticos.
Ele dispõe de clorofórmio puro, que contém 1% de etanol como conservante. O clorofórmio HCCl3 é um líquido incolor, não inflamável, que ferve a 61-62 °C (1 atm). A solubilidade do clorofórmio em água a 25 °C é de 1: 200 (v/v) CHCl3:H2O.
Com base nessas informações, o técnico purificou 100 mL do solvente usando o seguinte processo:
1. lavagem com água, em funil de separação, para remoção do etanol;
2. transferência do solvente para um frasco de vidro escuro, boca estreita, seguida de adição de 20 g/100 mL de cloreto de cálcio anidro, para secagem;
3. após 24 horas, filtração simples, seguida de destilação. Os primeiros 10 mL destilados foram desprezados.
Na aplicação dessa metodologia, foram utilizados os seguintes processos físicos:
Provas
Considere o seguinte sistema reacional:
CH4(g) + H2O(!$ l !$) !$ \rightleftarrows !$ CO(g) + 3H2 (g) !$ \Delta !$H = 192,3kJ
Nesse sistema reacional, a concentração dos produtos diminui mediante
Provas
Para determinar a concentração de uma base em uma solução problema, um técnico titulou 4 amostras dessa solução com ácido e registrou os volumes de ácido necessários para a neutralização, conforme indicado na tabela a seguir:
|
Amostra n.º |
Volume de ácido (mL) |
| 1 | 19,6 |
| 2 | 19,5 |
| 3 | 19,3 |
| 4 | 19,3 |
Para efetuar corretamente o cálculo da concentração da base na solução problema, o volume de ácido que o técnico deve utilizar é igual a
Provas
Utilizando métodos oficiais de análise de águas, um analista determinou as características físico-químicas e a composição química de uma amostra de água mineral e obteve os seguintes resultados:
Características Físico-Químicas: pH a 25 ºC: 5,45 – Temperatura da água na fonte: 21,5 ºC – Condutividade elétrica a 25 ºC: 455!$ \mu !$S/cm – Resíduo de evaporação a 180 ºC: 297,1 mg/L – Gás Carbônico: 2.182,4 mg/L.
Composição química (mg/mL): Bicarbonato: 258,88, – Potássio: 30,52 – Sódio: 30,17 – Cálcio: 26,49 – Magnésio: 11,21 – Sulfato: 2,42 – Cloreto: 1,38 – Nitrato: 0,91 – Bário: 0,35 – Fluoreto: 0,11 – Lítio: 0,028.
Com base nessas informações, é correto afirmar que o analista deverá classificar a amostra analisada como uma água
Provas
A qualidade do ar atmosférico é acompanhada pela comparação da concentração de poluentes com os limites máximos estabelecidos pelo IBAMA por meio da Resolução CONAMA n.º 03 de 28.06.90. São considerados os seguintes poluentes: partículas totais em suspensão, partículas inaláveis, fumaça, SO2, NO2, CO e O3.
Sobre as substâncias químicas identificadas no texto, é correto afirmar que
Provas
A cafeína é considerada um indicador da qualidade dos mananciais e do tratamento de água. A sua presença alerta para a contaminação por esgoto e, portanto, para a presença de outros contaminantes químicos na água.
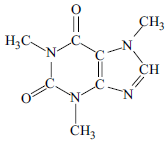
(http://cienciahoje.uol.com.br. Acesso em 10 de janeiro 2013. Adaptado)
Um dos métodos utilizados na quantificação da cafeína se baseia na absorção de radiação eletromagnética na região do ultravioleta (UV). A cafeína apresenta um máximo de absorção no UV entre os comprimentos de onda de 271 e 275 nm.
Essa absorção deve-se à presença, na molécula de cafeína, de
Provas
O reservatório de água de um edifício foi desinfetado com cloro. Depois da desinfecção, verificou-se que a água armazenada no tanque continha 15 mg/L de cloro ativo residual. Para reduzir essa quantidade a 5 mg/L, foi providenciada uma decloração da água do tanque, com bissulfito de sódio, segundo a reação descrita a seguir:
NaHSO3 + Cl2 + H2O !$ \rightarrow !$ NaHSO4 + 2HCl
Para se obter a redução da concentração de cloro ativo residual até o valor definido, a quantidade mínima de NaHSO3 consumida será igual a
Provas
O reservatório de água de um edifício foi desinfetado com cloro. Depois da desinfecção, verificou-se que a água armazenada no tanque continha 15 mg/L de cloro ativo residual. Para reduzir essa quantidade a 5 mg/L, foi providenciada uma decloração da água do tanque, com bissulfito de sódio, segundo a reação descrita a seguir:
NaHSO3 + Cl2 + H2O !$ \rightarrow !$ NaHSO4 + 2HCl
Sobre a reação de decloração, é correto afirmar que é um processo em que o
Provas
Para preparar uma solução de KCl, um técnico pesou 74,45 g do sal e transferiu para um balão volumétrico de 1L. Adicionou água para garantir a dissolução e em seguida completou o volume para 1L.
Ao terminar a preparação, o nível de líquido no balão apresentou-se como mostrado na figura a seguir:

Nessas condições, é correto afirmar que a concentração da solução que o técnico preparou é
Provas
Caderno Container