Foram encontradas 13.432 questões.
A respeito dos materiais para a indústria química, julgue o item a seguir.
O aço inoxidável apresenta pouca resistência à formação de incrustações e, por isso, não é utilizado em tubos para troca de calor, visto que os trocadores de calor perderiam a eficiência.
Provas
Julgue o item a seguir, acerca de águas industriais e potáveis.
A adsorção com carvão ativado e a filtração rápida constituem tecnologias eficientes para a remoção de sólidos dissolvidos das águas para consumo humano e industriais.
Provas
Julgue o item a seguir, acerca de águas industriais e potáveis.
Os íons de metais pesados dissolvidos na água podem ser removidos por precipitação química com hidróxidos seguida de floculação e filtração.
Provas
Julgue o item a seguir, acerca de águas industriais e potáveis.
O tratamento de água para abastecimento público em ciclo completo consiste no processo de coagulação/floculação da água seguido de filtração rápida e desinfecção da água filtrada.
Provas
Julgue o item a seguir, acerca de águas industriais e potáveis.
O processo de coagulação química, uma das etapas do tratamento de águas para abastecimento público em ciclo completo, consiste na agregação, por meio de agitação, das partículas coloidais presentes na água, o que facilita a remoção dessas partículas pelos processos de sedimentação ou de flotação.
Provas
Julgue o item a seguir, acerca de águas industriais e potáveis.
O processo de coagulação/floculação, seguido de flotação por ar dissolvido, pode ser utilizado no tratamento de águas naturais com presença de algas e de águas com baixa turbidez e elevada cor.
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
Se for realizada a volume constante, a reação de decomposição do N2O4(g) a N2O(g) absorverá mais calor do que se for realizada a pressão constante.
Provas
O N2O4, muito utilizado como propelente de foguetes, pode ser produzido a partir da oxidação catalítica da amônia. Na fase gasosa, ele estabelece o seguinte equilíbrio:
N2O4(g) + calor \( \rightleftharpoons \) 2NO2(g)
Considere que a reação de decomposição do N2O4(g) a N2O(g) obedeça a uma cinética de primeira ordem; que as entropias padrão molares do N2O4(g) e do N2O(g), a 25 ºC, sejam iguais a \( 304 \ J⋅ mol^{-1} ⋅ K^{-1} \) e \( 240 \ J ⋅ mol^{-1} ⋅ K^{-1} \), respectivamente; que, na temperatura \( T \), a constante de equilíbrio para a reação acima apresentada seja igual a 5,0; e que os gases apresentem comportamento ideal. Nessas condições, julgue o item a seguir.
Durante a oxidação catalítica da amônia, o papel do catalisador é o de aumentar a taxa de colisão entre as moléculas dos reagentes, o que eleva a taxa de formação dos produtos.
Provas
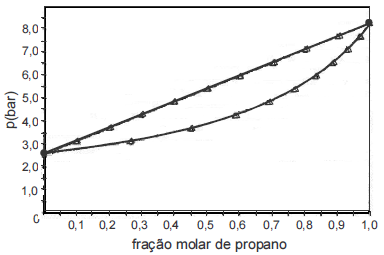
Considere que a figura acima represente o diagrama pressão-composição para a mistura propano-butano na temperatura de 293 K. Considere, ainda, que o propano e o butano formem uma mistura ideal e que o GLP apresente frações molares de butano e propano iguais a 0,30 e 0,70, respectivamente. A partir dessas informações, julgue o item a seguir.
No GLP sob pressão de 2,0 bar e temperatura de 20 ºC, as pressões parciais do butano e do propano são iguais a 0,6 bar e 1,4 bar, respectivamente.
Provas

Considere que a figura acima represente o diagrama pressão-composição para a mistura propano-butano na temperatura de 293 K. Considere, ainda, que o propano e o butano formem uma mistura ideal e que o GLP apresente frações molares de butano e propano iguais a 0,30 e 0,70, respectivamente. A partir dessas informações, julgue o item a seguir.
À temperatura de 20 ºC e sob pressão de 6,0 bar, uma mistura com a composição global do GLP apresentará duas fases: fase líquida, com fração molar de propano inferior a 0,70, e fase gasosa, com fração molar de propano superior a 0,70.
Provas
Caderno Container