Foram encontradas 40 questões.
Uma amostra de 100,0 mL de água salobra foi alcalinizada com amoníaco, e o sulfeto nela contido foi titulado com solução de AgNO3 0,0200 mol/L, resultando em um consumo de 15,00 mL.
Considerando a massa molar do H2S igual a 34,8 g/mol, a concentração de H2S na água salobra, em mg/L, equivale a:
Provas
A amostra de uma liga de massa igual a 0,2500 g foi digerida com água régia e, depois, avolumada a 25,00 mL.
Essa solução passou pela seguinte sequência de tratamento:
| - retirada de uma alíquota de 1,00 mL; |
Após esse tratamento, a solução final possui a concentração de 5,0 mg/L de níquel.
Com base nesses dados, o teor de níquel na liga corresponde a:
Provas
Nos gráficos abaixo, observam-se curvas de titulação de soluções aquosas.
A titulação de uma solução com mais de um soluto está representada em:
Provas
O erro indeterminado é também conhecido como:
Provas
Uma solução aquosa foi preparada pela dissolução de NaHCO3 e Na2CO3 puros e, em seguida, foi titulada com ácido forte. Observe a curva resultante da titulação.
Curva de Titulação

A análise da curva permite fazer a seguinte afirmação:
Provas
Um técnico, ao dosar uma amostra de persulfato de potássio, procedeu da seguinte maneira:
- pesou 5,406 g da amostra de persulfato de potássio (K2S2O8);
- dissolveu a amostra em água destilada, diluindo-se 500,0 mL em balão volumétrico;
- pipetou 50,00 mL da solução resultante para um frasco de Erlenmeyer, acrescentando-lhe 25,00 mL de ácido oxálico (H2C2O4) 0,0500 mol/L;
- titulou o excesso de ácido oxálico com solução de KMnO4 0,02000 mol/L.
Considere as seguintes informações:
| • S2O8 = + C2O4 !$ \rightleftarrows !$ 2 CO2 + 2 SO4 = |
Se o volume gasto na titulação foi igual a 15,00 mL, a percentagem mássica de persulfato na amostra corresponde a:
Provas
O valor real da concentração de uma solução é 0,100 mol/L; em sua determinação, porém, o resultado encontrado foi igual a 0,101 mol/L.
O erro absoluto e o percentual do erro relativo do resultado são, respectivamente:
Provas
Considere a tabela de indicadores ácido-base e a curva de titulação de um ácido diprótico, H2A, por solução de NaOH, mostradas abaixo:
| Indicador | Faixa de transição de pH | Mudança de cor |
| azul de timol | 1,2 – 2,8 | vermelho – amarelo |
| amarelo de metila | 2,9 – 4,0 | vermelho – amarelo |
| alaranjado de metila | 3,1 – 4,4 | vermelho – laranja |
| verde de bromocresol | 3,8 – 5,4 | amarelo – azul |
| vermelho de metila | 4,2 – 6,3 | vermelho – amarelo |
| púrpura de bromocresol | 5,2 – 6,8 | amarelo – púrpura |
| azul de bromotimol | 6,2 – 7,6 | amarelo – azul |
| vermelho de fenol | 6,8 – 8,4 | amarelo – vermelho |
| púrpura de cresol | 7,6 – 9,2 | amarelo – púrpura |
| fenolftaleína | 8,3 – 10,0 | incolor – vermelho |
| timolftaleína | 9,3 – 10,5 | incolor – azul |
| amarelo de alizarina GG | 10 – 12 | incolor – amarelo |
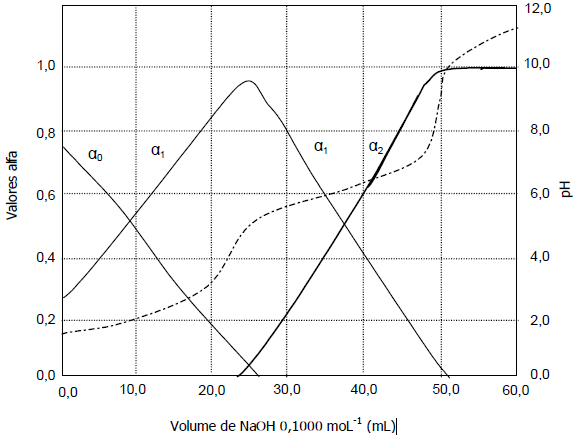
O indicador mais adequado para a determinação do primeiro ponto final da titulação é:
Provas
A solução obtida pela mistura de 300 mL de água com 200 mL de NaOH 0,0250 mol/L tem pH igual a:
Provas
Em uma balança analítica eletrônica, o desvio-padrão de uma simples medida de massa é de ± 0,0001 g.
Ao fazer uma medição com essa balança, usando o método da diferença, o desvio- padrão da medida de determinadasubstância, em gramas, corresponde a:
Provas
Caderno Container