Foram encontradas 250 questões.
A determinação de saliva em pele humana é um dado importante para a análise forense. Se for possível identificar a presença de saliva em alguma região da pele de um indivíduo, isso pode levar a uma análise de DNA e à identificação da pessoa que deixou os traços de saliva. A espectroscopia de fluorescência pode ser usada com vantagens na detecção de saliva seca em pele, pois é um método rápido e não-destrutivo. Basicamente, o método constitui-se na remoção da saliva seca do local com uma escova apropriada e a dissolução da mesma em solução de KC•. Em seguida, registra-se um espectro de emissão com excitação em 282 nm de uma amostra-controle (pele molhada apenas com água, depois seca e raspada) e outro da amostra suspeita de conter saliva. Um pico de emissão entre 345 nm e 355 nm, com intensidade significativamente superior ao controle (cerca de 98% acima), é uma forte indicação da presença de saliva. O perfil de fluorescência da saliva é muito semelhante ao obtido para soluções aquosas puras de amilase e triptofano.
Com relação à técnica descrita no texto, julgue os itens subseqüentes.O método utilizado na detecção, descrito acima, é um processo que envolve dois fótons, sendo o comprimento de onda do fóton absorvido menor que o do fóton emitido.
Provas
Níveis de confiança para alguns valores de z
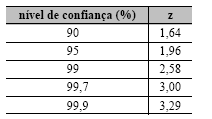
Para 95% de nível de confiança, a faixa de tolerância para as amostras I e II corresponde a uma precisão na medida da ordem de 0,1%, a metade da precisão inserida na especificação da norma pertinente.
Provas
Níveis de confiança para alguns valores de z

Provas
Níveis de confiança para alguns valores de z

Provas

A partir do quadro acima, no qual são mostradas as regiões espectrais em que fontes de excitação, seletores de comprimento de onda (monocromadores), materiais ópticos e detectores podem ser utilizados, julgue os itens que se seguem.
Para se determinarem teores de arsênio por espectroscopia de emissão atômica, o instrumento adequado deve estar equipado com uma lâmpada de catodo oco, como fonte de excitação, uma rede de difração de 2.500 linhas/mm, como seletor de comprimento de onda, e uma fotomultiplicadora, como detector.
Provas

A partir do quadro acima, no qual são mostradas as regiões espectrais em que fontes de excitação, seletores de comprimento de onda (monocromadores), materiais ópticos e detectores podem ser utilizados, julgue os itens que se seguem.
Para a determinação rotineira de nitrobenzeno em amostras de ar, tendo por base a sua absorção em 11,8 • m, poder-se-ia usar um interferômetro equipado com um beam splitter de KBr e um fotodiodo de silício, como detector.
Provas

A partir do quadro acima, no qual são mostradas as regiões espectrais em que fontes de excitação, seletores de comprimento de onda (monocromadores), materiais ópticos e detectores podem ser utilizados, julgue os itens que se seguem.
Um sistema portátil para a determinação de ferro em água natural, baseando-se em medidas de absorção do complexo vermelho Fe(SCN)2+, poderia ser constituído por: uma lâmpada de tungstênio, como fonte de excitação; um filtro de interferência, como seletor de comprimento de onda; e uma fotomultiplicadora, como detector.
Provas

A partir do quadro acima, no qual são mostradas as regiões espectrais em que fontes de excitação, seletores de comprimento de onda (monocromadores), materiais ópticos e detectores podem ser utilizados, julgue os itens que se seguem.
Para a análise de etanol em bebidas alcoólicas por espectroscopia no infravermelho próximo (IV-próximo) por transformada de Fourier, pode-se usar um beam splitter (divisor de feixes) de quartzo e um fotodiodo de germânio como detector.
Provas

A partir do quadro acima, no qual são mostradas as regiões espectrais em que fontes de excitação, seletores de comprimento de onda (monocromadores), materiais ópticos e detectores podem ser utilizados, julgue os itens que se seguem.
Provas
As emulsões fotográficas, usadas para recobrir filmes fotográficos, contêm brometo de prata e pequenas quantidades de iodeto de prata. Quando o filme é exposto à luz, íons brometo são oxidados fotoquimicamente, levando à liberação de elétrons que serão capturados pelos íons Ag+, ocasionando sua redução a Ag0. Durante o processo de revelação do filme, usa-se uma solução de tiossulfato de sódio. O íon tiossulfato é um poderoso agente complexante para íons prata, levando, assim, os íons que não foram reduzidos fotoquimicamente a se dissolverem na forma do íon complexo [Ag(S2O3)2]3•. A prata metálica, Ag0, não reage com o tiossulfato, ficando no filme, levando à formação do negativo da imagem. A partir dessas informações e considerando os dados M(AgBr) = 187,8g/mol, M(AgI) = 234,8 g/mol, M[Ag(S2O3)2]3• = 332,1 g/mol e RT/F = 0,06 V, julgue os itens abaixo, sabendo que os produtos de solubilidade do AgBr e do AgI são, respectivamente, 5,3 × 10•13 e 8,3 × 10•17.
Sabendo que a constante de formação do íon complexo [Ag(NH3)2]+ é 1,5 × 107, o menor volume de solução de NH3 1,0 mol/L para dissolver 50 mg de AgBr de uma amostra é 9,5 mL.
Provas
Caderno Container