Foram encontradas 70 questões.
Extrações líquido-líquido podem ser feitas em equipamentos simples do tipo mostrado na figura a seguir.

Planovsky & Nikolaev. Unit Operations and Equipment of Chemical Engineering. p. 378, Mir Publishers, 1990.
Considere a equação a!$ \rho !$h + (b-a)!$ \rho !$1 = c!$ \rho !$h
onde:
!$ \rho !$h = densidade da fase mais densa
!$ \rho !$1 = densidade da fase menos densa
a, b e c = alturas
L = corrente mais densa
G = corrente menos densa
Essa equação mostra a relação existente entre as densidades da corrente mais densa (L) e da corrente menos densa (G).
Assim, a análise do equipamento e da equação que rege o seu funcionamento mostram que a
Provas
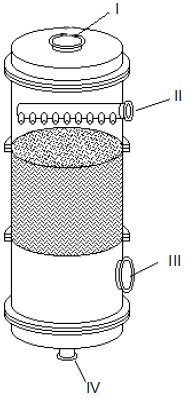
Um rejeito industrial que está contaminado por compostos orgânicos voláteis solúveis em água precisa ser tratado para poder ser descartado. Pretende-se remover esses compostos voláteis usando vapor d’água.
Considerando as correntes que serão introduzidas ou removidas da coluna nas posições de I a IV, conclui-se que se trata de uma operação de
Provas

A trietanolamina em solução aquosa é um solvente utilizado na retirada do H2S contido em diversos gases industriais. Numa refinaria, o gás proveniente de uma coluna de destilação de petróleo está contaminado com pequena quantidade de H2S. Deseja-se reduzir drasticamente a concentração de H2S no produto final usando a coluna recheada mostrada acima. Considerando as correntes que serão introduzidas ou removidas da coluna nas posições de I a IV, conclui-se que se trata de uma operação de
Provas
Na figura abaixo encontra-se esquematizada uma unidade de destilação azeotrópica.
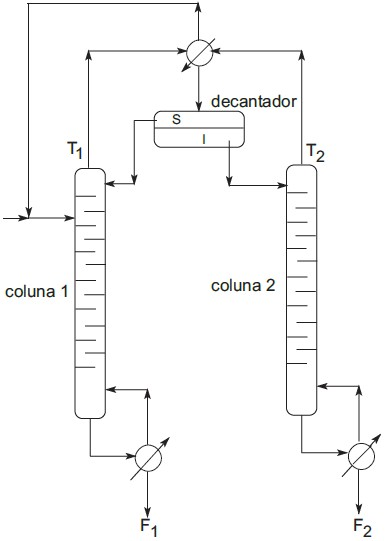
Para exemplificar o funcionamento de uma unidade desse tipo, considere a produção de etanol anidro a partir do etanol hidratado em que se usa o benzeno como solvente que forma azeótropo de máxima pressão de vapor.
A esse respeito, analise as afirmações a seguir.
I - O etanol anidro é retirado na corrente F1 e a água, na corrente F2.
II - O etanol anidro é retirado na corrente T2 e a água, na corrente F2.
III - A fase I no decantador é rica em etanol e água.
IV - O solvente sai majoritariamente na corrente F1.
V - O etanol hidratado sai na corrente T2 e a água, na corrente F2.
Estão corretas APENAS as afirmações
Provas
Considere desprezível a resistência do elemento filtrante de seção circular numa filtração convencional a vácuo (a pressão constante).
(Dados:
tempo de filtração = !$ \dfrac{\mu \alpha \text{cV}^2} {2\text{A}^2\text{P}} !$
onde
!$ \mu !$ = viscosidade do fluido
!$ \alpha !$ = resistência específica da torta
c = concentração da suspensão
v = volume de filtrado
P = pressão)
Ao se dobrar o raio do elemento filtrante, o tempo de filtração será
Provas
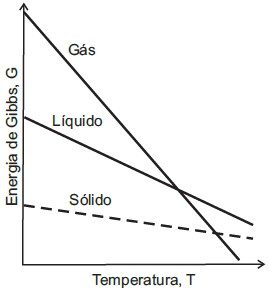
Considerando a pressão constante, e com base na interpretação das informações apresentadas no gráfico acima, analise as afirmações a seguir.
I - A Energia de Gibbs se altera mais sensivelmente na fase gasosa do que na fase líquida porque a entropia de uma substância é maior na fase gasosa do que na fase líquida.
II - A Energia de Gibbs se altera mais sensivelmente na fase sólida do que na fase líquida porque a entropia de uma substância é maior na fase líquida do que na fase sólida.
III - A Energia de Gibbs nas fases sólida, líquida e gasosa não depende da entropia.
Está(ão) correta(s) APENAS a(s) afirmação(ões)
Provas
Dentre os gráficos de I a V mostrados a seguir, os que correspondem à titulação de 100 mL de uma solução 0,1 M de NaCl e à titulação de 100 mL de uma solução 0,1 M de KI são, respectivamente, os gráficos

(Dados: Ksol (AgCl) = 1,2 !$ \times !$ 10–10 e Ksol (AgI) = 1,7 !$ \times !$ 10–16)
Provas
Ao ser titulado por uma base, um ácido polifosfórico apresentou pontos de equivalência em 30,4 cm3 e 45,6 cm3. O número de átomos de fósforo e a quantidade de hidrogênios ácidos dessa molécula correspondem, respectivamente, a
Provas
Considere os gráficos de derivada primeira e derivada segunda correspondentes à titulação potenciométrica de uma solução de ácido acético por solução de NaOH 0,1 M mostrados a seguir.
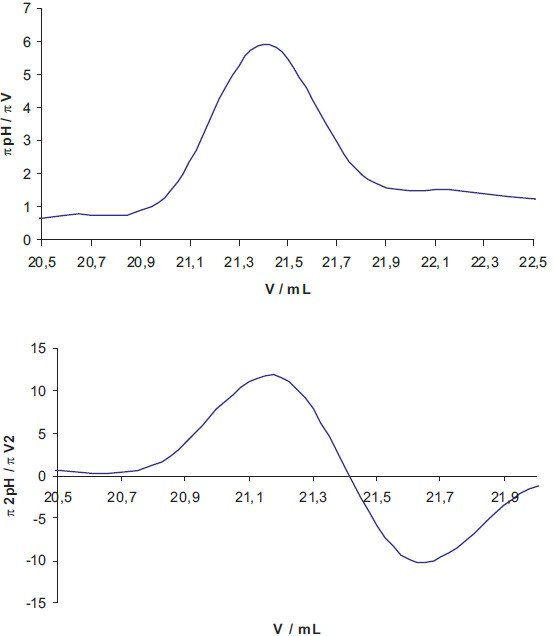
Com base na análise dos gráficos, o ponto de equivalência dessa titulação ocorre com a adição de
Provas
Os dados da tabela a seguir foram usados na construção de uma curva de calibração utilizada na dosagem da concentração de um metal presente numa água oriunda de um despejo industrial, através da técnica de ultravioleta-visível.
(Dados: A = k.b.C, onde k é uma constante característica do complexo metálico, b é a distância do percurso ótico e C é a concentração composto orgânico.)
|
!$ \mu !$g/mL |
Absorvância |
|
0 |
0,05 |
| 5 | 0,06 |
| 10 | 0,07 |
| 15 | 0,08 |
| 20 | 0,092 |
| 25 | 0,107 |
| 30 | 0,120 |
| 40 | 0,145 |
| 50 | 0,170 |
| 60 | 0,190 |
| 80 | 0,240 |
A análise de uma alíquota desse rejeito industrial apresentou um valor de absorvância (já corrigido em relação ao branco) igual a 0,150. A concentração do composto orgânico presente no rejeito industrial, em !$ \mu !$g/mL, é
Provas
Caderno Container