Foram encontradas 100 questões.
Duas soluções aquosas (I e lI) contêm, respectivamente, quantidades iguais (em moI) e desconhecidas de um ácido forte, K >> 1, e de um ácido fraco, K !$ \cong !$ 10 !$ ^{10} !$ (K = constante de dissociação do ácido). Na temperatura constante de 25°C, essas soluções são tituladas com uma solução aquosa 0,1 moI L !$ ^{-1} !$ de NaOH. A titulação é acompanhada pela medição das respectivas condutâncias elétricas das soluções resultantes. Qual das opções abaixo contém a figura com o par de curvas que melhor representa a variação da condutância elétrica (Cond.) com o volume de NaOH ( !$ V_{NaOH} !$) adicionado às soluções I e lI, respectivamente?
Provas
Qual das substâncias abaixo apresenta o menor valor de pressão de vapor saturante na temperatura ambiente?
Provas
O abaixamento da temperatura de congelamento da água numa solução aquosa com concentração molal de soluto igual a 0,100 mol kg!$ ^{-1} !$ é 0,55°C. Sabe-se que a constante crioscópica da água é igual a 1,86°C kg mol!$ ^{-1} !$. Qual das opções abaixo contém a fórmula molecular CORRETA do soluto?
Provas
Para minimizar a possibilidade de ocorrência de superaquecimento da água durante o processo de aquecimento, na pressão ambiente, uma prática comum é adicionar pedaços de cerâmica porosa ao recipiente que contém a água a ser aquecida. Os poros da cerâmica são preenchidos com ar atmosférico, que é vagarosamente substituído por água antes e durante o aquecimento. A respeito do papel desempenhado pelos pedaços de cerâmica porosa no processo de aquecimento da água são feitas as seguintes afirmações:
I. a temperatura de ebulição da água é aumentada.
II. a energia de ativação para o processo de formação de bolhas de vapor de água é diminuída.
III. a pressão de vapor da água não é aumentada.
IV. o valor da variação de entalpia de vaporização da água é diminuído.
Das afirmações acima está(ão) ERRADA(S)
Provas
A uma determinada quantidade de dióxido de manganês sólido, adicionou-se um certo volume de ácido clorídrico concentrado até o desaparecimento completo do sólido. Durante a reação química do sólido com o ácido observou-se a liberação de um gás (Experimento 1). O gás liberado no Experimento 1 foi borbulhado em uma solução aquosa ácida de iodeto de potássio, observando-se a liberação de um outro gás com coloração violeta (Experimento 2). Assinale a opção que contém a afirmação CORRETA relativa às observações realizadas nos experimentos acima descritos.
Provas
Considere os equilíbrios químicos abaixo e seus respectivos valores de !$ pK (pK = – \log K) !$, válidos para a temperatura de 25°C (K representa constante de equilíbrio químico).
Fenol !$ C_6H_5OH(aq) \rightleftarrows H^+(aq) + C_6H_5O^–(aq) !$ !$ \begin{matrix} pk \\9,89 \end{matrix} !$
Anilina !$ C_6H_5NH_2(l) + H_2O(l) \rightleftarrows C_6H_5NH_3^+(aq) + OH^–(aq) !$ !$ 9,34 !$
Ácido !$ CH_3COOH(aq) \rightleftarrows CH_3COO^–(aq) + H^+(aq) !$ !$ 4,74 !$
acético
Amônia !$ NH_3(g) + H_2O(l) \rightleftarrows NH_4^+(aq) + OH^–(aq) !$ !$ 4,74 !$
Na temperatura de 25 °C e numa razão de volumes !$ \le !$ 10, misturam-se pares de soluções aquosas de mesma concentração.
Assinale a opção que apresenta o par de soluções aquosas que ao serem misturadas formam uma solução tampão com pH próximo de 10.
Provas
Considere o elementogalvânico mostrado na figura abaixo. O semi-elemento A contém uma solução aquosa, isenta de oxigênio, 0,3 moI L !$ ^{-1} !$ em Fe !$ ^{2+} !$ e 0,2 moI L !$ ^{-1} !$ em Fe !$ ^{3+} !$. O semi-elemento B contém uma solução aquosa, também isenta de oxigênio, 0,2 moI L !$ ^{-1} !$ em Fe !$ ^{2+} !$ e 0,3 moI L !$ ^{-1} !$ em Fe !$ ^{3+} !$. M é um condutor metálico (platina). A temperatura do elemento galvânico é mantida constante num valor igual a 25°C.
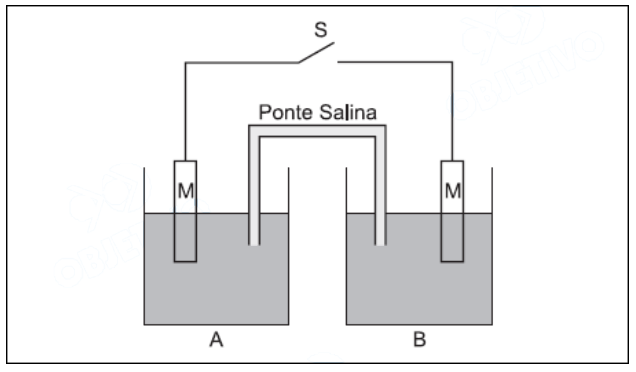
A partir do instante em que a chave “S” é fechada, considere as seguintes afirmações:
I. O sentido convencional de corrente elétrica ocorre do semi-elemento B para o semi-elemento A.
II. Quando a corrente elétrica for igual a zero, a relação de concentrações [Fe !$ ^{3+} !$(aq)] / [Fe !$ ^{2+} !$(aq)] tem o mesmo valor tanto no semi elemento A como no semi-elemento B.
III. Quando a corrente elétrica for igual a zero, a concentração de Fe !$ ^{2+} !$ (aq) no semi-elemento A será menor do que 0,3 mol L !$ ^{-1} !$.
IV. Enquanto o valor da corrente elétrica for diferente de zero, a diferença de potencial entre os dois semi-elementos será maior do que 0,118 !$ \log !$ (3/2).
V. Enquanto corrente elétrica fluir pelo circuito, a relação entre as concentrações [Fe !$ ^{3+} !$(aq)] / [Fe !$ ^{2+} !$(aq)] permanece constante nos dois semi-elementos.
Das afirmações feitas, estão CORRETAS
Provas
Considere as seguintes comparações de calores específicos dos respectivos pares das substâncias indicadas.
I. tetracloreto de carbono (l, 25°C) > metanol (l, 25 °C).
II. água pura (l, –5 °C) > água pura (s, –5 °C).
III. alumina (s, 25 °C) > alumínio (s, 25 °C).
IV. isopor (s, 25 °C) > vidro de janela (s, 25 °C).
Das comparações feitas, está(ão) CORRETA(S)
Provas
Num cilindro, provido de um pistão móvel sem atrito, é realizada a combustão completa de carbono (grafite). A temperatura no interior do cilindro é mantida constante desde a introdução dos reagentes até o final da reação.
Considere as seguintes afirmações:
I. A variação da energia interna do sistema é igual a zero.
II. O trabalho realizado pelo sistema é igual a zero.
III. A quantidade de calor trocada entre o sistema e a vizinhança é igual a zero.
IV. A variação da entalpia do sistema é igual à variação da energia interna.
Destas afirmações, está(ão) CORRETA(S)
Provas
Uma solução líquida é constituída de 1,2-dibromo etileno !$ (C_2H_2Br_2) !$ e 2,3-dibromo propeno !$ (C_3H_4Br_2) !$. A 85°C, a concentração do 1,2 dibromo etileno nesta solução é igual a 0,40 (moI/mol). Nessa temperatura as pressões de vapor saturantes do 1,2-dibromo etileno e do 2,3- dibromo propeno puros são, respectivamente, iguais a 173 mmHg e 127 mmHg. Admitindo que a solução tem comportamento ideal, é CORRETO afirmar que a concentração (em moI/mol) de 2,3-dibromo propeno na fase gasosa é igual a
Provas
Caderno Container