Foram encontradas 600 questões.
Em uma pilha combustível ocorre as seguintes semi - reações representadas abaixo, responda à questão.
O2(g) + 2 H2O(l) + 4e-
→ 4OH-(aq) E0
= +0,40V
2 H2O(l) + 2e-
→ H2(g) + 2OH-(aq) E0
= -0,83V
Provas
Questão presente nas seguintes provas
Em uma pilha combustível ocorre as seguintes semi - reações representadas abaixo, responda à questão.
O2(g) + 2 H2O(l) + 4e-
→ 4OH-(aq) E0
= +0,40V
2 H2O(l) + 2e-
→ H2(g) + 2OH-(aq) E0
= -0,83V
Provas
Questão presente nas seguintes provas
Analise as afirmativas a seguir sobre termoquímica.
I. Em uma reação endotérmica, a entalpia do sistema reativo cresce, ou seja, a entalpia dos produtos é maior do que a entalpia dos reagentes. II. A lei da conservação de energia estabelece que a energia não é criada nem destruída em uma mudança de estado físico. III. A variação de entalpia da reação depende do caminho que as reações ocorrem – Lei de Hess.
Está(Estão) correta(s) a(s) afirmativa(s)
I. Em uma reação endotérmica, a entalpia do sistema reativo cresce, ou seja, a entalpia dos produtos é maior do que a entalpia dos reagentes. II. A lei da conservação de energia estabelece que a energia não é criada nem destruída em uma mudança de estado físico. III. A variação de entalpia da reação depende do caminho que as reações ocorrem – Lei de Hess.
Está(Estão) correta(s) a(s) afirmativa(s)
Provas
Questão presente nas seguintes provas
O gás de cozinha é fundamentalmente composto pelos gases propano (C3H8) e butano (C4H10), a
queima deste gás está sendo usada para aquecer 3,60 Kg de água. Qual a quantidade de calor (q)
absorvida pela água sabendo-se que um mol do gás elevou a temperatura da água de 25ºC para 78,7ºC
Dados: calor específico da água (c) = 4,18 J/gºC.
Dados: calor específico da água (c) = 4,18 J/gºC.
Provas
Questão presente nas seguintes provas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
- Transformações Químicas e EnergiaTermoquímica
Sobre a termoquímica, é correto afirmar que
Provas
Questão presente nas seguintes provas
- Química OrgânicaCadeias Carbônicas
- Química OrgânicaFunções Nitrogenadas: Amina, Amida, Nitrila, Isonitrila e Nitro Composto
- Química OrgânicaIsomeria Plana e Espacial
A fórmula estrutural de um dos constituintes do jambu, erva típica da região Norte e muito apreciada
na culinária paraense, é a seguinte:
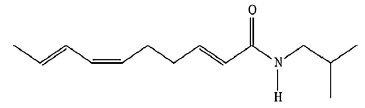
Sobre esta substância, faz-se as seguintes afirmativas:
I- possui a função amina, II- apresenta 7 carbonos com hibridação sp2 , III-possui 23 átomos de hidrogênio, IV- pode apresentar isomeria óptica, V- apresenta a função amida.
Estão corretos os itens

Sobre esta substância, faz-se as seguintes afirmativas:
I- possui a função amina, II- apresenta 7 carbonos com hibridação sp2 , III-possui 23 átomos de hidrogênio, IV- pode apresentar isomeria óptica, V- apresenta a função amida.
Estão corretos os itens
Provas
Questão presente nas seguintes provas
- Química InorgânicaSoluções e Substâncias InorgânicasSoluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais
Para preparar um tacacá saboroso, deve-se adicionar Cloreto de sódio na medida certa ao tucupi.
Em sua primeira experiência na cozinha, uma aspirante a tacacazeira adiciona 35,1 g desse sal em 3 L
de tucupi, mas percebe que está “muito salgado” e adiciona tucupi até alcançar uma concentração de
0,05 mols de NaCl por L de tucupi. A quantidade de tucupi adicionada foi de
Obs.: Massas molares em g.mol-1 : Na = 23 e Cl = 35,5.
Obs.: Massas molares em g.mol-1 : Na = 23 e Cl = 35,5.
Provas
Questão presente nas seguintes provas
Na mesma família do sódio, segundo a tabela periódica, encontra-se o elemento químico césio. Uma
amostra abandonada de seu isótopo 137 foi responsável pelo maior acidente radioativo registrado no
Brasil, mais especificamente em Goiânia, no ano de 1987. Considerando, hipoteticamente, que a meia-vida
deste isótopo fosse de 10 anos e que sua massa inicial em 1987 fosse igual a 30 g, em 2017 a
massa, em gramas, que restaria seria de
Provas
Questão presente nas seguintes provas
- Química CinéticaVelocidade de Reação, Energia de Ativação e Catalisadores
- Transformações Químicas e EnergiaRadioatividade
Na mesma família do sódio, segundo a tabela periódica, encontra-se o elemento químico césio. Uma
amostra abandonada de seu isótopo 137 foi responsável pelo maior acidente radioativo registrado no
Brasil, mais especificamente em Goiânia, no ano de 1987.
Considerando:
I) Os dados da questão anterior, II) Que o decaimento radioativo é um processo cinético de primeira ordem que atende à equação: ln N – ln N0 = λ. t III) ln 2 = 0,693.
A constante de decaimento, em ano-1 , para o césio 137 nesse caso seria igual a:
Considerando I) os dados da questão anterior, II) que o decaimento radioativo é um processo cinético de primeira ordem que atende à equação ln N – ln N0 = λ. t e III) que ln 2 = 0,693,
a constante de decaimento, em ano-1 , para o césio 137, nesse caso, seria igual a
Considerando:
I) Os dados da questão anterior, II) Que o decaimento radioativo é um processo cinético de primeira ordem que atende à equação: ln N – ln N0 = λ. t III) ln 2 = 0,693.
A constante de decaimento, em ano-1 , para o césio 137 nesse caso seria igual a:
Considerando I) os dados da questão anterior, II) que o decaimento radioativo é um processo cinético de primeira ordem que atende à equação ln N – ln N0 = λ. t e III) que ln 2 = 0,693,
a constante de decaimento, em ano-1 , para o césio 137, nesse caso, seria igual a
Provas
Questão presente nas seguintes provas
Em uma situação hipotética, uma amostra de césio 137 (Z=55) foi transportada de Goiânia para
análise em um laboratório em Belém e, durante a viagem, sofreu decaimento emitindo duas partículas
alfa e quatro partículas beta. Assim, pode-se dizer que a amostra que o analista em Belém recebeu
seria constituída por
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container