Uma grandeza útil para avaliar o grau de desvio do comportamento do modelo ideal por um gás real é o fator de compressibilidade Z, que corresponde à razão entre o volume molar do gás real e o volume molar do gás ideal. O gráfico a seguir traz a relação de Z coma pressão para alguns gases comuns.
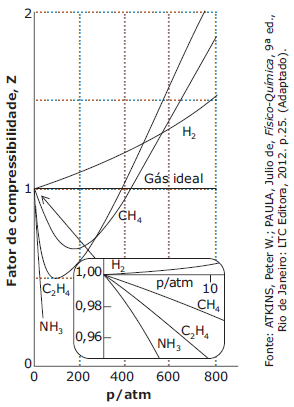
Considerando o gráfico e as informações expostas, analise as seguintes afirmativas.
I → O desvio do comportamento ideal pelo H2 é justificado pela forte interação atrativa existente entre as moléculas constituintes do gás.
II → Em baixas pressões, o valor de Z para o etano é menor do que para o metano devido à maior interação atrativa por forças de dispersão no etano.
III → A amônia apresenta desvio acentuado por causa de fortes ligações de hidrogênio.
IV → Em pressões maiores que 400 atm, as interações repulsivas no metano são maiores que as do etano.
Está(ão) correta(s)