Foram encontradas 35.934 questões.
O tipo de cromatografia de líquidos de alta eficiência, no qual a fase estacionária é um líquido imiscível com o líquido que compõe a fase móvel, é denominado cromatografia por:
Provas
Na sistematização da análise qualitativa de cátions metálicos, o grupo formado por chumbo, mercúrio I e prata em solução aquosa forma precipitados ao reagir com:
Provas
Uma amostra de 20 mL de uma solução aquosa de ácido nítrico foi titulada até o ponto de equivalência com 12 mL de uma solução aquosa de NaOH de concentração 0,20 mol/L.
A concentração, em mol/L, da solução ácida é igual a:
Provas
A aeração é um dos processos empregados para a remoção de íons Fe+2 no tratamento de águas. A remoção ocorre através de precipitação com formação de:
Provas
gás natural é um combustível cujo principal componente é o metano. As entalpias-padrão de formação das substâncias compostas participantes da reação de combustão do metano são apresentadas a seguir.

A entalpia-padrão de combustão do metano, em kJ/mol, corresponde a:
Provas
Uma mistura líquida de massa igual a 140 g é formada por 30% de propanol e 70% de hexano. Essa mistura é separada pelo processo de extração líquido-líquido mediante a adição de 60 g de água. Com a adição da água, são formadas duas fases: orgânica e aquosa. A fase orgânica tem massa igual a 100 g e é composta apenas por propanol e hexano. A fase aquosa é composta apenas por propanol e água. A concentração percentual de propanol na fase aquosa é igual a:
Provas
Em um estudo, avaliou-se a solubilidade do N2 em água a 20°C e 1 atm, sabendo-se que a pressão parcial do N2 é 0,80 atm e a constante de Henry é 7,0 x 10-4mol/L.atm.
Sua solubilidade, em gramas por litro, é aproximadamente igual a: Dado: N2 = 28 g/mol
Provas
Em um experimento, foi realizada a eletrólise do cloreto de potássio em solução aquosa com eletrodos inertes. O composto formado no catodo da eletrólise corresponde a:
Provas
O peróxido de hidrogênio se decompõe de acordo com a reação química apresentada a seguir.
2 H2O2 (aq) → 2 H2O (l) + O2 (g)
Em um estudo cinético dessa reação, mediu-se a velocidade da reação em dois experimentos nos quais se variou a concentração inicial de H2O2 , conforme apresentado a seguir:
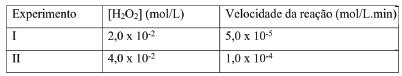
A constante de velocidade dessa reação, em min , é igual a:
Provas
O íon complexo [Zn(NH3)4 ]2+ é formado a partir da seguinte reação química:
![]()
Em um experimento, ao se atingir o equilíbrio químico, as concentrações dos participantes da reação são apresentadas na tabela a seguir.
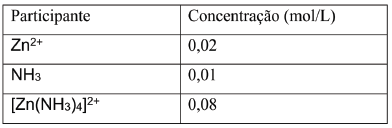
A constante de equilíbrio dessa reação é igual a:
Provas
Caderno Container