Foram encontradas 35.936 questões.
Observe as substâncias a seguir:
I. HNO3
II. K2SO4
III. BA(OH)2
IV. AI2O3
V. Ca(NO)2
Considerando tais substâncias, é CORRETO afirmar que:
Provas
O ácido hexafluorossilícico (H2SiF6) é utilizado para fornecer fluoreto em água de abastecimento. Em contato com a água, esse ácido hidrolisa de acordo com a equação (não balanceada) a seguir.
(H2SiF6(I)+H2O(I)!$ \rightleftharpoons !$HF(aq)+SiO2(s)
O volume, expresso em litros, de ácido hexafluorossilícico 2,0 mol/L necessário para manter o teor de fluoreto igual a 1,0 mg/L em 500 m3 de água, considerando o ácido fluorídrico totalmente dissociado nesse volume de água, é:
(Dados das massas molares: ácido hexafluorossilícico: 144,10 g/mol; fluor: 19,00 g/mol)
Provas
É necessário preparar uma solução concentrada de sulfato de potássio em uma dada temperatura. Considerando a solubilidade do sal em água igual a 13,0 g/100 mL nessa dada temperatura, a concentração máxima, expressa em mol/L, de íons potássio que essa solução pode ter para haver a dissolução total do sal é:
(Dados das massas molares (g/mol): sulfato de potássio = 174,26; potássio = 39,10)
Provas
Considere que a combustão incompleta de 25,00 g de ácido cítrico sólido (C6H8O7) produziu 3,90 g de carvão (C). Observe a equação global (não-balanceada) do processo envolvido, apresentada a seguir.
C6H8O7(s)!$ → !$C(s)+H2O(g)+CO(g)
Considerando as informações apresentadas e que as massas molares do ácido cítrico e do carbono são, respectivamente, 192,12 g/mol e 12,01 g/mol, o rendimento da conversão de ácido cítrico em carvão é:
Provas
A figura a seguir representa um Bico de Bunsen, utilizado como fonte de calor para o aquecimento de materiais.
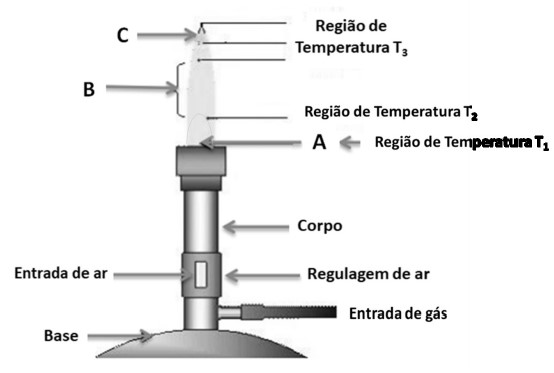
Fonte: Esboçado pelo autor.
Considerando as informações apresentadas, assinale a afirmativa CORRETA:
Provas
A figura a seguir apresenta os pictogramas observados nos rótulos de alguns reagentes de acordo com a proposta do Diamante de Hommel.
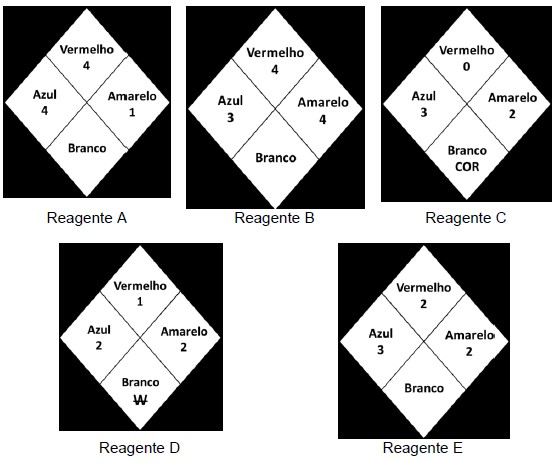
Fonte: Elaborado pelo autor.
Considerando as informações apresentadas, assinale a afirmativa INCORRETA:
Provas
Automóveis são veículos movidos por tração própria, gerada por um sistema mecânico central, normalmente à explosão, e por um sistema elétrico/eletrônico secundário e periférico, que comanda todos os acessórios e controles do veículo, movido a eletricidade, gerada por uma bateria. A bateria comumente usada é a bateria de chumbo, que deverá ser substituída periodicamente sempre que ocorrer diminuição na sua capacidade de recarga e geração de eletricidade. Alguns veículos ficam com as suas baterias originais de fábrica por 4 ou 5 anos, mas o mais comum é a troca ocorrer no período de 3 anos de uso.
As reações padrão de redução que compõem o sistema redox da bateria são as seguintes:
PbSO4(s) + H+ (aq) + 2 e - → Pb(s) + HSO4 - (aq) E0 = - 0,359 V
PbO2 (s) + 4 H+ (aq) + SO4 2- (aq) + 2 e - → PbSO4 (s) + 2 H2O (l) E0 = + 1,691 V
Considerando as informações apresentadas anteriormente, analise as afirmativas a seguir:
I. O Pb(s) é o anodo do sistema redox.
II. O PbO2(s) é o catodo do sistema redox.
III. Para se obter 12V em uma bateria de chumbo, são necessários 12 pares de eletrodos ligados em série.
IV. A bateria vai perder sua capacidade total de gerar eletricidade quando as reações envolvidas alcançarem o estado de equilíbrio.
Está CORRETO o que se afirma, apenas, em:
Provas
A figura a seguir apresenta os pictogramas observados nos rótulos de alguns reagentes de acordo com a proposta do Sistema Globalmente Harmonizado de Classificação e Rotulagem de Produtos Químicos (GHS).

Fonte: Esboçado pelo autor.
Considerando as informações apresentadas, assinale a afirmativa CORRETA:
Provas
Em um laboratório de ensino, uma das técnicas encontrou um frasco não identificado com um sólido branco. Ao fazer uma rápida inspeção sobre os reagentes disponíveis no laboratório e as características físicas do referido material, ela inferiu que aquela amostra poderia ser de nitrato de sódio, cloreto de sódio, carbonato de sódio ou sulfato de sódio. Dessa forma, decidiu realizar alguns testes, constatando inicialmente que a substância era solúvel em água. Em seguida, verificou que a solução obtida conduzia eletricidade e ficou rosa ao serem adicionadas algumas gotas de fenolftaleína. Por fim, a técnica verificou que o sólido reagiu com uma solução aquosa de ácido clorídrico, o que levou à formação de gás.
A partir das observações feitas por meio dos testes realizados e considerando que a amostra não seria de outro material além daqueles citados, a técnica deveria concluir que o frasco continha:
Provas
Há muito tempo, as pessoas utilizam saberes populares ou artefatos tradicionais para preverem algo com base em observações que permitam inferências sobre a natureza. Como exemplo, menciona-se o galo do tempo, em destaque na imagem a seguir.

Disponível em: www.amazon.com.br. Acesso em 10 de fev. de 2022.
Esse artefato é utilizado ainda hoje para inferir sobre as possíveis condições do tempo, com indicativo de chuva ou não. Isso ocorre em razão de o galo do tempo possuir em sua composição o cloreto de cobalto II. Quando esse composto se hidrata, a superfície do galo que o contém altera sua cor, passando de azul a rosa. Buscando contextualizar uma aula de Química e comprovar o fenômeno observado no galo do tempo, propôs-se uma prática na qual se preparou uma solução obtida pela dissolução de cloreto de cobalto II em ácido clorídrico, processo este que pode ser representado pela seguinte reação em equilíbrio:
[Co(H2O)6]2- (aq) + 4 Cl-(aq) ⇌ CoCl42-(aq) + 6 H2O(l)
(cor rosa) (cor azul)
Essa solução foi divida em duas partes, sendo cada uma delas colocada em tubos de ensaio identificados como A e B. Em seguida, o tubo A foi imerso em um béquer contendo gelo e o tubo B, em outro béquer com água em ebulição. Após certo tempo, observou-se que a solução presente no tubo A ficou rosa e que a solução do tubo B ficou azul. Considerando o exposto, é INCORRETO afirmar que:
Provas
Caderno Container