Foram encontradas 35.978 questões.
Relacione os pictogramas apresentados abaixo com as respectivas substâncias:
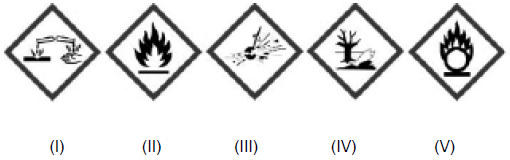
SUBSTÂNCIAS
( ) oxidantes
( ) explosivas
( ) corrosivas
( ) nocivas ao meio ambiente
( ) inflamáveis
A sequência correta é
Provas
Considere a representação da molécula de colesterol.
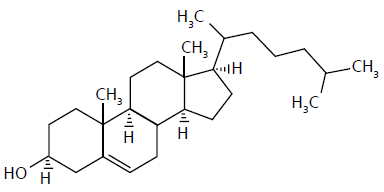
Sobre a estrutura acima, analise se as afirmativas são verdadeiras (V) ou falsas (F):
( ) Apresenta a função fenol.
( ) Apresenta isomeria óptica.
( ) Possui quatro centros de quiralidade.
( ) Possui baixa solubilidade em água.
( ) É um composto meso.
A sequência correta é
Provas
Considere as estruturas representadas abaixo.
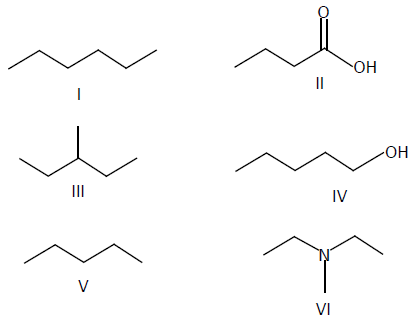
Em relação às propriedades físico-químicas dos compostos, é INCORRETO afirmar que
Provas
Os elementos essenciais à reação de combustão são
Provas
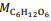 = 180 g/mol e
= 180 g/mol e 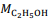 = 46 g/mol.
= 46 g/mol. De acordo com os experimentos de Faraday, a quantidade de produto formado ou de reagente consumido em uma reação eletrolítica é estequiometricamente proporcional à diferença de potencial aplicada entre os eletrodos da célula eletrolítica.
Provas
- Química CinéticaRepresentação das Transformações Químicas
- Química OrgânicaGlicídios, Lipídios, Aminoácidos e Proteínas.
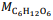 = 180 g/mol e
= 180 g/mol e 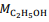 = 46 g/mol.
= 46 g/mol. De acordo com a reação descrita, para a obtenção de 1,0 kg de etanol, são necessários mais de 2,0 kg de glicose.
Provas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
O ângulo de ligação entre átomos de hidrogênio é maior em uma molécula de amônia que em uma molécula de água.
Provas
De acordo com a teoria de ligação de valência, a molécula de água é constituída por quatro orbitais híbridos do tipo sp3 arranjados de forma tetraédrica em torno do oxigênio, de maneira que dois orbitais participam das ligações simples O–H e outros dois acomodam os pares de elétrons não ligantes.
Provas
- FundamentosLigações Químicas
- FundamentosPropriedades das Substâncias
- Química InorgânicaGeometria Molecular, Polaridade e Forças Intermoleculares
A molécula de N2H2 é linear e nela há uma dupla ligação entre os átomos de nitrogênio, sendo cada átomo de hidrogênio ligado a um dos átomos de nitrogênio.
Provas
Uma das principais vantagens da teoria de ligação de valência é a possibilidade de explicar, satisfatoriamente, fenômenos associados a estados de excitação e de prever os espectros de absorção e emissão de energia eletrônica das moléculas.
Provas
Caderno Container