Foram encontradas 36.167 questões.
Um sistema contendo oxigênio atômico (na forma do isótopo estável mais abundante) e hidrogênio atômico (na forma dos dois isótopos mais estáveis) é colocado a reagir em duas condições diferentes, levando à formação de produtos únicos e distintos, X e Y, respectivamente. Considere que X e Y correspondem a moléculas neutras, estáveis e que obedecem à regra do octeto, e que a massa molar média de X é menor do que a de Y. Assinale a opção que relaciona corretamente as possíveis razões entre as massas de hidrogênio e de oxigênio nas moléculas que constituem X e Y.
Provas
Um eletrólito genérico BA2 ioniza em solução aquosa, de acordo com a equação química:
!$ BA_2 \rightleftharpoons B^2 + 2A^- !$
Considere duas soluções aquosas, preparadas com as mesmas quantidades desse eletrólito, nas seguintes condições de equilíbrio:
Solução 1: Volume V1, temperatura T1 e grau de ionização do eletrólito α1.
Solução 2: Volume V2 = 2V1, temperatura T2 e grau de ionização do eletrólito α2 = α1.
Com base nessas informações, assinale a opção que relaciona corretamente a constante de equilíbrio da ionização do eletrólito na solução 2, K2, com a constante de equilíbrio na solução 1, K1.
Provas
Considere os seguintes compostos:
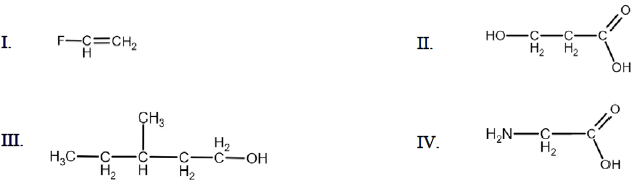
Qual(is) dos compostos acima forma(m) comumente polímeros de condensação?
Provas
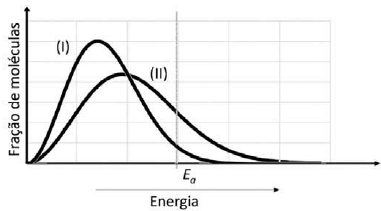
Considere que as curvas (I) e (II) representam uma mesma reação química em fase gasosa, mas em diferentes condições. Sabendo que Ea é a energia de ativação, é CORRETO afirmar que
Provas
Considere as seguintes afirmações relacionadas a átomos e íons atômicos no estado gasoso:
I. A afinidade eletrônica do átomo de oxigênio é maior do que a do ânion O−.
II. A energia de ionização do átomo de oxigênio é maior do que a do ânion O2−.
III. O raio atômico do átomo de oxigênio é maior do que o do ânion O−.
IV. O átomo de oxigênio tem maior afinidade eletrônica e menor energia de ionização do que o átomo de nitrogênio.
Das afirmações I a IV, acima destacadas, são CORRETAS
Provas
Sabe-se que a constante de velocidade (k) de uma reação é função da temperatura (T) conforme a Lei de Arrhenius:
!$ K = Ae^{ \left( { \large -E-a \over RT} \right )} !$
em que A é o fator de frequência e Ea é a energia de ativação. Em um estudo cinético, observou-se que a velocidade de uma determinada reação aumenta 1000 vezes quando a temperatura do meio reacional aumenta de 400 K para 500 K, permanecendo constantes todos os demais parâmetros iniciais. Assinale a opção que apresenta a energia de ativação desta reação, em kcal mol−1, considerando que A e Ea não dependem da temperatura.
Provas
Constantes
Constante de Avogadro (NA) = 6,02 × 1023 mol−1
Constante de Faraday (F) = 9,65 × 104 C mol−1 = 9,65 × 104 A s mol−1 = 9,65 × 104 J V−1 mol−1
Carga elementar = 1,60 × 10−19 C
Constante dos gases (R) = 8,21 × 10−2 atm L K−1 mol−1 = 8,31 J K−1 mol−1 = 1,98 cal K−1 mol−1
Constante de Planck (h) = 6,63 × 10−34 J s
Velocidade da luz no vácuo = 3,0 × 108 m s−1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 × 105 N m−2 = 1,01325 bar
Energia: 1 J = 1 N m = 1 kg m2 s−2 = 6,24 × 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 °C e 1 atm
Condições ambientes: 25 °C e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol L−1 (rigorosamente: atividade unitária das
espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em
questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol L−1
ln X = 2,3 log X
Massas Molares
| Elemento | Número Atômico | Massa Molar |
| H | 1 | 1,01 |
| Li | 3 | 6,94 |
| B | 5 | 10,81 |
| C | 6 | 12,01 |
| N | 7 | 14,01 |
| O | 8 | 16,00 |
| F | 9 | 19,00 |
| Na | 11 | 22,99 |
| Al | 13 | 26,98 |
| Elemento | Número Atômico | Massa Molar |
| P | 15 | 30,97 |
| S | 16 | 32,06 |
| Cl | 17 | 35,45 |
| k | 19 | 39,10 |
| Ca | 20 | 40,08 |
| Ga | 31 | 69,72 |
| Se | 34 | 78,96 |
| Sr | 38 | 87,62 |
Em uma titulação, 100 mL de uma solução de um ácido monoprótico fraco, cuja constante de ionização é igual a 10−9, são neutralizados com 25 mL de uma solução 0,5 mol L−1 de hidróxido de sódio.
Assinale a opção que apresenta o pH no ponto de equivalência da titulação.
Provas
Considere a teoria dos gases ideais e a equação dos gases de van der Waals dada abaixo.
!$ P=\dfrac{nRT}{V-nb}-\dfrac{an^2}{V^2} !$
Assinale a opção correta.
Provas
A prednisona é um pró-fármaco que é convertido, pelo fígado, no metabólito ativo prednisolona, o qual possui potente ação anti-inflamatória. Suas estruturas são mostradas abaixo:
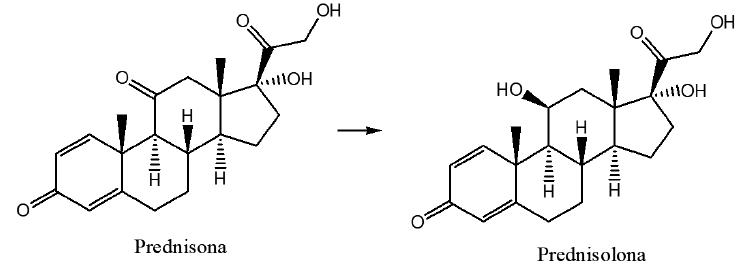
Considerando as estruturas acima, são feitas as afirmações abaixo.
I. A prednisona sofre redução para se transformar em prednisolona.
II. Ambas as moléculas têm o mesmo número de carbonos quirais.
III. Os grupos cetona, álcool e éster são funções orgânicas presentes em ambas as moléculas.
Assinale a opção que apresenta APENAS a(s) afirmativa(s) verdadeira(s).
Provas
Identifique a fórmula estrutural do principal produto da reação entre o cicloexa-1,4-dieno e o ciclopentadieno, ocorrida mediante aquecimento.
Provas
Caderno Container