Foram encontradas 36.167 questões.
Uma amostra inicial de 110,4 g contém uma mistura de KClO3,
KHCO3 e K2CO3. De modo a determinar sua composição
centesimal, tal amostra foi aquecida até a decomposição
completa, originando as seguintes transformações.
• 2KClO3 (s) → 2 KCl (s) + 3 O2 (g) • 2 KHCO3 (s) → K2O (s) + H2O (g) + 2 CO2 (g) • K2CO3 (s) → K2O (s) + CO2 (g)
Nas condições reacionais empregadas, o rendimento foi de 100% e produziu 1,80 g de água, 19,2 g de gás oxigênio e 22,0 g de gás carbônico.
Os percentuais aproximados de KClO3, KHCO3 e K2CO3 na amostra inicial são, respectivamente, iguais a
• 2KClO3 (s) → 2 KCl (s) + 3 O2 (g) • 2 KHCO3 (s) → K2O (s) + H2O (g) + 2 CO2 (g) • K2CO3 (s) → K2O (s) + CO2 (g)
Nas condições reacionais empregadas, o rendimento foi de 100% e produziu 1,80 g de água, 19,2 g de gás oxigênio e 22,0 g de gás carbônico.
Os percentuais aproximados de KClO3, KHCO3 e K2CO3 na amostra inicial são, respectivamente, iguais a
Provas
Questão presente nas seguintes provas
- Sistemas de EquilíbrioSistemas Homogêneos: Equilíbrio Iônico: Conceitos, Diluição de Ostwald, Efeito do Íon Comum
A força de um ácido está diretamente ligada a sua capacidade de
sofrer ionização. Essa força pode ser determinada
experimentalmente e expressa a partir do valor da constante de
ionização ácida (Ka).
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
Observe a tabela a seguir que contém os valores de pKa para cinco ácidos inorgânicos distintos.
ÁCIDO pKa carbônico 6,37 hipocloroso 7,53 hipobromoso 8,69 bórico 9,14 cianídrico 9,31
O ácido mais forte é o
Provas
Questão presente nas seguintes provas
Quando uma ligação química se forma, os átomos rearrumam
seus elétrons de modo a atingirem a configuração eletrônica de
um gás nobre. A esse princípio, o químico norte-americano G. N.
Lewis deu o nome de Regra do Octeto. No entanto, hoje sabemos
que diversos compostos não obedecem a esse princípio.
Um exemplo de composto que viola esse princípio é o
Provas
Questão presente nas seguintes provas
Um experimento de cinética química bastante conhecido é
chamado de “reação relógio”. Nele, os íons persulfato reagem
com íons iodeto conforme a reação balanceada a seguir.
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.
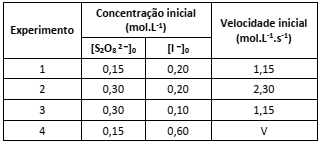
A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
S2O8 2 – (aq) + 3 I – (aq) → 2 SO4 2 – (aq) + I3 – (aq)
A tabela a seguir contém dados experimentais sobre a reação em condições específicas de temperatura e pressão.

A partir das informações apresentadas é possível prever que a velocidade (V) do Experimento 4 será
Provas
Questão presente nas seguintes provas
Desde o início do século XX ficou claro que a mecânica clássica
não seria capaz de explicar a estrutura interna dos átomos. Novas
leis precisaram ser desenvolvidas e ficaram conhecidas como
mecânica quântica.
A partir dessas novas leis foi possível determinar a(o)
A partir dessas novas leis foi possível determinar a(o)
Provas
Questão presente nas seguintes provas
- Química OrgânicaIsomeria Plana e Espacial
- Química OrgânicaPropriedades Físicas dos Compostos Orgânicos
Os mono-nitrofenóis (estruturas a seguir) têm diversas aplicações
industriais, sendo usados, por exemplo, como intermediários na
síntese de corantes e pesticidas organofosforados.
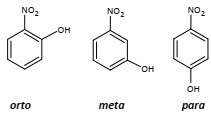
Apesar de serem isômeros entre si, eles possuem diferentes pontos de ebulição. Dentre eles, o composto de menor ponto de ebulição é o isômero

Apesar de serem isômeros entre si, eles possuem diferentes pontos de ebulição. Dentre eles, o composto de menor ponto de ebulição é o isômero
Provas
Questão presente nas seguintes provas
Em uma aula experimental sobre eletrólise, um professor ligou
três cubas eletrolíticas (I, II e III) em série, como ilustra a figura a
seguir.
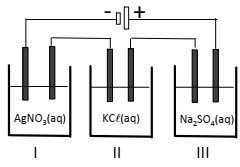
Cada cuba era constituída por um par de eletrodos inertes, continham soluções aquosas de AgNO3, KCl e Na2SO4 de mesma concentração e operaram durante um mesmo período de tempo em iguais condições.
A partir dessas informações, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Na cuba I observa-se formação de gás no cátodo.
( ) Na cuba II o pH da solução aumenta ao longo do processo. ( ) Na cuba III um depósito sólido é formado no ânodo.
As afirmativas são, respectivamente,

Cada cuba era constituída por um par de eletrodos inertes, continham soluções aquosas de AgNO3, KCl e Na2SO4 de mesma concentração e operaram durante um mesmo período de tempo em iguais condições.
A partir dessas informações, assinale V para a afirmativa verdadeira e F para a falsa.
( ) Na cuba I observa-se formação de gás no cátodo.
( ) Na cuba II o pH da solução aumenta ao longo do processo. ( ) Na cuba III um depósito sólido é formado no ânodo.
As afirmativas são, respectivamente,
Provas
Questão presente nas seguintes provas
Estereoisômeros apresentam propriedades químicas idênticas,
mas diferem quanto à propriedade física de girar o plano de luz
polarizada. Todavia, a síntese seletiva desses compostos é
complexa e, portanto, eles são frequentemente obtidos em
laboratório na forma de misturas racêmicas.
Considere a síntese em laboratório de uma molécula quiral que produziu uma mistura racêmica contendo 12,5% de cada estereoisômero.
A molécula sintetizada foi o
Considere a síntese em laboratório de uma molécula quiral que produziu uma mistura racêmica contendo 12,5% de cada estereoisômero.
A molécula sintetizada foi o
Provas
Questão presente nas seguintes provas
O cobalto-60, utilizado no tratamento de câncer, pode ser
preparado através de um processo denominado transmutação
induzida por nêutron.
Esse processo ocorre em três etapas e inicia-se a partir do ferro58. Na primeira etapa, o ferro-58 é convertido a ferro-59 pela
absorção de um nêutron. A segunda etapa consiste no
decaimento beta do ferro-59 para cobalto-59. Na etapa final, o
cobalto-59 absorve outro nêutron, sendo convertido a cobalto-60.
A reação global do processo de transmutação descrito pode ser representada po
A reação global do processo de transmutação descrito pode ser representada po
Provas
Questão presente nas seguintes provas
O cloreto de fosforila (POCl3), usado na síntese de ésteres, pode
sofrer decomposição segundo a reação abaixo.
2 POCl3(g) → 2 PCl3(g) + O2(g)
Nas condições-padrão a 298 K, a variação de entalpia (ΔH0 ) e a variação de entropia (ΔS 0 ) para esse processo valem, respectivamente, 572 kJ e 179 J/K. A partir das informações apresentadas, analise as afirmações a seguir.
I. O processo de decomposição do cloreto de fosforila é endotérmico. II. O processo leva à diminuição da desordem do sistema. III. O processo é não-espontâneo nas condições-padrão.
Está correto apenas o que se afirma em
2 POCl3(g) → 2 PCl3(g) + O2(g)
Nas condições-padrão a 298 K, a variação de entalpia (ΔH0 ) e a variação de entropia (ΔS 0 ) para esse processo valem, respectivamente, 572 kJ e 179 J/K. A partir das informações apresentadas, analise as afirmações a seguir.
I. O processo de decomposição do cloreto de fosforila é endotérmico. II. O processo leva à diminuição da desordem do sistema. III. O processo é não-espontâneo nas condições-padrão.
Está correto apenas o que se afirma em
Provas
Questão presente nas seguintes provas
Cadernos
Caderno Container