Foram encontradas 36.167 questões.
Antes do surgimento da indústria do petróleo no século XIX, o óleo de baleia era largamente utilizado para iluminação pública e fabricação de velas, por produzir uma chama limpa e duradoura. O palmitato de cetila (C32H64O2) é o principal componente do óleo extraído do crânio das baleias cachalotes.
Considere as equações termoquímicas a seguir e suas respectivas variações de entalpia em kJ/mol:
32C+32H2+O2 !$ \rightarrow !$ C32H64O2 !$ \Delta !$H = x
C + O2 !$ \rightarrow !$ CO2 !$ \Delta !$H = y
2CO +O2 !$ \rightarrow !$ 2CO2 !$ \Delta !$H = z
2H2 + O2 !$ \rightarrow !$ 2H2O !$ \Delta !$H = w
A expressão matemática para o cálculo do calor liberado à pressão constante (!$ \Delta !$Hr), durante a combustão incompleta de um mol do palmitato de cetila, com formação de monóxido de carbono, é
Provas
Os microrganismos são capazes de sintetizar substâncias que podem apresentar atividades biológicas interessantes. A estrutura química de um pigmento, denominado esclerotiorina, produzido pelo fungo Penicillium sclerotiorum, está representada a seguir.
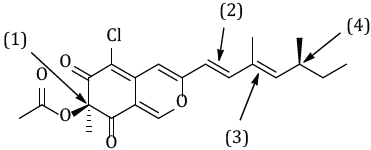
Fórmula estrutural da esclerotiorina
Nessa estrutura foram apontados dois átomos de carbono que são centros assimétricos (1 e 4) e duas duplas (2 e 3) que apresentam isomeria E/Z.
A configuração absoluta dos carbonos e a configuração das duplas ligações, de acordo com a sequência numérica, são
Provas
Preencha as lacunas do texto a seguir.
Para a descrição da molécula de BF3, pela Teoria da Ligação de Valência, é necessária a promoção de elétron (s) 2s para orbital (is) 2p e no B.
A sequência que preenche corretamente as lacunas é
Provas
Um laboratório de pesquisa procurava obter um composto molecular inédito por síntese orgânica.
Após obtenção e purificação do sólido, preparou-se uma solução com 4,0 g do produto em 100 mL de água. Essa solução apresentou ponto de ebulição igual a 100,5 °C à pressão de 1 atm. Considere a constante de elevação ebulioscópica da água igual a 0,51 K.kg/mol e sua densidade na temperatura do experimento igual a 1,0 g/mL.
Qual é a massa molar, em g/mol, determinada para o composto?
Provas
Leia o texto a seguir, a respeito de algumas reações que podem ocorrer com alcenos, e preencha as lacunas.
Os alcenos são substâncias muito reativas sob diversas condições de reação. Para a síntese de álcoois a partir de alcenos, sem que ocorram rearranjos, podemos empregar a reação de . Se o objetivo é formar um álcool a partir de uma reação de hidratação, onde o grupo hidroxila deve ser ligado ao carbono menos substituído, deve-se empregar a reação de . Na síntese de diois, deve-se usar o peróxido ácido meta-cloroperbenzoico (MCPBA) em meio ácido, para obtenção do produto de di-hidroxilação anti. Porém, se o objetivo é obter o produto de di-hidroxilação sin, deve-se empregar o (a) .
A sequência que preenche corretamente as lacunas do texto é
Provas
O nitrato de amônio é um dos fertilizantes mais conhecidos do mundo devido ao seu alto teor de nitrogênio e sua solubilidade em água.
Sobre as estruturas de Lewis dominantes dos íons amônio e nitrato, é correto afirmar que o (s)
Provas
Um sal, com propoção 1:1 entre seus íons, contendo o ânion cloreto, foi obtido por precipitação em condições ambientes, sendo seu Kps igual a 1,6x10-9. Após filtração, o sólido foi lavado com 100 mL de solução de HCl 1,0 mol/L para amenizar a solubilização do mesmo durante esse processo. Considere que o sal não sofre reação em meio ácido e que a concentração da solução ácida é muito maior que a solubilidade do sal nesse meio.
Comparando-se a solubilização do composto ao ser lavado com solução de HCl 1,0 mol/L com a solubilização que teria acontecido caso o sólido fosse lavado com 100 mL de água pura, em quantas vezes a solubilização do sólido foi diminuída graças à lavagem ter sido feita com a solução descrita?
Provas
Reações de desidratação podem levar à formação de uma variedade de alcenos, produtos dessa reação.
É possível prever qual será o produto principal para esse tipo de reação com base na análise dos intermediários de reação e na estabilidade do produto formado.
Observe a reação de desidratação do álcool a seguir:

O produto principal de desidratação para essa reação é
Provas
Experimentos como o do efeito fotoelétrico e de difração permitiram aos cientistas reverem suas concepções sobre a natureza da radiação eletromagnética e de partículas como o elétron. A dualidade onda-partícula passou a fazer parte da interpretação da matéria, revolucionando a concepção da estrutura atômica a partir do século XX.
Sobre a dualidade onda-partícula, avalie as afirmações a seguir.
I – O padrão de máximos e mínimos gerados pela interferência de um feixe de luz com um objeto gera a difração, fornecendo a evidência mais contundente de que a radiação eletromagnética se comporta como partícula.
II – Um cristal é capaz de difratar um feixe de elétrons a partir do seu arranjo regular dos átomos, dando suporte ao caráter ondulatório do elétron.
III – A colisão de um fóton com energia suficiente promove a ejeção imediata de um elétron, proporcionando suporte ao caráter de partícula da radiação eletromagnética.
IV – A energia cinética do elétron ejetado no efeito fotoelétrico aumenta linearmente com a frequência da radiação incidente, dando suporte ao comportamento ondulatório da radiação eletromagnética.
Está correto apenas o que se afirma em
Provas
Um frasco utilizado exclusivamente para descarte de soluções de sulfato de cobre, com diferentes concentrações, continha solução com concentração desconhecida. Para determinar a concentração dessa solução, montou-se uma pilha com eletrodos de cobre metálico na qual a solução com concentração desconhecida foi colocada no anodo e outra solução de Cu2+ com concentração exata de 1 mol/L foi colocada no catodo. Sabe-se que essa pilha apresentou o potencial global de + 0,0592 V.
Dado: E°red (Cu2+/Cu) = +0,34 V.
A concentração, em mol/L, da solução desconhecida é
Provas
Caderno Container